Клінічний випадок захворювання, підозрілого на хворобу Лайма, з незвичайними результатами серологічного обстеження
Практикуючому лікарю
УДК 616.98:579.834.114]-07:57.083.33
DOI : https://doi.org/10.61948/prevmed-2024-1-39
І. А. Зайцев
Національний медичний університет ім. О. О. Богомольця, м. Київ, Україна
Адреса для листування. Е-mail: for.prof.zaytsev@gmail.com
У статті наведено випадок захворювання, підозрілого на хворобу Лайма з незвичайними результатами серологічного обстеження: позитивними результатами дослідження на антитіла IgM та IgG до B. burgdorferi, отриманими методом блот-аналізу (WB), та негативними результатами обстеження методом імуноферментного аналізу (ІФА), що були зроблені пізніше у двох інших лабораторіях.
Розглянуто переваги двоетапної діагностики хвороби Лайма з послідовним використанням ІФА та WB і можливі наслідки діагностики захворювання з використанням тільки однієї лабораторної техніки. Звертається увага на відмінності в інтерпретації результатів WB згідно з критеріями Центру з контролю та профілактики захворювань (CDC, США) та виробників альтернативних тест-систем.
Розглянуто фактори, що можуть сприяти хибнопозитивним результатам обстеження: залежні від пацієнта (наявність супутніх ревматичних, інфекційних хвороб) та від помилкової інтерпретації результатів лабораторних досліджень (врахування слабопозитивних смуг як позитивний результат, наявність декількох смуг в межах однієї, нехтування незначним зміщенням смуги щодо її розташування у контролі тощо). Також звертається увага на вплив на результати дослідження наявності «анамнестичних» антитіл у певного відсотка людей, що проживають у ендемічних із хвороби Лайма областях.
Ґрунтуючись на наведених теоретичних положеннях, проведено ретельний аналіз щодо відповідності клінічних проявів випадку захворювання, що розглядається у статті, критеріям ранньої локалізованої форми хвороби Лайма. На підставі критеріїв, знайдених в наукових публікаціях, проведено клініко-епідеміологічне зіставлення даних пацієнтки з результатами лабораторного обстеження щодо їх достовірності.
Під час діагностики хвороби Лайма слід спиратись насамперед на клінічні дані, а результати лабораторного обстеження вважати додатковим підтвердженням діагнозу. Підкреслюється, що висока специфічність (98%) лабораторного обстеження забезпечується тільки завдяки двоетапному методу дослідження при послідовному використанні ІФА та WB. У випадку сумнівних результатів WB слід провести зіставлення клініко-епідеміологічних даних з результатами лабораторного обстеження щодо їх достовірності.
Ключові слова: Borrelia burgdorferi, діагностика, IgM IgG імуноблот, хвороба Лайма, серологія.
A clinical case of suspected lyme disease with unusual serological results
Bogomolets National Medical University, Kyiv, Ukraine
I.A.Zaytsev
The article presents a case of a disease suspected of Lyme disease with unusual results of serological examination: positive results of IgM and IgG antibodies to B. burgdorferi, obtained by the method of blot analysis (WB), and negative results of examination by the method of enzyme immunoassay (ELISA), which were made later in two other laboratories.
The advantages of the two-stage diagnosis of Lyme disease with the sequential use of ELISA and WB and the possible consequences of the diagnosis of the disease using only one laboratory technique are considered. Attention is drawn to differences in the interpretation of WB results according to the criteria of the Center for Disease Control (CDC, USA) and manufacturers of alternative test systems.
Factors that can contribute to false-positive examination results are considered: depending on the patient (the presence of concomitant rheumatic, infectious diseases) and on the erroneous interpretation of the results of laboratory tests (considering weakly positive bands as a positive result, the presence of several bands within one, neglecting a slight shift of the band in relation to its location in control, etc.). Attention is also drawn to the impact on the results of the study of the presence of «anamnestic» antibodies in a certain percentage of people living in areas endemic for Lyme disease.
Based on the above theoretical propositions, a thorough analysis was carried out regarding the compliance of the clinical manifestations of the case of the disease considered in the article with the criteria of the early localized form of Lyme disease. On the basis of the criteria found in scientific publications, a clinical and epidemiological comparison of the patient’s data with the results of laboratory examination was carried out regarding their reliability.
A conclusion is made regarding the need to rely on clinical data when diagnosing Lyme disease, and to consider laboratory examination results as additional confirmation of the diagnosis. It is emphasized that the high specificity (98%) of the laboratory examination is ensured only due to the two-stage research method with the sequential use of ELISA and WB. In case of questionable WB results, clinical and epidemiological data should be compared with the results of laboratory examination for their reliability.
Key words: Borrelia burgdorferi, diagnosis, IgM IgG immunoblot, Lyme disease, serology.
Хвороба Лайма є найпоширенішим трансмісивним захворюванням в Україні. За 11 місяців 2022 р. в Україні було зареєстровано 3 671 випадок захворювання, за той самий час 2023 року — вже 4 734 (приріст 28,9%) [1]. За відсутності національних рекомендацій з цього захворювання, здається дуже важливим накопичення певних знань та обмін досвідом ведення складних для діагностики та лікування хворих з хворобою Лайма чи підозрою на неї. В даній статті проведено аналіз клінічного випадку захворювання, підозрілого на хворобу Лайма, з незвичайними результатами серологічного обстеження. Також наводяться літературні дані стосовно можливої інтерпретації отриманих результатів обстеження та альтернативного діагнозу.
Пацієнтка К., 1991 р. н., 26.05.23 помітила сверблячу пляму на передній поверхні лівої гомілки. За порадою дерматолога обстежилася на бореліоз. Методом вестерн-блот (WB) 28.05.23 виявлено антитіла IgM та IgG до B. burgdorferi. Дослідження методом ІФА, проведене 30.05.23 та 01.06.23 в іншій лабораторії, показало негативний результат. На думку пацієнтки, укус кліщем був можливий на початку травня (06.05.23), коли пацієнтка ходила у високій траві, хоча факту укусу комахи того дня не пам’ятає.
За словами пацієнтки, більше року тому теж могли бути укуси кліщів. З приводу артралгій, які турбують пацієнтку декілька років, неодноразово зверталась до ревматолога, однак, ані інструментально, ані лабораторно підтвердженого ушкодження суглобів встановлено не було. У зв’язку з викиднем, на підставі обстеження, гінекологом встановлено діагноз антифософліпідного синдрому.
При огляді 06.06.23 на передній поверхні лівої гомілки є пляма до 3-4 см в діаметрі з папулою в центрі. Центр плями забарвлений більш інтенсивно з ціанотичним відтінком. Розміри плями не змінилися з дати її появи. Аналізуючи даний випадок, слід звернути увагу на два аспекти: клінічний, тобто на відповідність проявів хвороби діагнозу хвороба Лайма, та лабораторний, щодо підтвердження діагнозу методом WB та його спростування методом ІФА.
Формально, є певні дані щодо хвороби Лайма, точніше її ранньої, локалізованої стадії, а саме — мігруючої еритеми (МЕ): укус кліща не виключено, інкубаційний період, хоча і довгий (20 днів), але можливий, в місці укусу є досить велика еритема. Оскільки пацієнтка зверталася до дерматолога, можна вважати, що альтернативні дерматологічні діагнози було виключено.
Наскільки вірогідним є клінічний діагноз? Пацієнтка не впевнена щодо укусу кліща, але, згідно з літературними даними, про укус кліща пам’ятають не більше 25% пацієнтів з еритемою. У цьому випадку все ускладнюється локалізацією еритеми. Підвищені шанси передачі інфекції виникають здебільшого тоді, коли кліщ був прикріплений до шкіри протягом більше 36 годин [2]. Вочевидь, що з цим критерієм є певні проблеми, бо важко уявити, що кліща протягом цього часу не помітили саме на передній поверхні гомілки. Тому, МЕ знаходять переважно в пахвовій западині, пахвинній ділянці, підколінній ямці чи лінії поясу або поруч із нею, тобто у таких місцях, де кліща важко одразу помітити. МЕ зазвичай повільно розширюється протягом декількох днів або тижнів, часто з просвітленням у центрі, і може досягати діаметра більше 20 см. І лише у перші дні МЕ може бути рівномірно червоною. Пацієнтку було оглянуто на 12-й день хвороби, і на цей час пляма була відносно невелика — до 3-4 см в діаметрі, без будь якого просвітлення в центрі. Навпаки, вона була більш інтенсивно забарвлена і в центрі плями була папула. І головне, що, за словами пацієнтки, розміри плями не змінилися з дати її появи. Також у пацієнтки не було таких конституціональних симптомів, як стомлюваність, нездужання, млявість, легкий головний біль, міалгії, артралгії, регіонарна лімфаденопатія, але ж вони не є обов’язковими.
Отже, сумнівний епідеміологічний анамнез, відносно тривалий інкубаційний період, відсутність динаміки у розвитку передбачуваної МЕ, говорить про те, що клінічно діагноз хвороби Лайма є малообґрунтованим.
Що можна сказати стосовно проведеного лабораторного обстеження хворої? По-перше, якщо діагноз МЕ не викликає сумнівів, то жодного лабораторного підтвердження хвороби взагалі не потрібно. Це пов’язано з тим, що у більшості випадків імуноглобуліни в крові на момент появи МЕ ще відсутні. По-друге, призначення антибіотиків впливає, з одного боку, на продукцію антитіл, з іншого — на переключення синтезу IgM на IgG. Оскільки таким способом негативний результат тесту не виключає діагноз, лабораторне обстеження хворих з очевидною МЕ не є обов’язковим. Слід зазначити, що у мешканців високоендемічних регіонів в крові можуть бути наявні антитіла внаслідок контакту зі збудником у минулому, що теж утруднює інтерпретацію результатів лабораторного обстеження.Але, якщо рішення про необхідність обстеження прийнято, то воно повинно бути проведено за певними правилами, а саме: за так званою двоетапною (двоступеневою) схемою [3]. Спершу призначається обстеження на наявність антитіл IgM та IgG методом ІФА, потім — підтверджуючий тест методом WB. Така стратегія тестування була запроваджена ще у 1995 році [4], оскільки з самого початку появи комерційних тест-систем стало зрозуміло, що їх чутливість загалом була адекватною, однак специфічність виявилася доволі низькою. Тобто використання тільки ІФА супроводжувалося великою кількістю хибнопозитивних результатів. Тому зараз, за наявності позитивного або сумнівного результату обстеження методом ІФА, хворих обстежують методом WB (рис. 1).

По-перше, це дає певну економічну ефективність, оскільки дослідження методом ІФА є дешевшим, ніж WB. По-друге, метод ІФА є більш чутливим, ніж WB, що дозволяє виявити якомога більше хворих. По-третє, використання WB, якому притаманна більша специфічність, дозволяє відхилити хибнопозитивні результати ІФА, отримані на першому етапі діагностики [5]. У такий спосіб специфічність двоетапного методу дослідження вдалося довести до більш ніж 98% [6].
Як ми знаємо, ці правила при обстеженні пацієнтки були порушені: спочатку було проведено дослідження методом WB, яке показало наявність як IgM, так і IgG, потім, двічі, в різних лабораторіях, — методом ІФА, який показав відсутність антитіл. Оскільки раніше було доведено, що клінічний діагноз хвороби Лайма є малоймовірним, питання стосовно результатів лабораторного обстеження слід сформулювати так: наскільки вірогідними можуть бути хибнопозитивні результати обстеження методом WB?
Висока специфічність WB досягається внаслідок визначення антитіл до окремих високоспецифічних антигенів B. burgdorferi. Згідно з рекомендаціями Центру з контролю та профілактики захворювань США (CDC), WB IgM вважається позитивним, якщо виявлено антитіла щонайменше до двох з трьох антигенів, що використовуються, а про наявність WB IgG — 5 із 10 (таблиця 1).
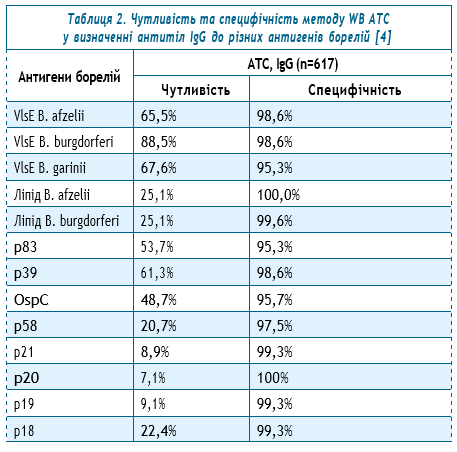
Використання WB як єдиного тесту різко зменшує число хворих, які можуть бути виявлені внаслідок відносно низької, порівняно з ІФА, чутливості WB (таблиця 2), та підвищує ймовірність хибнопозитивного результату. Такі результати можуть призвести до того, що люди лікуватимуться від хвороби Лайма, коли у них її немає, замість того, щоб лікувати справжню причину їхнього захворювання.
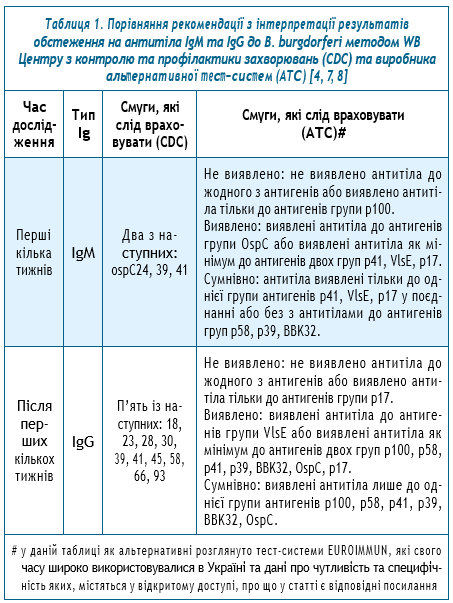
Протягом усього часу з моменту відкриття збудника у 1981 році, виробники діагностичних тест-систем намагалися підвищити точність діагностики захворювання. Процес йшов шляхом введення до тест-систем більш специфічних антигенів, у тому числі, рекомбінантних, та збільшення їх чисельності [9]. Все це, звісно, вплинуло на інтерпретацію результатів дослідження. Принцип залишився той самий — необхідна певна кількість смуг для того, щоб зробити висновок про наявність антитіл, але їх набір і кількість вже відрізняється від рекомендованого CDC і визначається суто виробником тест-системи (таблиця 1).
Іноді виробники АТС використовують відносно невелику кількість пацієнтів з хворобою Лайма та в контрольній групі для оцінки нових мультиантигенних аналізів та критеріїв їх інтерпретації. Porwancher R. зі співавт. порівняли два найбільш часто використовувані альтернативні критерії інтерпретації імуноблоту (А та В) з критеріями CDC, використовуючи дані з кількох схвалених Управлінням з санітарного нагляду за якістю харчових продуктів та медикаментів (США) наборів для WB IgG і IgM. Ці однорівневі альтернативні критерії інтерпретації продемонстрували значно більше хибнопозитивних або сумнівних результатів у здорових людей, ніж дворівневі критерії CDC (12,4% та 35,0% для тест-систем A та B відповідно порівняно з 1,0% за критеріями CDC). Через обмежену стандартизацію та високий рівень хибнопозитивних результатів, однорівневі альтернативні критерії інтерпретації WB, що оцінюються в даний час, поступаються дворівневим критеріям CDC [5].
Іншими причинами, що обмежують точність WB, є суб’єктивна інтерпретація отриманих результатів, а саме: визнання слабопозитивних смуг як позитивний результат, наявність декількох смуг у межах однієї, нехтування незначним зміщенням смуги щодо її розташування у контролі [8]. Дослідження, проведене у США, показало, що хибнопозитивні результати обстеження на IgM методом WB не обмежуються будь-якою комерційною лабораторією. Однак на долю двох комерційних лабораторій, які позиціонують себе як «спеціалізовані лабораторії для діагностики хвороби Лайма» і послугами яких широко користуються на північному сході США, припало 50% хибнопозитивних результатів досліджень. Ці лабораторії використовували критерії інтерпретації WB, відмінні від рекомендованих CDC [10]. Загалом WB дає більшу частоту хибнопозитивних результатів дослідження на IgM, ніж на IgG і характеризується низькою чутливістю для виявлення раннього захворювання [11]. Наприклад, включення результатів обстеження на наявність IgМ до інтерпретації зразків WB контрольної групи призвело до хибнопозитивних результатів у трьох з чотирьох досліджених лабораторій (показник 2,5–25%). Одна спеціалізована лабораторія, яка використовувала власні критерії інтерпретації наявності IgG або IgM, отримувала хибнопозитивні результати в 57% зразків із групи негативного контролю [12].
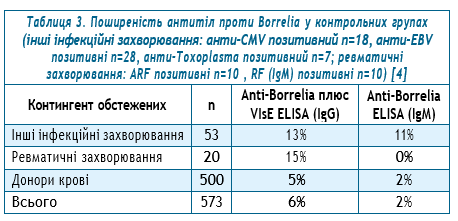
Наявність антитіл проти B. burgdorferi не повинна розглядатися у відриві від клінічної картини та епідеміологічних даних. Зокрема, у здорових донорів університетської клініки Любека (Німеччина) антитіла класу IgG визначалися у 5%, а IgM — у 2%, що, найімовірніше, пов’язано з субклінічною інфекцію у минулому або хибнопозитивними результатами дослідження. Але, у будь якому випадку, ці цифри можна розглядати як фонові для певної популяції. Наявність інших інфекційних захворювань збільшує ризик хибнопозитивних результатів ще десь на 8-9% щодо IgM та IgG. Передусім це стосується інфекційних агентів, які викликають поліклональну стимуляцію В-клітин, таких як вірус Епштейна-Барр [13]. Навпаки, наявність ревматичних захворювань, навіть з наявними антитілами IgM до ревматоїдного фактору, впливає переважно на хибнопозитивні результати визначення IgG (таблиця 3).

Отже, наведені вище дані переконливо доводять, що незважаючи на високу специфічність WB-аналізу, хибнопозитивні результати дослідження все ж таки можливі, а їх частота при використанні класичного підходу CDC оцінюється не менше ніж у 9% [14].
Цікавим, з погляду оцінки достовірності результатів обстеження методом WB на IgM до B. burgdorferi, є дослідження Seriburi V. зі співавт., де у 50 із 182 (27,5%, 95% ДІ: 21,1–34,6) пацієнтів, яких направили до приватної дорослої практики лікаря-інфекціоніста з приводу можливої хвороби Лайма, було виявлено хибнопозитивний WB IgM. 78,0% з цих пацієнтів отримували непотрібну антибіотикотерапію [15]. Спираючись на отримані дані, автори пропонують низку простих критеріїв щодо вирішення питання, чи є результат WB дійсним. На хибнопозитивні результати можуть вказувати: (А) Недотримання критеріїв CDC щодо серопозитивності, тобто, коли пропущено тест першого рівня (ІФА), або коли він був негативний, а WB виявився позитивним; коли симптоми тривають понад 4 тижні, а результат WB IgG залишається негативним; коли інтерпретацію WB проведено не відповідно до критеріїв CDC. Важливим епідеміологічним фактором, що вказує на хибнопозитивні результати дослідження на IgM методом WB, є відсутність виявлення кліща (Б). На це можуть вказувати позитивні результати тестування на IgM, що отримані в зимові місяці (в грудні, січні, лютому або березні). Коли людина була поза географічною зоною, де, як відомо, присутні кліщі-переносники. Клінічними критеріями (В), що свідчать на користь хибнопозитивного WB IgM, можуть бути симптоми, нетипові для ранньої локалізованої або ранньої дисемінованої хвороби Лайма, тобто відсутність уражень шкіри, подібних до мігруючої еритеми, гострого лихоманкового захворювання, менінгіту, паралічу черепних нервів, радикулопатії, ознак міокардиту; або взагалі відсутність будь яких симптомів. До лабораторних критеріїв, що свідчать про хибнопозитивні результати WB (Г), можуть бути віднесені негативні результати при повторному серологічному тестуванні протягом 4 тижнів після позитивного імуноблоту.
Якщо скористатися цими критеріями, то на користь хибнопозитивного результату дослідження на хворобу Лайма у нашої пацієнтки свідчать: (а) неправильно проведене обстеження (пропущений тест першого рівня (ІФА)), (б) двічі негативний ІФА за наявності позитивного WB; (в) відсутність виявлення кліща; (г) нетипові для ранньої локалізованої хвороби Лайма симптоми (невеликих розмірів пляма на 12-й день хвороби без тенденції до збільшення та без будь якого просвітлення в центрі, відсутність конституціональних симптомів). До цього можна додати, що позитивні результати дослідження WB на наявність IgM та IgG, отримані вже на 2-й день хвороби, теж свідчать на користь того, що вони є хибнопозитивними.
Ми розглянули декілька причин хибнопозитивних результатів на наявність антитіл до B. burgdorferi у нашої пацієнтки. Всі вони ґрунтуються на припущенні про порушення алгоритму діагностики або інтерпретації результатів дослідження. Але наш аналіз не буде повним, якщо не згадати про те, що хвора спостерігається в акушера-гінеколога з приводу викиднів, які пов’язують з наявністю у неї антифосфоліпідного синдрому. Згідно з даними O’Callaghan зі співавт., хибнопозитивні антитіла до збудника хвороби Лайма визначаються у 14% пацієнтів з первинним антифосфоліпідним синдромом [16]. І цей факт може бути ще однією причиною, яка пояснює хибнопозитивні результати обстеження хворої.
Якщо відкинути хворобу Лайма як причину клінічних проявів у хворої, а саме — еритеми, які можуть бути альтернативні діагнози?
Оскільки пацієнтка була оглянута дерматологом і дерматологічні діагнози були відхилені, слід розглянути інші можливості, насамперед — шкірну реакцію на укус комахи. Укуси комах можуть викликати кілька типів місцевих реакцій, папульозну кропив’янку або системні алергічні реакції. Інколи виникають інші форми таких системних реакцій, як сироваткова хвороба [17]. Реакція на укус комахи виникає здебільшого відразу після укусу, тому треба припустити, що пацієнтка була укушена незадовго до появи у неї еритеми. Знову ж таки, слід вважати, що укус комахи залишився непоміченим. Якщо взяти до уваги тривалість захворювання, то найбільш відповідним поясненням клінічної картини може бути укус москіта (рід Culicoides), які зустрічаються скрізь. Це крихітні сіро-чорні крилаті комахи менше 3 мм завдовжки, часто залишаються непоміченими. Місцеві реакції виникають зазвичай протягом однієї години після укусу. Потім можуть розгорнутись відстрочені системні та ізольовані відстрочені реакції, що складаються з сверблячих папул або везикул, які можуть зберігатися від тижнів до місяців [18, 19].
Виходячи з цього, пацієнтці було встановлено діагноз шкірної відтермінованої реакції на укус невідомої неотруйної комахи та призначено лікування антигістамінними препаратами і місцевими глюкокортикоїдами. Одужання настало протягом тижня.
Висновки:
- Під час діагностики хвороби Лайма слід відштовхуватися від клінічних даних. Результати лабораторного обстеження є додатковим підтвердженням діагнозу.
- Висока специфічність (98%) лабораторного обстеження забезпечується тільки завдяки двоетапному методу дослідження при послідовному використанні ІФА та
- У випадку сумнівних результатів WB слід провести зіставлення клініко-епідеміологічних даних з результатами лабораторного обстеження щодо їх достовірності. Автор заявляє про відсутність конфлікту інтересів та отримання будь-якого фінансування для написання даної статті.
Література
- Інфекційна захворюваність населення України за листопад 2022 — листопад 2023 р. Доступно на: https://phc.org.ua/kontrol-zakhvoryuvan/inshi-infekciyni-zakhvoryuvannya/ infekciyna-zakhvoryuvanist-naselennya-ukraini. Доступ: Січень 8,
- Lantos M., Rumbaugh J., Bockenstedt L. K. et al. Clinical Practice Guidelines by the Infectious Diseases Society of America (IDSA), American Academy of Neurology (AAN), and American College of Rheumatology (ACR): 2020 Guidelines for the Prevention, Diagnosis, and Treatment of Lyme Disease. Arthritis Care Res (Hoboken). 2021 Jan;73(1):1–9.
- Наказ МОЗ України №218 від 05.2005. Про посилення заходів з діагностики та профілактики іксодових кліщових бореліозів в Україні. Доступно на: https://ips.ligazakon.net/document/view/ MOZ4459?an=195. Доступ: Січень 8, 2024.
- Centers for Disease Control and Prevention Recommendations for test performance and interpretation from the Second National Conference on Serologic Diagnosis of Lyme MMWR. 1995; 44: 590-591
- Lyme disease. Nice Guideline. Available from: nice.org.uk/ guidance/ng95. Accessed: January 8, 2024.
- Moore , Nelson C., Molins C., Mead P., Schriefer M. Current Guidelines, Common Clinical Pitfalls, and Future Directions for Laboratory Diagnosis of Lyme Disease, United States. Emerg Infect Dis. 2016 Jul;22(7):1169–77.
- Mead , Petersen J., Hinckley A. Updated CDC Recommendation for Serologic Diagnosis of Lyme Disease. MMWR Morb Mortal Wkly Rep 2019; 68 :703.
- Differentiated Borrelia Diagnostics. Available from: https://www. com/ documents/Indications/Infections/Borrelia/ HI_2132_I_UK_C.pdf. Accessed: January 8, 2024.
- Porwancher ; Levin A.; Trevejo R. Immunoblot Criteria for Diagnosis of Lyme Disease: A Comparison of CDC Criteria to Alternative Interpretive Approaches. Pathogens 2023, 12, 1282.
- Feder M., Johnson B. J., O’Connell S. et al. A critical appraisal of “chronic Lyme disease”. N Engl J Med. 2007; 357: 1422-30
- Porwancher B., Hagerty C. G., Fan J., Landsberg L., Johnson J., Kopnitsky M., Steere A. C., Kulas K., Wong S. J. Multiplex immunoassay for Lyme disease using VlsE1-IgG and pepC10-IgM antibodies: improving test performance through bioinformatics. Clin Vaccine Immunol. 2011 May;18(5):851-9.
- Fallon A., Pavlicova M., Coffino S. W. et al. A comparison of Lyme disease serologic test results from 4 laboratories in patients with persistent symptoms after antibiotic treatment. Clin Infect Dis 2014; 59: 1705–10.
- Goosens H. A., Nohlmans M. K., Van Den Bogaard A. E. Epstein-Barr virus and cytomegalovirus infections cause false-positive results in IgM two-test protocol for early Lyme Infection. 1999; 27: 231
- Callister SM, Jobe DA, Agger WA, Schell RF, Kowalski TJ, Lovrich SD, Marks JA. Ability of the borreliacidal antibody test to confirm lyme disease in clinical practice. Clin Diagn Lab Immunol. 2002 Jul;9(4):908-12.
- Seriburi V., Ndukwe N., Chang Z., Cox M. E., Wormser G. P. High frequency of false positive IgM immunoblots for Borrelia burgdorferi in clinical Clin Microbiol Infect. 2012 Dec;18(12):1236-40.
- Dusse L., Silva F., Freitas L. et al. Antiphospholipid syndrome: a clinical and laboratorial Rev Assoc Med Bras 2014; 60(2):181-186пееее
- Vander Does A., Labib A., Yosipovitch G. Update on mosquito bite reaction: Itch and hypersensitivity, pathophysiology, prevention, and Front Immunol. 2022 Sep 21; 13:1024559.
- Lee F., Yang K. J., Wang N. M., Chiu Y. T., Chen P. C., Chen Y. H. The development of a murine model for Forcipomyia taiwana (biting midge) allergy. PLoS One. 2014 Mar 20;9(3): e91871.
- Adkinson N. F., Bochner B. S., Burks A. W. рet al. Middleton’s Allergy: Principles and Practice, Eighth Edition, Elsevier, 2013
Відомості про авторів:
Зайцев І. А. — д. м. н., професор кафедри терапії, інфекційних хвороб та дерматовенерології ПДО НМУ ім. О. О. Богомольця, бульвар Тараса Шевченка, м. Київ, 13, 01601, Україна; Телефакс: +380 (44) 234-92-76;
e-mail: for.prof.zaytsev@gmail.com; ORCID 0000-0003-1943-3511
Information about the authors:
Zaytsev I. A. — MD, PhD, Professor, Department of Therapy, Infectious Diseases and Dermatovenerology Postgraduate Education, Bogomolets National Medical University.
e-mail: for.prof.zaytsev@gmail.com; ORCID 0000-0003-1943-3511
