Від епідемій минулого до сьогодення і хвороби х, досвід боротьби та перспективи
УДК 616-036.22:311.219.1.+17.024.4
DOI : https://doi.org/10.61948/prevmed-2024-1-3
ДУ «Інститут епідеміології та інфекційних хвороб ім. Л. В. Громашевського НАМН України», Київ
З епідеміями та пандеміями люди стикалися з давніх часів, ще не розуміючи ні їхню природу, ні наслідки, ні як вберегтися та запобігти розповсюдженню. Кожна інфекційна хвороба має свої історію, особливості, пов’язані з вірулентністю збудника, механізмом його передачі, контагіозністю, від яких залежать епідемічний потенціал, інтенсивність епідемічного процесу, наслідки для кожного індивідуума і суспільства загалом. Щороку з’являються нові мікроорганізми людини, серед яких провідна роль належить вірусам, формуються нові або набувають змін вже існуючі паразитарні системи, в яких людина стає біологічним хазяїном того чи іншого патогену. Показано, що зоонозні мікроорганізми превалюють серед патогенів людини, зокрема серед емерджентних. Серед патогенів з епідемічним і пандемічним потенціалом переважають віруси. У статті розглянуто хронологію великих епідемій та пандемій, починаючи від невідомої хвороби в Китаї 5 000 років тому і закінчуючи мавпячою віспою, поширення якої почалося в травні 2022 року. Значна увага приділена теперішнім інфекційним хворобам із пандемічним потенціалом, а саме: зоонозному грипу, емерджентним коронавірусним інфекціям (SARS, MERS, COVID-19), хворобам Ебола і Зіка, реемерджентній мавпячій віспі. Надано перелік 10 потенційно пандемічних інфекційних хвороб, що ВООЗ визначила як пріоритетні, до якого також входить хвороба Х. Зазначено, що натепер відбувається підготовка до прийняття Конвенції ВООЗ, угоди чи іншого міжнародного документа щодо запобігання пандемії, готовності та відповіді, проєкт якої проходить етап узгодження. Наголошується, що національна система біобезпеки України потребує суттєвого вдосконалення в напряму посилення системи епідеміологічного нагляду за інфекційними хворобами.
Ключові слова: епідемія, пандемія, емерджентна інфекція, патоген, MERS, COVID-19, мавпяча віспа, хвороба Х.
I. Zadorozhna, V. R. Shahinian, N. P. Vynnyk
From the epidemics of the past to the present and disease x, experience of the fight and perspectives
State Institution “L. V. Hromashevskyi Institute of Epidemiology and Infectious Diseases of National Academy of Medical Science of Ukraine”, Kyiv
People have faced epidemics and pandemics since ancient times, without yet understanding either their nature, their consequences, or how to protect themselves and prevent their spread. Each infectious disease has its own history, features related to the virulence of the pathogen, the mechanism of its transmission, contagiousness, which depend
on the epidemic potential of the pathogen, the intensity of the epidemic process of infection, and the consequences for each individual and society in general. Every year, new human microorganisms appear, among which viruses play a leading role, new parasitic systems are formed or already existing parasitic systems change, in which a person becomes the biological host of one or another pathogen. It is shown that zoonotic microorganisms prevail among human pathogens, in particular among emergent ones. Viruses predominate among pathogens with epidemic and pandemic potential. The article examines the chronology of major epidemics and pandemics, starting with an unknown disease in China 5,000 years ago and ending with monkeypox, the spread of which began in May 2022. Considerable attention is paid to current infectious diseases with pandemic potential, namely zoonotic influenza, emerging coronavirus infections (SARS, MERS, COVID-19), Ebola and Zika diseases, re-emerging monkeypox. A list of 10 potentially pandemic infectious diseases, which WHO has identified as priority, is provided, which also includes disease X. Taking into account the lessons of the COVID-19 pandemic, all countries, including Ukraine, need to make a lot more efforts to achieve a truly adequate level of preparedness for preventing biological threats and responding to future challenges. It is noted that preparations are currently underway for the adoption of the WHO Convention, an agreement or another international document on pandemic prevention, preparedness and response, the draft of which is currently undergoing the coordination stage. The implementation of its provisions at the international and national levels will contribute to increasing the effectiveness of international and national biosecurity systems and strengthening the potential for combating biological threats. It is emphasized that the national biosafety system in Ukraine needs significant improvement in the direction of strengthening the system of epidemiological surveillance of infectious diseases.
Key words: epidemic, pandemic, emergent infection, pathogen, MERS, COVID-19, monkeypox, disease X.
Інфекційні хвороби супроводжують людство від початку його існування. З епідеміями та пандеміями люди також стикалися з давніх часів, спочатку не розуміючи ні їхню природу, ні наслідки, а найголовніше — у який спосіб вберегтися та запобігти розповсюдженню. Наприклад, про поліомієліт як давню хворобу, нам нагадує кам’яна стела, яку знайшли в Мемфісі (столиці Стародавнього Єгипту). На ній зображено жерця із залишковими явищами поліомієліту. За давністю вона належить до 1400-х років до н. е. А перший великий спалах цієї хвороби був описаний у США (132 випадки) у 1894 році. Надалі в 1916 р. лише в Нью-Йорку було зареєстровано понад 9 000 випадків поліомієліту [1, 2]. Найбільшого розповсюдження ця хвороба набула після Другої світової війни, залишаючи після себе дітей-інвалідів, що заставило швидко винайти засоби профілактики, а саме: вакцини (живу поліомієлітну вакцину Себіна та інактивовану — Солка), а в подальшому досягти зниження захворюваності на 99% та припинення циркуляції «дикого» поліовірусу в 5 із 6 регіонів ВООЗ.
Кожна інфекційна хвороба має свою історію, свої особливості, пов’язані з вірулентністю збудника, механізмом його передачі, контагіозністю, від яких залежать епідемічний потенціал патогена, інтенсивність епідемічного процесу інфекції, наслідки для кожного індивідуума і суспільства загалом. Щороку з’являються нові мікроорганізми, які викликають захворювання у людини, формуються нові або набувають змін вже існуючі паразитарні системи, в яких людина стає біологічним хазяїном того чи іншого патогену. Серед нових для людини інфекційних агентів провідна роль належить вірусам.
За останні 5 десятиліть з’явилося багато нових вірусів, які мають великий вплив на системи охорони здоров’я в усьому світі. Більшість «нових» інфекцій ймовірно викликано патогенами, які вже існували раніше, й отримали вибіркову перевагу через набуття можливості інфікувати популяції нових біологічних хазяїв. Для близько 80% відомих вірусів людини природним резервуаром є сільськогосподарські ссавці та свійська птиця, меншою мірою — дикі тварини та членистоногі. За оцінками, зоонозні інфекційні агенти становлять близько 60% відомих патогенів людини та до 75% «нових» патогенів людини [3]. У XXI столітті ці захворювання стають все більш серйозною глобальною проблемою через їхні наслідки для здоров’я та економіки як у розвинених, так і в країнах із обмеженими ресурсами [4].
Шотландські дослідники M. Woolhouse та E. Gaunt відзначають 4 ознаки, які, на їх думку, описуватимуть більшість майбутніх нових патогенів: переважання РНК-вірусів; патогени з резервуарами серед тварин; патогени із широким колом хазяїв; патогени з деяким (можливо, спочатку обмеженим) потенціалом їх передачі від людини до людини. Вони зазначають, що натепер близько 1 400 патогенів інфікують людину, із яких 500 можуть передаватися від людини до людини, серед них менше 150 потенційно здатні викликати епідемічні або ендемічні захворювання. Водночас триваючі глобальні екологічні зміни будуть сприяти появі нових інфекційних хвороб зі значною швидкістю — приблизно 3 хвороби на рік [5].
Надзвичайно серйозний урок людству надала пандемія COVID-19, забравши понад 7 млн життів, поєднавши світ однією проблемою та роз’єднавши обмежувальними заходами, змінивши в багатьох напрямах традиційні принципи біоетики та націливши людство на активну протидію майбутнім біологічним загрозам, ризики яких, на жаль, продовжують зростати.
Як з’ясувалося, жодна країна світу не була готова до такого виклику, як пандемія COVID-19. У жовтні 2019 р. у Глобальному індексі безпеки охорони здоров’я, виданому Школою громадської охорони здоров’я Блумберга при Університеті Джонса Хопкінса, США та Великобританія очолили список зі 195 країн, що вважалися найбільш підготовленими до «швидкого реагування» на біологічні виклики. Однак на практиці, ці країни показали високий рівень захворюваності та смертності від цієї інфекції. Зокрема, у США зареєстровано найвищий рівень смертності від COVID-19 на душу населення — більш ніж 700 000 смертей на початок жовтня 2021 року. Україна в Глобальному індексі безпеки за показником «швидке реагування та протидія поширенню епідемії» займала лише 100-е місце [6]. Мета роботи: провести в історичному аспекті аналіз деяких відомих епідемій та пандемій, зокрема і з позиції розвитку протиепідемічних і профілактичних заходів, оцінити сучасні епідемічні ризики щодо емерджентних і реемерджентних інфекцій та готовність доналежної їм протидії.
Деякі з найстрашніших епідемій і пандемій в історії прирекли цілі цивілізації та поставили на коліна колись могутні країни, забравши мільйони життів. Хоча нові спалахи хвороб все ще загрожують людству, завдяки досягненням сучасної епідеміології та інших наук є шанс сподіватися, що ми більше не стикнемося з такими жахливими наслідками, як колись наші предки [7]. Водночас пандемія COVID-19 показала свій руйнівний потенціал і неготовність до таких масштабних викликів систем охорони здоров’я навіть найбільш розвинутих країн світу, забравши близько 7 млн життів, і це лише за офіційними даними, які набагато нижче фактичних.
Нижче ми наводимо хронологію епідемій і пандемій зі скороченими їхніми характеристиками, з якими довелося і доводиться стикатися людству, і в процесі протидії яким формувалися протиепідемічні та профілактичні заходи, а також виникла і розвивається наука епідеміологія.
Ці дані (табл.) опрацьовані на підставі аналізу наукових та аналітичних джерел [7–22] та представлені в інтерпретації авторів роботи, виходячи із їхнього власного досвіду та погляду на проблему.
Етіологію всіх епідемій та пандемій минулого натепер не завжди можливо достовірно диференціювати, зокрема бубонної чуми і натуральної віспи, які асоціювалися у людей із «чорною смертю». Тим паче, що епідемії різних інфекцій змінювали одна одну, а інколи могли поширюватися одночасно. Ніхто не міг тоді достовірно оцінити розповсюдженість захворювань та втрати від них. Тому наведені в таблиці історичні дані треба сприймати як інформацію, що висвітлює значення інфекційних хвороб для людства з погляду не тільки впливу на здоров’я, а й на розвиток цивілізацій, медицини, протиепідемічних та профілактичних заходів та загалом системи біологічної безпеки в глобальному розумінні.
Найбільш вагомі пандемії та епідемії, з якими стикнулося людство
| № з/п | Місце виникнення | Хвороба | Період часу | Додаткова інформація |
|---|---|---|---|---|
| 1 | Китай | Невідомо | Близько 5 000 років тому | Епідемія знищила цілий регіон в Китаї. Тіла померлих спалили в будинках. Там знайшли скелети різного віку: неповнолітніх, людей молодого і середнього віку. |
| 2 | Греція | Черевний тиф, або геморагічна гарячка | 430 років до н. е. | Епідемія тривала 5 років і спустошила Афіни. Кількість жертв могла досягати 100 тисяч. Грецький історик Фукідід писав про симптоми епідемії. |
| 3 | Римська імперія | «Антонінова чума», або «чума Галена» (можливо, натуральна віспа) | 165–180 рр. н. е | Спустошила римську армію та, можливо, знищила понад 5 млн осіб у Римській імперії. «Антонінова чума» могла створити умови для занепаду Римської імперії. |
| 4 | Єгипет, Рим | «Чума Кипріяна» | 250–271 роки н. е. | Названа на честь св. Кипріяна, єпископа Карфагена. За оцінками, лише в Римі помирало 5 тис. людей на день. Тіла покривали товстим шаром вапна та спалювали. |
| 5 | Єгипет, Візантійська імперія, і інші регіони | «Чума Юстиніана» | 541–542 роки н. е. | Візантійська імперія була спустошена епідемією чуми, що поклала початок її занепаду. За деякими оцінками, загинуло до 10% населення світу. |
| 6 | Абіссінія, Іспанія, європейське Середземномор’я, Японія, Америка | Натуральна віспа | З VI століття | Від VI ст. віспа фігурує під її латинською назвою variola. Запровадження методу варіоляції у XVIII ст. сприяло запобіганню хворобі. |
| 7 | Азія, Європа | «Чорна смерть» (чума) | 1346–1353 рр. | Хвороба розповсюдилася з Азії до Європи, змінивши перебіг історії Європи. Померло близько 25–30 млн людей, що складало 30–50% населення. |
| 8 | Мексика, Гватемала, Центральна Америка | «Коколідзлі» (геморагічна гарячка або паратиф) | 1545–1548 рр. | Епідемія знищила 15 млн жителів Мексики та Центральної Америки. «Cocoliztli» — ацтекське слово, що означає «шкідник». Спочатку підозрювали, що це була геморагічна гарячка, але теперішні дослідження ДНК зі скелетів померлих ідентифікували Salmonella paratyphi C. |
| 9 | Америка | Епідемії «Американської чуми» (збірне поняття, зокрема і натуральна віспа) | XVI століття | Поняття цих епідемій стосувалося групи євразійських хвороб, завезених європейцями. Ці хвороби, у тому числі віспа, сприяли краху цивілізацій інків та ацтеків. За деякими оцінками, 90% корінного населення Західної півкулі було втрачено. Крім того, армії ацтеків та інків були спустошені хворобами та не змогли протистояти іспанським військам. |
| 10 | Англія | «Велика лондонська чума» | 1665–1666 рр. | Чума почалася у квітні 1665 р. і швидко поширилася протягом спекотних літніх місяців. Передача збудника відбувалася через блох від інфікованих гризунів. На момент закінчення епідемії померло близько 100 тис. осіб, у тому числі 15% населення Лондона. |
| 11 | Франція | «Велика марсельська чума» | 1720–1723 рр. | Епідемія чуми почалася, коли корабель із вантажем товарів зі східного Середземномор’я пришвартувався у Марселі. Хоча корабель знаходився на карантині, це не попередило епідемію. Чума швидко поширилася, і за наступні 3 роки у Марселі та прилеглих районах могло померти до 100 тис. осіб. За оцінками, померло до 30% населення Марселя. |
| 12 | Росія | «Російська чума» | 1770–1772 рр. | В охопленій чумою Москві терор громадян, які перебували на карантині, переріс у насильство. Заворушення поширилися містом і завершилися вбивством архієпископа Амвросія, який закликав натовпи не збиратися на богослужіння. Імператриця Катерина II намагалася стримати чуму і видала поспішний наказ перенести всі заводи з Москви. За оцінками, могло померти до 100 тис. осіб. |
| 13 | Сполучені Штати, Філадельфія | «Жовта лихоманка» | 1793 р. | Коли хвороба охопила Філадельфію (тодішню столицю США), помилково вважалося, що раби невразливі, тому закликали наймати людей африканського походження для догляду за хворими. Під час особливо спекотної та вологої літньої погоди у Філадельфії того року різко зросла популяція комарів — векторів збудника. Лише коли настала зима, епідемія припинилася. Померло понад 5 тис. осіб. |
| 14 | Починалися з Індії | 5 пандемій холери | 1817–1823 рр.; 1829–1851 рр.; 1852–1859 рр.; 1863–1875 рр.; 1881–1896 рр. | Пандемії холери спустошили багато регіонів світу. Найбільш смертоносною була епідемія 1852–1859 рр., що вразила Азію, Європу, Північну Америку та Африку. У 1883 р. Р. Кох виділив холерний вібріон. Під час спалаху в 1892 р. Гамбург втратив майже 1,5% населення. |
| 15 | Росія, далі всі регіони світу | Пандемія грипу | 1889–1890 рр. | Перші випадки зафіксовано в Росії. Вірус швидко поширився Європою та світом, навіть за відсутності авіаперевезень. За кілька місяців хвороба охопила всю земну кулю, померло близько 1 млн осіб. Епідемія досягла піку летальності за 5 тижнів. |
| 16 | Почалася з Індії | 6-а пандемія холери | 1899–1923 рр. | Значною мірою не торкнулася Західної Європи та Північної Америки через досягнення в медицині та санітарії. Але хвороба все ще спустошувала Індію, Росію, Близький Схід та Північну Африку. Протягом 1918–1919 рр. в Індії померло понад 500 тис. осіб. |
| 17 | Сполучені Штати | Епідемія поліомієліту | 1916 р. | Епідемія поліомієліту, що почалася в Нью-Йорку, призвела до 27 тис. випадків захворювання та 6 тис. смертей у США. |
| 18 | Усі регіони світу | Пандемія «Іспанського грипу» | 1918–1920 рр. | За оцінками, 500 млн людей у світі захворіли. Померло 50–100 млн (3–5% населення світу), а деякі корінні громади опинилися на межі зникнення. Розповсюдженню грипу та летальності сприяли обмежені умови утримання солдатів та погане харчування під час Першої світової війни. Незважаючи на те, що хвороба швидше за все, почалася не в Іспанії, назва «Іспанський грип» прижилася. |
| 19 | Китай, Сінгапур, Гонконг | Пандемія «Азіатського грипу» | 1957–1958 рр. | Збудник — вірус-реассортант вірусів пташиного грипу. Загальна кількість померлих у світі становила понад 1,1 млн, причому 116 тис. випадків — у США. |
| 20 | Почалася з Індонезії | 7-а пандемія холери | Із 1961 р. по теперішній час | Поширилася Азією та Близьким Сходом, досягнувши в 1971 р. Африки. У 1991 р. після 100-річної відсутності холера повернулася до Південної Америки. У 1-й рік у Перу померло 3 тис. осіб. Пандемія торкнулася близько 120 країн, переважно менш розвинутих. У 2008–2009 рр. — спалах у Зімбабве (захворіло близько 97 тис., померло 4,2 тис. осіб), у 2010–2011 рр. спалах на Гаїті (захворіло понад 500 тис. осіб). |
| 21 | Гонконг, Китай, Сінгапур, Малайзія, Філіппіни, В’єтнам із подальшим поширенням | Пандемія «Гонконгського грипу» | 1968–1969 рр. | Викликана вірусом А(H3N2), який походить від А(H2N2), що спричинив пандемію в 1957–1958 рр. через антигенний шифт. Померло від 1 до 4 млн осіб. Натепер цей вірус є одним із етіологічних агентів сезонного грипу. Летальність становила 0,2%. |
| 22 | Глобальне поширення | ВІЛ-інфекція/СНІД | Із 1981 р. | Набув характеру глобальної пандемії. Забрав близько 35 млн життів з моменту його першого виявлення. Нині близько 64% із приблизно 40 млн людей, які живуть із ВІЛ, проживають у країнах Африки на південь від Сахари. Натепер існують ефективні ліки, що припиняють передачу вірусу. |
| 23 | Китай + 25 країн 5 континентів | Епідемія SARS | 2002–2003 рр. | Новий коронавірус циркулював із листопада 2002 по липень 2003 року. Природними хазяями визнано віверру цибетову (родина котячих) та кажанів. Викликав атипову пневмонію. Захворіло 8 096 осіб у 26 країнах, померло — 774, летальність — 9,6%. |
| 24 | Мексика, Сполучені Штати з подальшим поширенням | Пандемія свинячого/каліфорнійського грипу А(H1N1) (вірус А(H1N1) pdm09) | 2009–2010 рр. | Пандемія була викликана новим вірусом, який сформувався в Мексиці навесні 2009 р., а потім поширився на решту світу. Вірус виявився четвертинним реассортантом свинячого вірусу грипу А, який мав гени вірусів грипу людини, птиці та 2 ві- русів свиней. Згідно з даними CDC, за рік у світі інфікувалося 1,4 млрд осіб і померло від 151,7 до 575,4 тис. осіб. Глобальна кількість смертей від цієї пандемії приблизно в 15 разів більша за лабораторно підтверджені випадки. 80% смертей припало на осіб молодших 65 років. Натепер цей грип набув характеристики сезонного. |
| 25 | Аравійський півострів + 26 країн | Близькосхідний респіраторний синдром (MERS) | Із 2012 р. | Із квітня 2012 р. до 12 лютого 2024 р. загалом було зареєстровано 2 621 випадок MERS, у тому числі 949 летальних (36,2%). |
| 26 | Західна Африка (Гвінея, Ліберія, Сьєрра-Леоне) | Епідемія хвороби Ебола | 2014–2016 рр. | Вірус відомий із 1976 року. Набув реемерджентних властивостей і викликав епідемію в Західній Африці в 2014–2016 рр. Понад 28,6 тис. осіб заразилися, 11,3 тис. померли (39,6%). Під час епідемії хвороба поширилася ще на 7 країн: Італію, Малі, Нігерію, Сенегал, Іспанію, Велику Британію та США. Вторинні інфікування відбулися в Італії, Малі, Нігерії та США. Вперше були застосовані вакцини за принципом «для емерджентного застосування». |
| 27 | Північна і Центральна Америка | Хвороба Зіка | 2015–2016 рр. | Як вірус, здатний викликати захворювання у людей, відомий з 1952 року. Вектор — комарі роду Aedes. Набув нових біологічних властивостей: здатності викликати мікроенцефалію у дітей при внутрішньоутробному інфікуванні, неврологічні ураження (синдром Гійєна-Барре), передаватися статевим шляхом та персистувати в репродуктивних органах чоловіків. У 2016 р. ризик уроджених дефектів у немовлят, пов’язаних із інфікуванням матерів вірусом Зіка, виріс у 20 разів. Основні заходи профілактики — боротьба з комарами та запобігання їхнім укусам. |
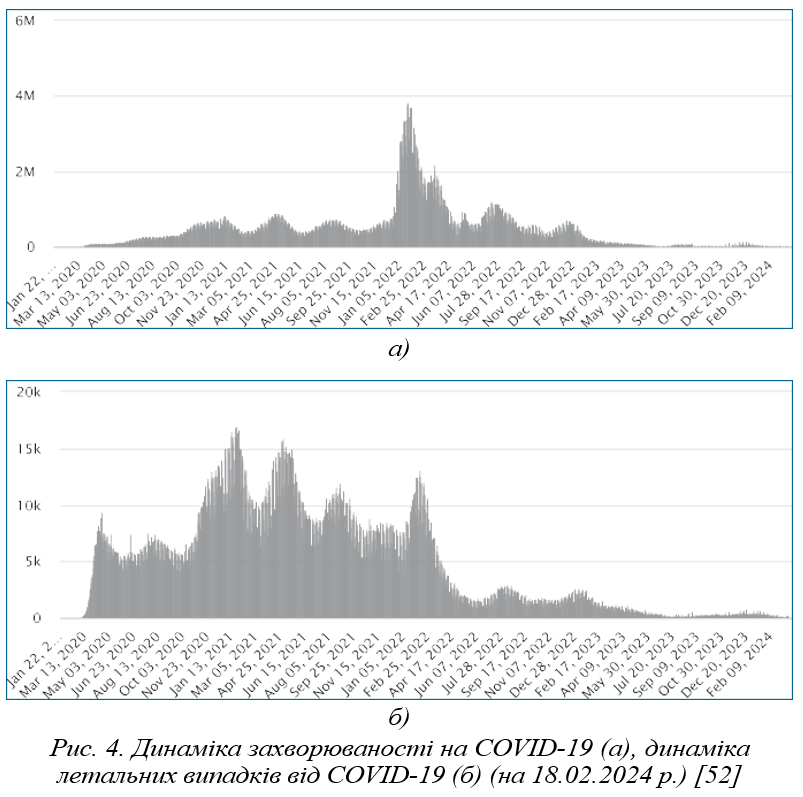
| 28 | Китай з подальшим поширенням | Пандемія COVID-19 | 2020–2023 рр. | На 11.02.2024 р. у світі офіційно зареєстровано 702 951 342 випадки, зокрема 6 981 061 летальний. Спостерігається швидка мутація вірусу SARS-CoV-2, поступове зниження вірулентності, зростання контагіозності та набуття хворобою характеристик сезонної інфекції. |
| 29 | 111 країн | Мавпяча віспа | 2022–2023 рр. | На 07.02.2024 р., починаючи з 2022 р., у 111 неендемічних країнах зареєстровано 91 373 випадки. 23.07.2022 р. ВООЗ було оголошено про надзвичайну ситуацію в галузі охорони здоров’я міжнародного значення. Провідною групою ризику є чоловіки, що мають секс із чоловіками, бісексуали, особи з багатьма сексуальними партнерами, переважно чоловічої статі. Однак сприйнятливими до вірусу є більшість населення світу. Летальність при реемерджентному варіанті вірусу — 0,17%. |
Епідемії проходили світом, знищуючи певну частку населення. Так звана «Антонінова чума» призвела в наступному до занепаду Римської імперії, а колонізація Американського континенту супроводжувалася поширенням нових для цього регіону інфекцій та втратою більшості корінного населення. Вивчаючи історію епідемій і пандемій, можна простежити, як поступово відбувалося сприйняття «заразності» тих хвороб, які нестримно розповсюджувалися і які називали «пошестю», і як на підставі багатовікового досвіту поступово впроваджувалися ті чи інші обмежувальні заходи. Зокрема, під час «чуми Кипріяна» (ІІІ ст. н. е.) тіла померлих від цієї хвороби покривали товстим шаром вапна та спалювали. Із Індії та Китаю (VІІІ–Х ст.) поширився метод профілактики натуральної віспи — варіоляція. У 1796 р. Дженнер вперше провів щеплення проти цієї інфекції, використавши вірус коров’ячої віспи, заклавши основи вакцинопрофілактики. Карантинні заходи застосовували вже у XVIII ст. проти чуми та в XIX ст. проти холери.
На жаль, у сучасний період епідемічні загрози продовжують залишатися надзвичайно актуальною проблемою. Періодично з’являються нові (емерджентні) для людини збудники, а деякі вже давно відомі та, начебто, взяті під контроль, знову починають розповсюджуватися і набувати характеристик реемерджентних. Нещодавно світ пережив безпрецедентну за масштабами і епідеміологічними особливостями пандемію COVID-19, новий збудник якої (коронавірус SARS-CoV-2) назавжди опанував людську популяцію як біологічного хазяїна, продовжуючи інтенсивно циркулювати і еволюціонувати. Протягом ХХ–ХХІ ст. епідемії та пандемії переважно були викликані вірусами. Винятки становлять 6-а і 7-а пандемії холери.
Холера. Загалом, ураховуючи динаміку захворюваності на холеру та її поширеність у різних регіонах світу, із початку XIX ст. визначено 7 пандемій цієї інфекції. Остання, що розпочалася в 1961 р., триває дотепер. Незважаючи на стрімкий розвиток медицини, зусилля національних систем охорони здоров’я, міжнародних організацій у боротьбі з інфекціями, зокрема й тими, що мають фекально-оральний механізм передачі збудника, у 2023 р. від холери, або так званої гострої водянистої діареї, у світі постраждало 708 200 людей, зокрема 4 300 померло, що значно більше, ніж у 2022 р. (472 697 випадків і 2 349 смертей відповідно). Така динаміка є досить тривожною. У 2023 р. випадки були зареєстровані в 30 країнах у 5 із 6 регіонів ВООЗ, включаючи 9 країн, в яких зафіксовано понад 10 000 випадків. Епідемічні ризики зберігаються і в 2024 р.: лише в січні було зареєстровано 40 900 випадків, зокрема 775 летальних, у 17 країнах 4 регіонів: Африканського, Східного Середземномор’я, Американського та регіону Південно-Східної Азії. На глобальну боротьбу з холерою впливає гостра нестача пероральних вакцин проти цієї інфекції. Із січня 2023 р. до січня 2024 р. потреба в них становила 76 млн доз при доступності лише 38 млн доз. У січні 2023 р. ВООЗ класифікувала глобальне поновлення холери як надзвичайну ситуацію 3-го класу, що є найвищим внутрішнім рівнем надзвичайних ситуацій [23].
ВІЛ-інфекція/СНІД. Ми не будемо зупинятися детально на всіх епідеміях та пандеміях, які супроводжували і супроводжують людство. Поступово ми бачимо, що бактеріальні хвороби, які мали виражений епідемічний потенціал і широке розповсюдження, витіснилися вірусними інфекціями. Про пандемію ВІЛ-інфекції/СНІДу існує багато окремих досліджень, а також чисельні публікації. Загалом 85,6 млн (65,0– 113,0 млн) осіб було інфіковано вірусом ВІЛ і близько 40,4 млн (32,9–51,3 млн) осіб померло від ВІЛ. Станом на кінець 2022 р. у світі 39,0 млн (33,1–45,7 млн) осіб жили з ВІЛ. За оцінками, 0,7% (0,6–0,8%) дорослих у віці 15–49 років у світі живуть з ВІЛ, хоча тягар цієї інфекції продовжує значно відрізнятися між країнами та регіонами. У 2022 р. від хвороб, пов’язаних з ВІЛ, загалом померло 630 000 осіб. Африканський регіон ВООЗ залишається найбільш постраждалим, де майже 1 з кожних 25 дорослих (3,2%) живе з ВІЛ, і на нього припадає більше двох третин осіб, які живуть із ВІЛ у всьому світі [24].
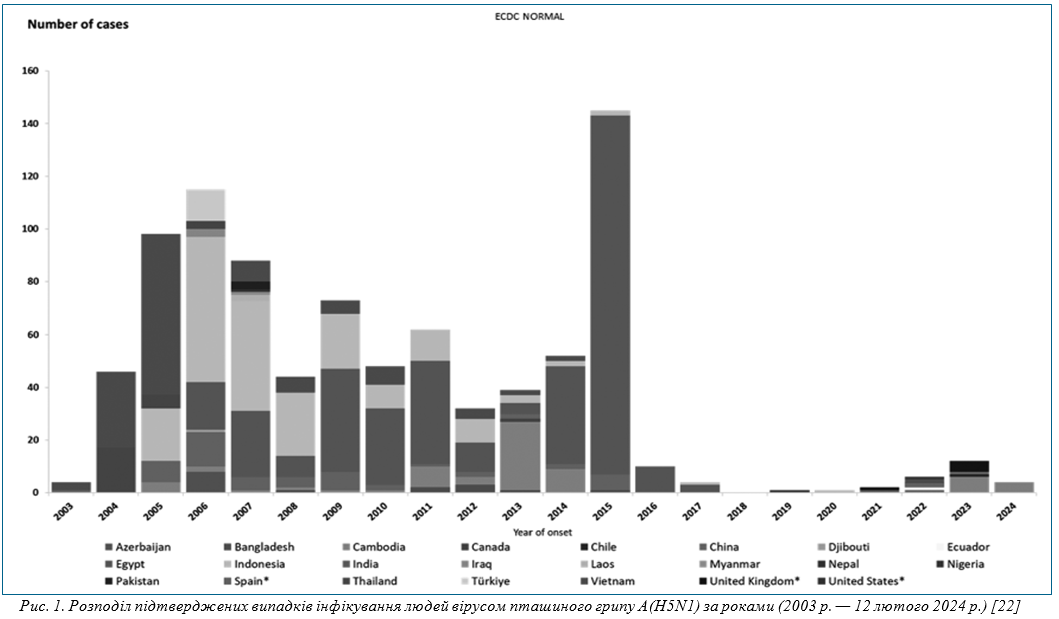
Грип. Із кінця XIX ст. світ пережив 5 пандемій грипу, останню — уже в нинішньому ХХІ столітті. Наприкінці ХХ ст. (із 1997 р.) почали реєструватися випадки грипу серед людей, викликані високопатогенним пташиним вірусом А(H5N1). Перші випадки виникли в Гонконзі на тлі спалаху серед свійської птиці. З метою його зупинки знищили 1,5 млн птиці. Зростання кількості випадків та розширення територій, де вони реєструвалися, певні генетичні ознаки адаптації вірусу до людського організму дали підставу прогнозувати, що наступна пандемія буде викликана саме цим вірусом [25–27]. Загальна кількість випадків протягом 1997–2023 рр. становила 902 із понад 50% летальністю [28]. Найбільша кількість випадків зареєстрована в період 2004–2015 рр., протягом 2016–2021 рр. був виражений період спаду захворюваності з наступним теперішнім підйомом (рис. 1) [22]. На підставі доступної інформації, на даний момент ВООЗ оцінює ризик цього вірусу для населення як низький.
Отже, попередні прогнози щодо пандемії пташи-
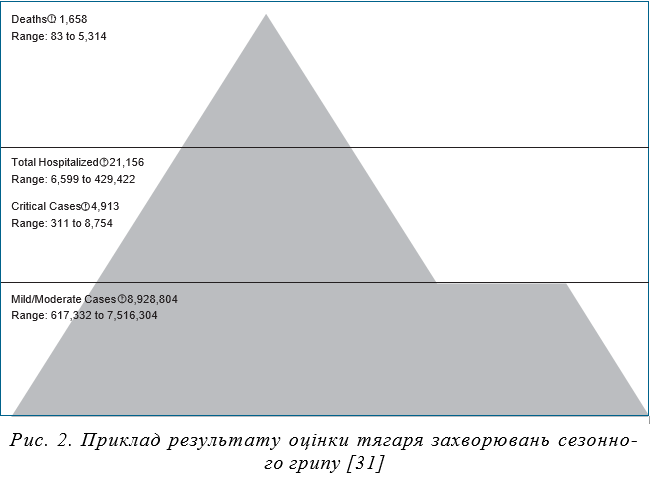
ного грипу не збулися, а в 2009–2010 рр. виникла пандемія свинячого або каліфорнійського грипу, викликана новим вірусом А(H1N1)pdm09, який виявився четвертинним реассортантом свинячого вірусу грипу А та мав гени вірусів грипу людини, птиці та 2 вірусів свиней, тобто містив унікальну комбінацію генів вірусів грипу, раніше не ідентифікованих у тварин або людей. Протягом 12 квітня 2009 р. — 10 квітня 2010 р., за оцінками CDC, у США було 60,8 млн випадків (діапазон: 43,3–89,3 мільйона), 274 304 госпіталізації (195 086–402 719) і 12 469 смертей (8 868–18 306). Щодо клінічної особливості відносно важкості перебігу слід відмітити той факт, що 87% смертей сталися серед осіб віком до 65 років, причому ризики госпіталізації та смерті у дітей та дорослих у 4–7 разів і 8–12 разів відповідно перевищували оцінки впливу сезонного грипу в 1976–2001 рр. [29]. Для оцінки глобального тягаря пандемії в 2009 р. було розраховано, що в цей час сталося 201 200 смертей, пов’язаних із респіраторною патологією (діапазон 105 700–395 600) та додатково 83 300 смертей (46 000–179 900), викликаних серцево-судинною патологією, які були наслідком пандемії. 80% смертей припадало на людей молодше 65 років, а 51% таких випадків сталися в Південно-Східній Азії та Африці [30]. Натепер ця емерджентна хвороба набула сезонного характеру і доповнила розмаїття вірусів, що викликають гострі респіраторні захворювання, а її збудник увійшов до складу сезонних вакцин. Вірус А(H1N1)pdm09 у процесі циркуляції, як й інші віруси грипу, змінює свої антигенні властивості, що потребує відповідного постійного моніторингу та періодичної заміни вакцинних штамів на актуальні. Водночас сезонний грип, епідемічні підйоми якого ми спостерігаємо восени і взимку, а іноді ускладнення епідемічної ситуації може тривати й до весни, також є важким тягарем для суспільства і систем охорони здоров’я країн [31] (рис. 2). Кількість легких і середньої тяжкості випадків щорічно у світі може сягати близько 9 млн, важких і критичних, що потребують госпіталізації, — понад 20 тис. (6 599 — 429 422), летальних випадків — понад 1 600 (83–5 314). Отже, незважаючи на існування ефективних вакцин проти сезонного грипу, ефективних противірусних препаратів, епідемічний процес грипу не знижує своєї інтенсивності, продовжує забирати життя, впливаючи на економіку країн внаслідок ураження працездатного населення.
Крім зазначених вище нових вірусів грипу, протягом останніх 25 років стало відомо й про здатність інших пташиних вірусів грипу викликати захворювання у людини: А(H9N2) (1998), А(H7N7) (2003), А(H7N3), А(H10N7) (2004), А(H7N9), А(H10N8) (2013), А(H5N6) (2014), А(H7N4) (2018), А(H10N3), A(H5N8) (2021), А(H3N8) (2022), А( H10N5) (2023). Про новий вірус А(H10N5) у
Китаї ВООЗ повідомила нещодавно — 13.02.2024 р. [32]. Це був вперше виділений від людини вірус грипу цього підтипу — у пацієнтки віком 60 років, яка мала контакт із хворою птицею. Крім того, в неї одночасно було визначено і сезонний вірус А(H3N2). Зазначене є ще одним підтвердженням постійного існування ризиків формування вірусів-реассортантів, які можуть у подальшому набути епідемічного потенціалу.
Привертає увагу той факт, що за останні 3 роки, тобто під час пандемії COVID-19 (2021–2023 рр.) було відкрито 4 нових пташиних віруси грипу, здатних викликати захворювання у людей. Із 2018 р. по 13.02.2024 р. серед людей зареєстровано 174 випадки пташиного грипу, із них 130 (75%) — протягом 2021–2023 рр. [33]. Це пов’язано з декількома факторами. З одного боку — із збільшенням виробництва птиці та комерційної торгівлі; зростанням ролі диких птахів, що зумовлено їх періодичною міграцією, зокрема й інфікованих птахів; зміною в моделях міграції через зміну клімату або залучення нових земель під сільськогосподарську діяльність [34]. З іншого — із підвищенням ефективності епідеміологічного нагляду під час пандемії COVID-19 за тяжким гострим респіраторним синдромом, тяжкими гострими респіраторними інфекціями та грипоподібними захворюваннями. Високу загрозу щодо формування епідемічно значущих вірусів грипу становить вірус свиней. Однак кількість підтипів вірусу свиней, на відміну від пташиних вірусів, лише три — А(H1N1)v, А(H1N2)v, А(H3N2)v. Протягом сезонів 2017/2018–2022/2023 рр. зареєстровано 49 випадків зоонозного грипу у людей, викликаних цими вірусами. Найбільша кількість випадків свинячого грипу, так само, як і пташиного, була зареєстрована в період пандемії COVID-19 (61%). На початку 2024 р. ВООЗ уже повідомила про 3 випадки, які сталися в Бразилії, Іспанії та Китаї [32, 35, 36]. Окремо треба наголосити також на тому, що свині, як біологічна популяція, розглядаються як природний потенційний резервуар для формування нових реассортантів вірусів грипу.
У 2022 р. виповнилося 70 років Глобальній системі епідеміологічного нагляду за грипом та реагування на нього [37]. Завдяки її функціонуванню відбувається постійний моніторинг циркулюючих вірусів грипу, як сезонних, так і зоонозних. Це дозволяє відбирати віруси-кандидати для вакцин. Штами сезонних вірусів використовуються для сезонних вакцин з урахуванням прогнозів щодо епідемічної значущості тих чи інших антигенних варіантів вірусів. Віруси-кандидати для вакцин проти зоонозного грипу зберігаються на випадок загострення епідемічної ситуації, тобто, якщо той чи інший зоонозний вірус грипу набуде здатності до стійкої передачі від людини до людини, або використовуються для виготовлення вакцин для застосування у тварин.
Проте наскільки проблема зоонозного грипу актуальна з погляду його пандемічних ризиків, свідчить прийняття ВООЗ Плану високого рівня впровадження III Рамкової програми підготовки до пандемії грипу на 2024–2030 рр., в якому з урахуванням досвіду пандемії COVID-19 наголошується на посиленні епідеміологічного нагляду, технічному оснащенні його вірусологічної складової, зокрема геномного секвенування, та удосконаленні вакцинних технологій [38].
Тяжкий гострий респіраторний синдром. У 2002 р. неочікуваною загрозою стала емерджентна коронавірусна інфекція, викликана новим для людини вірусом, який натепер називається SARS-CoV-1, що викликав тяжкий гострий респіраторний синдром, тобто атипову пневмонію. Хвороба розпочалася в Китаї та розповсюдилася ще на 25 країн. Хоча циркуляція вірусу припинилася в 2003 р., загальна кількість захворілих досягла 8 096 осіб, із яких 774 померло (9,6%). Циркуляція поступово припинилася, нова паразитарна система проіснувала недовго, вірус не закріпився в популяції нового для нього біологічного хазяїна, зник як біологічний вид і натепер не визначається [12].
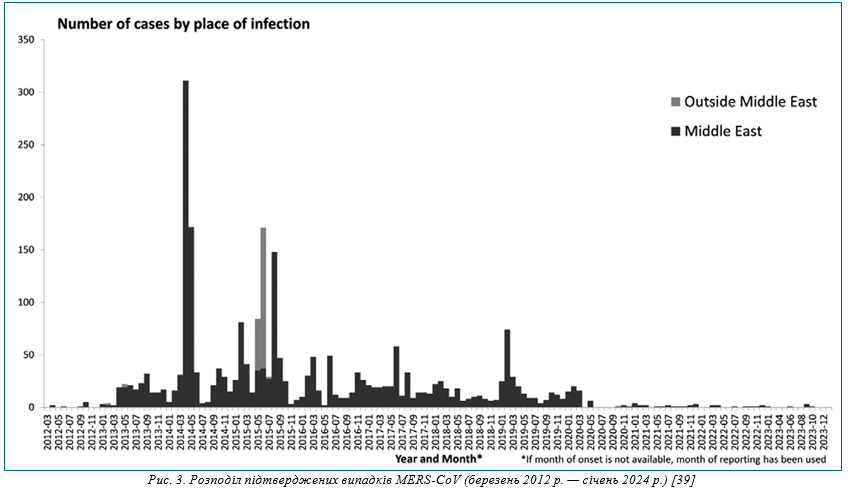
Близькосхідний респіраторний синдром. Із 2012 р. почав циркулювати новий для людини коронавірус MERS-CoV, який став етіологічним агентом емерджентної інфекції — близькосхідного респіраторного синдрому (MERS), летальність при якому сягала 36,2%. На теперішній час (на 12.02.2024 р.) захворіла 2 621 людина. Найбільша кількість захворювань зареєстрована в 2014–2015 роках. Рівні захворюваності, які спостерігалися протягом 2014–2015 рр., викликали занепокоєння щодо подальшого поширення цієї інфекції, тим паче, що у 2015 р. вона вийшла поза межі Близького Сходу [39] (рис. 3).
Як з’ясувалося, природним резервуаром збудника інфекції є верблюди. Натепер випадки зареєстровані в 27 країнах, найбільша кількість — у Саудівській Аравії, Республіці Корея, Об’єднаних Арабських Еміратах, Йорданії. Найбільший спалах за межами Близького Сходу стався в Республіці Корея в 2015 р. (186 випадків і 39 смертей). Групою ризику є люди, які знаходяться в тісному контакті з верблюдами (наприклад, фермери, працівники бійні, пастухи, власники верблюдів) та медичні працівники, що доглядають за пацієнтами з MERS. Передача вірусу MERS-CoV була задокументована протягом 2012–2016 рр. у кількох країнах, включаючи Саудівську Аравію, Йорданію, Об’єднані Арабські Емірати, Францію, Сполучене Королівство та Республіку Корея, з різними розмірами спалаху (2–180 випадків). Із 2 600 випадків MERS, про які було відомо в 2022 р., принаймні 17% (454/2 600) спостерігалися у медичних працівників. На теперішній час інтенсивність циркуляції вірусу знизилася [40], а загроза стійкої передачі вірусу від людини до людини оцінюється як низька.
Хвороба Ебола. Перший випадок хвороби Ебола (тоді називалася «гарячка Ебола») у людини було зареєстровано в 1976 році. Від того часу періодично в деяких країнах Африки (переважно Центральної Африки) спостерігалися епідемічні спалахи, які вдавалося локалізувати і припинити. Стійкої передачі збудника від людини до людини не спостерігалося. У 2014–2016 рр. у Західній Африці виникла широкомасштабна епідемія хвороби Ебола. Її збудник (Zaire ebolavirus) почав циркулювати в Гвінеї ще з кінця 2013 р., поширившись пізніше на Ліберію та Сьєрра-Леоне. Почалася передача вірусу від людини до людини. За понад 2 роки захворіло 28 625 осіб, зокрема 11 325 померли (39,6%). Було зареєстровано завезення випадків хвороби Ебола ще в 7 країн (Італію, Малі, Нігерію, Сенегал, Іспанію, Великобританію та США), в деяких із них спостерігалися вторинні випадки інфікування (в Італії, Малі, Нігерії та США). При цій епідемії вперше були застосовані вакцини за принципом «для емерджентного застосування». Натепер уже існує дві ліцензовані вакцини проти Zaire ebolavirus, які пройшли відповідну реєстрацію в 2019 та 2020 рр. [41–43].
Хвороба Зіка. Майже в той же період (2015–2016 рр.) відбулося ускладнення епідемічної ситуації з хвороби Зіка. Вірус Зіка вперше був виявлений в Уганді в 1947 р. у мавп, у 1948 р. — у комарів Aedes africanus, пізніше, у 1952 р. — у людей в Уганді та Танзанії. Перший великий спалах цієї інфекції було зареєстровано в 2007 р. на о. Яп (у Тихому океані). У 2013–2014 рр. вірус викликає спалахи на 4 інших групах тихоокеанських островів [44].
У березні 2015 р. Бразилія повідомила про великий спалах хвороби, що супроводжувалася гарячкою та висипкою, яку невдовзі ідентифікували як хворобу Зіка. Протягом лютого–квітня 2015 р. було зареєстровано понад 7 000 випадків. У липні 2015 р. було встановлено, що одним із клінічних проявів цієї хвороби є синдром Гієна-Барре. За теперішніми оцінками його поширеність становить 1,23%. У 2016 р. ВООЗ оголосила про зв’язок хвороби Зіка з випадками мікроцефалії та іншими неврологічними розладами. Це було визнано надзвичайною ситуацією в галузі охорони здоров’я, яка викликає міжнародне занепокоєння. На березень 2017 р. було повідомлено вже про понад 750 000 підозрілих або підтверджених випадків хвороби Зіка, які були зареєстровані на території Північної та Південної Америки. Натепер 86 країн повідомили про факти інфікування вірусом Зіка за участю комарів як векторів [45–47]. Головним вектором вірусу Зіка є комарі Aedes aegypti, для яких показана можливість трансваріальної передачі вірусу Зіка [48]. Також треба мати на увазі ризики розширення ареалу комарів різних видів у зв’язку зі зміною кліматичних умов, а з ними — і ризики поширення хвороби Зіка.
Вірус визначали в спермі у 61% чоловіків, обстежених протягом 30 днів після початку хвороби. У 1 чоловіка (1% від числа обстежених) РНК вірусу визначалася протягом 281 дня [16].
Після епідемії цієї інфекції кілька країн Латинської Америки рекомендували жінкам відкладати вагітність на період від 6 місяців до 2 років. Ці рекомендації поклали початок критичним дискусіям щодо проблем їх реалізації в суспільствах з обмеженим доступом до протизаплідних засобів, широко поширеними соціально-економічними нерівностями та високим рівнем незапланованої та підліткової вагітності. Водночас у деяких країнах, які постраждали від епідемії Зіка, через обмежувальну репродуктивну політику законне переривання вагітності більше не є можливим навіть на ранніх термінах, тоді, коли вади розвитку головного мозку, як частину вродженого синдрому Зіка, можна виявити за допомогою УЗД. Оскільки через зміни клімату прогнозується розширення географічної зони, де може відбуватися місцева передача вірусу Зіка, взаємозв’язок між вірусом, тератогенезом та репродуктивними правами є ще й біоетичною проблемою, яка буде актуальною на довгі роки вперед [49].
При цьому справжні географічні масштаби хвороби Зіка залишаються до кінця нез’ясованими через припущення про заниження даних. І це можна розглядати як ключовий компонент недостатньої готовності реагування на ситуацію [50]. Також треба додати, що наразі не існує вакцин для профілактики хвороби Зіка. Широко застосовуються неспецифічні засоби профілактики, спрямовані на боротьбу с комарами та захист від їхніх укусів.
COVID-19. Наступним важким випробуванням для людства стала пандемія COVID-19, викликана коронавірусом SARS-CoV-2. Вона розпочалася на початку 2020 р., швидко поширилася світом, несучи з собою безпрецедентне навантаження на системи охорони здоров’я країн та супроводжуючись високою летальністю, особливо серед людей старше 65 років та тих, хто мав супутню патологію. Це була емерджентна інфекція, до збудника якої на початку його циркуляції імунітет був взагалі відсутнім. Вірус характеризувався швидкою мінливістю, що призводило до формування значної кількості мутацій, в тому числі мутацій так званої «вакцинної втечі», а специфічний імунний захист — нетривалістю.
На початку пандемії спостерігався невисокий індекс контагіозності, який поступово збільшувався на тлі зниження патогенності SARS-CoV-2. Це відповідає класичним уявленням про формування нових паразитарних систем та їх функціонування. Патогенетичні особливості розвитку інфекційного процесу, особливо на початку пандемії, були не характерними для респіраторних інфекцій — відмічалася значна кількість коагулопатій та імунопатологічних реакцій. Але незалежно від походження збудника, при новій інфекційній хворобі еволюція епідемічного процесу розвивалась за класичним варіантом.
Натепер інтенсивність епідемічного процесу COVID-19 значно знизилася, наближаючись до характеристик сезонних респіраторних інфекцій, а його збудник циркулює паралельно з іншими респіраторними вірусами. Особливості епідемічного процесу COVID-19 в Україні нами були всебічно проаналізовані та описані [51]. Що стосується глобальної ситуації щодо цієї інфекції, то значне зниження захворюваності та кількості летальних випадків спостерігається, починаючи із середини 2023 р. (рис. 4) [52]. Це пов’язано зі зміною циркулюючих варіантів коронавірусу, набуттям переважною більшістю населення специфічного імунітету як внаслідок природного інфікування, так і вакцинації, та свідчить про формування нової стійкої паразитарної системи. Однак треба пам’ятати, що еволюція вірусу SARS-CoV-2 продовжується, не виключена можливість розширення паразитарної системи завдяки включенню до її структури нових видів ссавців як біологічних хазяїв, ураховуючи багаторазові факти виділення цього вірусу від тварин. Натепер відомо щонайменше про 18 видів тварин, які можуть бути інфіковані цим вірусом [53]. Крім того, описано навіть локальні спалахи COVID-19 серед норок [54]. Віруси, що циркулюють серед людей і тварин, потребують постійного молекулярно-генетичного моніторингу для прогнозування епідемічної ситуації та своєчасної протидії.
Мавпяча віспа (MPX). Вірус мавпячої віспи (monkeypox virus — MPXV) був відомий із 1958 р., а перший випадок захворювання людини зареєстрований у 1970 р. у Демократичній Республіці Конго. У травні 2022 р. на тлі пандемії COVID-19 з’явилися повідомлення про поширення цього давно відомого збудника за межі ендемічного для нього регіону, який обмежувався 7 країнами Західної та Центральної Африки. Також для цієї реемерджентної інфекції став характерним дещо інший клінічний перебіг у порівнянні з раніше відомою хворобою і новий шлях передачі збудника — статевий. Основною групою ризику для цього варіанту MPX виявилися чоловіки, які мають секс із чоловіками [55]. Багатьма дослідженнями було доведено факт наявності MPXV, здатного до реплікації, у зразках сперми пацієнтів у гострій стадії захворювання [56–58].
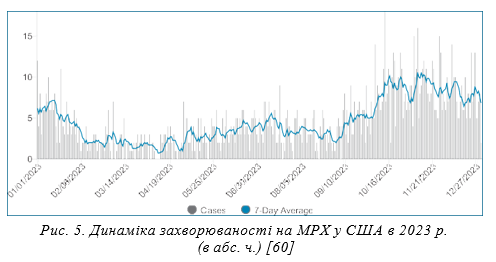
Менше ніж за 2 роки хвороба розповсюдилася на 111 країн, а кількість зареєстрованих випадків на 07.02.2024 р. досягла 9 373 (проти 2 124 — в 7 ендемічних країнах), серед них 156 закінчилися летально (0,17%). В ендемічних країнах спостерігався 21 летальний випадок, а смертнісь дорівнювала 1%, тобто була в 6 разів вищою, ніж при реемерджентній MPX. Найвищі показники захворюваності спостерігаються у США (31 894), Бразилії (10 967), Іспанії (7 752), Франції (4 171), Колумбії (4 090), Мексиці (4 079), Великій Британії (3 875), Перу (3 812), Німеччині (3 800), Китаї (1 611), Чилі (1 449), Канаді (1 419), Нідерландах (1 287), Португалії (1 162), Аргентині (1 136). Достатньо високою є захворюваність на MPX і в інших країнах Європи: Італія — 989 випадків, Бельгія — 800, Швейцарія — 563, Австрія — 338, Ірландія — 275, Швеція — 267, Польща — 217, Данія — 198, Греція — 89, Угорщина — 82, Чехія — 71, Люксембург — 60, Румунія — 47, Фінляндія — 43, Мальта — 35, Ісландія — 17, Словаччина — 14, Естонія — 11 [59]. Інтенсивність епідемічного процесу MPX у США показано на рисунку 5 для того, щоб підкреслити, з одного боку, той факт, що епідемічний процес цієї інфекції не припиняється, з іншого боку, що за умов функціонування в країні ефективної системи епідеміологічного нагляду, випадки МРХ виявляються регулярно [60].

В Україні за цей період виявлено лише 5 випадків MPX, що на тлі епідемічної ситуації в сусідніх країнах та високих показників постійних міграційних процесів свідчить про відсутність належного епідеміологічного нагляду за цією інфекцією.
Ураховуючи широке розповсюдження MPX у світі та укорінення нового варіанту MPXV у людській популяції, натепер широко піднімається питання щодо розробки нових лікарських засобів проти MPXV, зокрема таких, які б запобігали формуванню резистентності до цих вірусів [61], що б стало протидією подальшому поширенню MPXV.
Особливості сучасних епідемій і пандемій, потенційно пандемічні патогени, хвороба Х. Ми ще раз підкреслюємо той факт, що на теперішній час серед збудників, що ускладнювали епідемічну ситуацію у світі та які є потенційними етіологічними агентами майбутніх епідемій і пандемій, переважають віруси. Це пов’язано з багатьма чинниками, які можуть впливати окремо або комплексно: більш швидкою їх мінливістю, відсутністю в більшості випадків специфічного лікування, більш легкою можливістю реалізації механізму передачі збудника внаслідок тривалого його збереження в абіотичних об’єктах, меншою «інфікуючою» дозою, глобалізацією міграційних процесів, зростанням чисельності населення та щільності заселення територій, розширенням сільськогосподарських угідь, тваринництва, різноманітних контактів із дикими тваринами, що збільшує потенціал нових зоонозних інфекцій.
Як нами вже підкреслювалось, загалом близько 60% інфекційних хвороб людини мають зоонозне походження. На подальше формування емерджентних зоонозних збудників впливає також зміна кліматичних умов, що сприяє розширенню ареалу проживання птахів і ссавців, які є природним резервуаром чисельної кількості патогенів, а також різноманітних комах — векторів патогенів. Зокрема, антропофільні види комарів A. aegypti і A. albopictus, які натепер віддають перевагу розмноженню в міському середовищі, стали головними векторами вірусів-збудників жовтої гарячки, денге, чикунгуньї, хвороби Зіка. Слід зазначити, що ці віруси виникли багато століть тому як збудники інфекцій тварин у лісових осередках [62].
Аналізуючи епідемії і пандемії з великою швидкістю розповсюдження, не можна забувати й про ті інфекції, які наразі уже набули глобального або регіонального ендемічного характеру і які значно впливають на летальність від інфекційних хвороб та є важким економічним та соціальним тягарем (наприклад, ВІЛ-інфекція/СНІД, вірусні гепатити В і С, туберкульоз, малярія, інфекції, викликані резистентними бактеріями тощо). Виходячи із цього переліку, не можна також зменшувати роль бактеріальних інфекцій.
У роботі R. A. Weiss and N. Sankaran [62] наданий рисунок (рис. 6), який демонструє приблизні оцінки глобальної смертності внаслідок окремих інфекційних хвороб у 2020 р. Автори підкреслюють, що хоча COVID-19 став основним фактором смертності від інфекцій у 2020 р., але, як правило, не помічається, що подібна кількість смертей була спричинена грибко- вими інфекціями, які включають нещодавно виниклу епідемію, викликану Candida aureus. Показовим є приклад тягаря для суспільства такої розповсюдженої вірусної інфекції, як сказ. Вона вважається контрольованою завдяки вакцинації тварин і постраждалих від їхніх укусів людей. Водночас на тлі, здавалося б, поодиноких випадків сказу серед людей, за оцінками, щороку стається щонайменше 50 000 летальних випадків від нього, що призводить до економічних втрат у розмірі 8,6 млрд доларів США [63].
Вплив зміни клімату на виникнення «нових» збудників і поширення інфекційних хвороб натепер розглядається як надзвичайно актуальна проблема, яка потребує постійного вивчення і контролю.
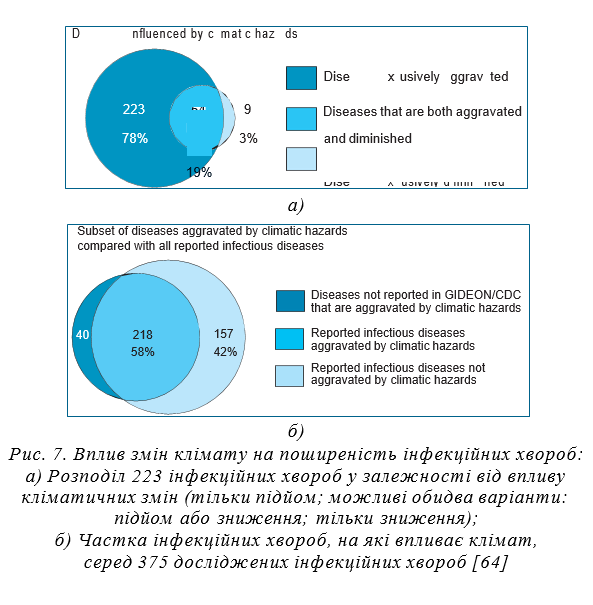
При визначенні впливу 10 кліматичних небезпек, пов’язаних із викидами парникових газів, на відомі інфекційні хвороби людини, показано, що поширення 58% інфекційних хвороб (218 із 375 досліджених) у даний момент збільшилося внаслідок кліматичного впливу (рис. 7). При детальному вивченні 223 хвороб, такий вплив визначено для 78% інфекцій. Зроблено висновок про те, що інфекційних хвороб людини та шляхів передачі їх збудників, ускладнених кліматичними небезпеками, надто багато для комплексної адаптації суспільства. Це підкреслює нагальну потребу працювати над джерелом проблеми — скороченням викидів парникових газів [64].

В останній час усе частіше піднімається питання про ризики наступної пандемії та потенційно вищу вірулентність її збудника в порівнянні з попередніми. Мова йде як про відомі натепер інфекції, так і про так звану «хворобу Х». Ще в травні 2015 р. ВООЗ скликала широку коаліцію експертів для проєктування плану досліджень та розроблень щодо запобігання епідеміям. Основна увага приділялася серйозним емерджентним хворобам, які можуть призвести до надзвичайної ситуації в галузі охорони здоров’я. Акценти були зроблені на наступні напрями: оцінка епідемічної загрози та визначення пріоритетних збудників; розроблення дорожніх карт для прискорення отримання й оцінки діагностичних, терапевтичних засобів та вакцин; визначення відповідних нормативних та етичних шляхів. Була надана методологія, спрямована на виявлення основних глобальних загроз інфекційних хвороб у межах постійного процесу переоцінки пріоритетів із урахуванням мінливості обставин. Передбачено, що щороку повинні визначатися 10 найбільш пріоритетних патогенів за такими критеріями: передача від людини до людини; медичні протидії; тяжкість клінічного перебігу або летальність; взаємодія в популяції людина/ тварина; інші фактори; стан громадської охорони здоров’я постраждалої території; потенційний вплив на суспільство; еволюційний потенціал [65].
Використовуючи такий інструмент ВООЗ, на даний момент пріоритетними інфекційними хворобами, які становлять найбільший ризик для громадського здоров’я через їх епідемічний потенціал та/або відсутність або недостатність контрзаходів, є:
- COVID-19;
- Крим-Конго геморагічна гарячка;
- хвороба Ебола та хвороба, викликана вірусом Марбург;
- гарячка Ласса;
- MERS і SARS;
- Ніпата геніпавірусні інфекції;
- гарячка долини Рифт;
- хвороба Зіка;
- хвороба X [66].
До цього переліку не входять інфекції, які хоча й становлять пандемічний ризик, але для яких існують міжнародні ініціативи моніторингу та протидії, наприклад, зоонозний грип.
Термін «хвороба Х» не є новим. Раніше при визначенні пріоритетних щодо пандемічного поширення інфекційних хвороб одну з них позначали, як «нова хвороба», пізніше стали використовувати термін «хвороба Х». Хвороба Х означає, що серйозну міжнародну епідемію може спричинити патоген, який на даний момент невідомий як збудник хвороби людини. План протидії повинен бути спрямований на ранню готовність до всебічних досліджень і розробок щодо невідомої хвороби X [66–68].
Натепер створено Міжурядовий орган переговорів для розробки та узгодження Конвенції ВООЗ, угоди чи іншого міжнародного документа щодо запобігання пандемії, готовності та відповіді, що працює над проєктом зазначеного документу. Його передбачається затвердити в 2024 р. Експерти з України також беруть участь у цій роботі. У документі велика увага приділяється науковим дослідженням як основі прийняття організаційних рішень та забезпечення системи охорони здоров’я діагностичними, лікувальними та профілактичними засобами. Прийняття цієї Конвенції та впровадження її положень на національному рівні дозволить підвищити ефективність систем біобезпеки та нарощування потенціалу протидії біологічним загрозам.
Що стосується готовності України до потенційних глобальних біологічних викликів, то, як зазначалося вище, у Глобальному індексі безпеки охорони здоров’я її рейтингове місце за показником «швидке реагування» серед 195 країн становило 100, а за загальною оцінкою готовності системи охорони здоров’я — 94 (рис. 8) [6]. Індекс швидкого реагування на виклики за 100-бальною оцінкою, розрахований для України, становив лише 34,8, у той час, як для Великої Британії та США він дорівнював відповідно 91,9 та 79,7 при середньому показнику для світу 38,4.
Хоча пандемія COVID-19 показала значення та необхідність відбудови чіткої системи швидкого реагування на біологічні небезпеки, з організації боротьби з нею винесено уроки, які продовжують аналізуватися і враховуються в більшості документів, що затверджуються на національних і міжнародних рівнях. Однак усім країнам, зокрема й Україні, необхідно докласти ще багато зусиль для досягнення дійсно належного рівня готовності попередження біологічних загроз та реагування на майбутні виклики.

Висновки.
- Епідемії та пандемії минулого були потужною руйнівною силою, забираючи мільйони життів і навіть змінюючи хід цивілізацій. Тоді ж, спочатку на емпіричній основі, а потім на підставі доказових наукових досліджень були закладені основи протиепідемічних і профілактичних заходів, починаючи від карантинних і закінчуючи вакцинопрофілактикою.
- Натепер зоонозні інфекційні агенти превалюють серед патогенів людини, зокрема й серед емерджентних. Серед патогенів з епідемічним і пандемічним потенціалом переважають віруси. Це пов’язано з багатьма чинниками, що впливають окремо або комплексно (швидка мінливість вірусів, відсутність специфічного лікування, легша реалізація механізму передачі внаслідок тривалого збереження в абіотичних об’єктах, менша «інфікуюча» доза, глобалізація міграційних процесів, зростання чисельності населення та щільності заселення територій). Потенціал нових зоонозних інфекцій збільшується завдяки розширенню сільськогосподарських угідь, тваринництва, різноманітних контактів із дикими тваринами тощо.
- На тлі формування нової стійкої паразитарної системи інтенсивність епідемічного процесу COVID-19 значно знизилася, наближаючись до характеристик сезонних респіраторних інфекцій, а його збудник циркулює паралельно з іншими респіраторними вірусами. Однак ризики включення до її функціонування деяких видів тварин, як біологічних хазяїв, потребують постійного моніторингу.
- ВООЗ, відповідно до розроблених критеріїв, проводить постійний моніторинг потенційно пандемічних агентів, визначаючи 10 пріоритетних хвороб, включаючи хворобу Х. До переліку не включені хвороби з пандемічним потенціалом, для яких існують стійкі міжнародні ініціативи моніторингу і протидії (наприклад, зоонозний грип).
- Прийняття Конвенції ВООЗ, угоди чи іншого міжнародного документа щодо запобігання пандемії, готовності та відповіді, проєкт якої натепер проходить етап узгодження, та впровадження її положень на міжнародному та національних рівнях будуть сприяти підвищенню ефективності систем біобезпеки та потенціалу протидії біологічним загрозам.
- Національна система біобезпеки України потребує суттєвого вдосконалення в напряму посилення епідеміологічного нагляду за інфекційними хворобами.
Література
- Задорожна В. І., Фролов А. Ф., Зубкова Н. Л. та ін. Поліомієліт: імунопрофілактика та її вплив на еволюцію епідемічного процесу. [Poliomijelit: imunoprofilaktyka ta i’i’ vplyv na evoljuciju epidemichnogo procesu]. Київ: DІА; 272 p. (in Ukrainian).
- Risse G. B. Revolt against quarantine: community responses to the 1916 polio epidemic, Oyster Bay, New Trans Stud Coll Physicians Phila. 1992;14(1):23–50. PMID: 1604465.
- Sudhan S. S., Sharma P. Human Viruses: Emergence and Evolution. Emerging and Reemerging Viral Pathogens. 2020:53–68. Available from: https://doi.org/10.1016%2FB978-0-12-819400-3.00004-1
- Sabin S., Calliope A. S., Simpson S. V. et al. Implications of human activities for (re)emerging infectious diseases, including COVID-19. J Physiol Anthropol. 39, 29(2020). Available from: https://doi.org/10.1186/ s40101-020-00239-5
- Institute of Medicine (US) Forum on Microbial Microbial Evolution and Co-Adaptation: A Tribute to the Life and Scientific Legacies of Joshua Lederberg: Workshop Summary. Washington (DC): National Academies Press (US); 2009. 5, Infectious Disease Emergence: Past, Present, and Future. Available from: https://www.ncbi.nlm.nih.gov/ books/NBK45714/
- Cameron E., Nuzzo J. B., Bell J. A. et al. Global Heath Security Index (GHSI) 2019. Available from: https://ghsindex.org/wp-content/ uploads/2019/10/2019-Global-Health-Security-Index.pdf.
- Jarus О. The worst epidemics and pandemics in Live Science. last updated January 31, 2023. Available from: http://swww.livescience.com/ worst-epidemics-and-pandemics-in-history.html
- Sabbatani , Fiorino S. La peste antonina e il declino dell’Impero Romano. Ruolo della guerra partica e della guerra marcomannica tra il 164 e il 182 d.c. nella diffusione del contagio [The Antonine Plague and the decline of the Roman Empire]. Infez Med. 2009;17(4):261–75. Italian. PMID: 20046111
- Sarris Peter, Viewpoint New Approaches to the “Plague of Justinian”, Past & Present. 2022; 254(10): 315–46, Available from: https://doi.org/10.1093/ pastj/gtab024
- Jilani N., Jamil R. T., Siddiqui A. H. H1N1 Influenza. [Updated 2022 Oct 25]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2024 Jan. Available from: httpshttp://www.ncbi.nlm.nih.gov/books/NBK513241/gov/books/NBK513241/
- Натуральна віспа. Енциклопедія сучасної України. https://esu.com. ua/article-70582
- Фролов А. Ф., Задорожная В. И. Молекулярная эпидемиология вирусных и прионных инфекций [Molekuljarnaja эpydemyologyja vyrusnыh y pryonnыh ynfekcyj] Київ: DІА; 280 p. (in Russian).
- Hasan , Khan M. O., Ali M. Swine Flu: Knowledge, Attitude, and Practices Survey of Medical and Dental Students of Karachi. Cureus. Cureus. 2018; 10(1): e2048 Available from: https://doi.org/10.7759%2Fcureus.2048
- Cartwright Black Death. World History Encyclopedia. 2023. Available from: https://www.worldhistory.org/Black_Death/
- Delaney , Mai C., Smoots A. et al. Population-Based Surveillance of Birth Defects Potentially Related to Zika Virus Infection — 15 States and U.S. Territories, 2016. MMWR Wkly Rep 2018;67:91–6. Available from: http:// dx.doi.org/10.15585/mmwr.mm6703a2
- Mead S., Duggal N. K., Hook S. A., Delorey M., Fischer M. et al. Zika Virus Shedding in Semen of Symptomatic Infected Men. N Engl J Med. 2018;378(15):1377–85. DOI: 10.1056/NEJMoa1711038
- Mpox Outbreak Global Map. 022-2023 Mpox Outbreak Global Map. — https://www.cdc.gov/poxvirus/Mpox/response/2022/world-map.html
- Задорожна В. І., Сергеєва Т. А., Шагінян В. Р. Мавпяча віспа: реемерджентна інфекція та подальші епідеміологічні ризики. Журнал Національної академії медичних наук України. 2022;28(2): 399–421. DOI: 37621/JNAMSU-2022-2-3.
- HISTORY. 2024. Available from: https://www.history.com/ topics/inventions/history-of-cholera.
- WHO (13 December 2022). Disease Outbreak News; Cholera — Haiti. Available from: https://www.who.int/emergencies/disease-outbreak-news/item/2022-DON427)
- Hong Kong From Wikipedia, the free encyclopedia. Available from: https://en.wikipedia.org/wiki/Hong_Kong_flu
- European Centre for Disease Prevention and Communicable Disease Threats Report. Week 7, 11–17 February 2024. Available from: https://www.ecdc.europa.eu/sites/default/files/documents/ communicable-disease-threats-report-week-7-2024.pdf
- WHO: Multi-country outbreak of External Situation Report n. 11, published 12 February 2024. Available from: https://reliefweb.int/ attachments/13745ff2-c3af-433a-b181-30d26efbc608/20240212_multi-country_outbreak-of-cholera_sitrep_11.pdf
- HIV. https://www.who.int/data/gho/data/themes/hiv-aids
- Geeraedts , Goutagny N., Hornung V., Severa M., de Haan A., Pool J., Wilschut J., Fitzgerald K. A., Huckriede A. Superior Immunogenicity of Inactivated Whole Virus H5N1 Influenza Vaccine is Primarily Controlled by Toll-like Receptor Signalling. PLoS Pathogens, August 2008. Available from: https://doi.org/10.1371/journal.ppat.1000138
- Wallace R. G. Breeding Influenza: The Political Virology of Offshore Antipode. 2009;41(5):916-51. Available from: https://doi. org/10.1111/j.1467-8330.2009.00702.x
- Balish L., Davis C. T., Saad M. D., El-Sayed N., Esmat H., Tjaden et al. (). Antigenic and Genetic Diversity of Highly Pathogenic Avian Influenza A (H5N1) Viruses Isolated in Egypt. Avian Diseases, 2010;54(1): 329–334. http://www.jstor.org/stable/40601080
- CDC: Technical Report: Highly Pathogenic Avian Influenza A(H5N1) Updated. December 29, 2023. Available from: https://www.cdc.gov/flu/ avianflu/spotlights/2022-2023/h5n1-technical-report_december.htm
- Shrestha S., Swerdlow D. L., Borse R. H., Prabhu V. S., Finelli L., Atkins C.et al. Estimating the burden of 2009 pandemic influenza A (H1N1) in the United States (April 2009-April 2010). Clin Infect Dis. 2011;52(1):S75–82. DOI: https://doi.org/10.1093/cid/ciq012
- Dawood S., Iuliano A. D., Reed C., Meltzer M. I., Shay D. K., Cheng P.et al. Estimated global mortality associated with the first 12 months of 2009 pandemic influenza A H1N1 virus circulation: a modelling study. Lancet Infect Dis. 2012;12(9):687–95. DOI: https://doi.org/10.1016/s1473-3099(12)70121-4
- WHO (31 December 2022) Pandemic Influenza Preparedness Framework: annual progress report. Geneva. Available from: https://iris.who.int/ bitstream/handle/10665/372197/9789240076907-eng.pdf?sequence=1
- WHO (13 February 2024). Disease Outbreak News; Avian Influenza A(H10N5) and Influenza A(H3N2) coinfection — Available from: https://www. who.int/emergencies/disease-outbreak-news/item/2023-DON504
- WHO: Surveillance -Avian Avian Influenza Weekly Update 2018 -2024. Available from: https://www.who.int/westernpacific/ emergencies/surveillance/avian-influenza
- Reports of Avian Influenza (AI) “Bird Flu” Outbreaks Increased Globally from 2013–2022. September 7, 2023. Available from: https:// www.cdc.gov/flu/avianflu/spotlights/2022-2023/avian-influenza-outbreaks-increased-globally.htm
- WHO (7 February 2024). Disease Outbreak News; Influenza A(H1N1) variant virus — Brazil. Available from: https://www.int/emergencies/disease-outbreak-news/item/2024-DON502
- WHO (9 February 2024). Disease Outbreak News; Influenza A(H1N1) variant virus — Spain. Available from: http://www.who.int/emergencies/ disease-outbreak-news-/item/2024-DON503
- WHO (15 March 2022). Celebrating 70 years of the Global Influenza Surveillance and Response System. Available from: https://www.who. int/news-room/featurestories/detail/celebrating-70-years-of-the-global-influenza-surveillance-and-response-system
- WHO (19 April 2023). Pandemic influenza preparedness framework: partnership contribution high-level implementation plan III 2024–2030. Available from: https://www.who.int/publications/i/item/9789240070141
- European Centre for Disease Prevention and Communicable Disease Threats Report. Week 7, 11–17 February 2024. Available from: https://www.ecdc.europa.eu/sites/default/files/documents/ communicable-disease-threats-report-week-7-2024.pdf
- WHO (November 2022). Middle East respiratory syndrome: global summary and assessment of risk.16 Available from: https://iris.who. int/bitstream/handle/10665/364525/WHO-MERS-RA-2022.1-eng. pdf?sequence=1
- Kaner , Schaack S. Understanding Ebola: the 2014 epidemic. Global Health. 2016;12(1):53. DOI: https://doi.org/10.1186/s12992-016-0194-4
- Ebola. West Africa, March 2014–2016. Available from:https://www. who.int/emergencies/situations/ebola-outbreak-2014-2016-West-Africa
- WHO (11 January 2020). Ebola virus disease: Vaccines. Available from:https://www.int/news-room/questions-and-answers/item/ ebola-vaccines
- WHO (7 February ) The history of zika virus. Available from:https:// www.who.int/news-room/feature-stories/detail/the-history-of-zika-virus
- Zika virus disease. Outbreak 2015–2016. Available from:https:// www.who.int/emergencies/situations/zika-virus-outbreak
- Barbi L., Coelho A.V.C., Alencar L.C.A., Crovella S. Prevalence of Guillain-Barré syndrome among Zika virus infected cases: a systematic review and meta-analysis. Braz J Infect Dis. 2018;22(2):137-41. DOI: https://doi. org/10.1016/j.bjid.2018.02.005
- Hills L., Fischer M., Petersen L. R. Epidemiology of Zika Virus Infection. J Infect Dis. 2017;216(10):S868-74. DOI: https://doi.org/10.1093/infdis/ jix434
- Li X., Guo X. X., Deng Y. Q., Xing D., Sun A. J., Liu Q. M. et al. Vector competence and transovarial transmission of two Aedes aegypti strains to Zika virus. Emerg Microbes Infect. 2017;6(4):e23. Available from: https:// doi.org/10.1038%2Femi.2017.8
- Stein R. A., Grayon A., Katz A., Chervenak F. A. The Zika virus: an opportunity to revisit reproductive health needs and Germs. 2022;12(4):519–37. DOI: https://doi.org/10.18683%2Fgerms.2022.1357
- Sun H., Dickens B. L., Jit M., Cook AR., Carrasco LR. Mapping the cryptic spread of the 2015–2016 global Zika virus BMC Med. 2020;18(1):399. DOI: https://doi.org/10.1186/s12916-020-01845-x
- Задорожна В. І., Сергеєва Т. А., Шагінян В. Р., Люльчук М. Г. Епідемія COVID-19 в Україні та проблеми біобезпеки. Журнал НАМН України. 2023; 3–4 (29):246–66. DOI: 10/37621/JNAM
- COVID-19 coronavirus pandemic. Last updated: February 18, 2024. Available from: https://www.worldometinfo/coronavirus/
- Cui , Liu Y., Zhao J., Peng X., Lu G., Shi W., Pan Y., Zhang D., Yang P., Wang An Updated Review on SARS-CoV-2 Infection in Animals. Viruses. 2022;14(7):1527. DOI: https://doi.org/10.3390/v14071527
- Michelitsch A., Wernike K., Ulrich L., Mettenleiter T. C., Beer M. SARS-CoV-2 in animals: From potential hosts to animal Adv Virus Res. 2021;110:59-102. DOI: https://doi.org/10.1016/bs.aivir.2021.03.004
- Huang , Mu L. & Wang W. Monkeypox: epidemiology, pathogenesis, treatment and prevention. Sig Transduct Target Ther 2022;7:373. Available from: https://doi.org/10.1038/s41392-022-01215-4
- Lapa , Carletti F., Mazzotta V., Matusali G., Pinnetti C., Meschi S. et al. Monkeypox virus isolation from a semen sample collected in the early phase of infection in a patient with prolonged seminal viral shedding. The Lancet Infectious Diseases, 2022;22(9):1267-9. DOI: https://doi. org/10.1016/s1473-3099(22)00513-8
- Peiró-Mestres , Fuertes I., Camprubí-Ferrer D., Marcos MÁ, Vilella A., Navarro M., et al. Hospital Clinic de Barcelona Monkeypox Study Group. Frequent detection of monkeypox virus DNA in saliva, semen, and other clinical samples from 12 patients, Barcelona, Spain, May to June 2022. Euro Surveill. 2022;27(28):2200503. Available from: https://doi. org/10.2807%2F1560-7917.ES.2022.27.28.2200503
- Reda , Abdelaal A., Brakat A. M., Lashin B. I., Abouelkheir M., Abdelazeem B., Rodriguez-Morales A. J., Sah R. Monkeypox viral detection in semen specimens of confirmed cases: A systematic review and meta-analysis. J Med Virol. 2023;95(1):e28250. Available from: https://doi.org/10.1002/jmv.28250
- 2022–2023 Mpox Outbreak Global Map. Data as of 07 Feb 2024. Available from: https://www.cdc.gov/poxvirus/mpox/response/2022/world-map.html
- U.S. Mpox Case Trends Reported to CDC. Data as Reported to CDC as of 11 Jan 2024. Available from: https://www.cdc.gov/poxvirus/ mpox/response/2022/mpx-trends.html
- Lu , Xing H., Wang C. et al. Mpox (formerly monkeypox): pathogenesis, prevention, and treatment. Sig Transduct Target Ther 2023; 8: 458 Available from: https://doi.org/10.1038/s41392-023-01675-2
- Weiss R. A., Sankaran N. Emergence of epidemic diseases: zoonoses and other origins. Fac Rev. 2022;11:2. Available from: https://doi. org/10.12703%2Fr%2F11-2
- Hampson , Coudeville L., Lembo T., Sambo M., Kieffer A., Attlan M. et al. Global Alliance for Rabies Control Partners for Rabies Prevention. Estimating the global burden of endemic canine rabies. PLoS Negl Trop Dis. 2015;9(4):e0003709. Available from: https://doi.org/10.1371/journal.pntd.0003786
- Mora , McKenzie T., Gaw I. M. et al. Over half of known human pathogenic diseases can be aggravated by climate change. Nat. Clim. Chang. 2022; 12: 869–75. Available from: https://doi.org/10.1038/s41558-022-01426-1
- Methodology for Prioritizing Severe Emerging Diseases for Research and Developmen. Available from: https://cdn.who.int/media/ docs/default-source/blue-print/prioritizing-methodology.pdf
- Prioritizing diseases for research and development in emergency contexts. Available from: https://www.who.int/activities/prioritizing-diseases-for-research-and-development-in-emergency-contexts/prioritizing-diseases-for-research-and-development-in-emergency-contexts
- WORKSHOP ON PRIORITIZATION OF 8-9 December 2015. Blueprint for R&D preparedness and response to public health emergencies due to highly infectious pathogens. Available from: https:// cdn.who.int/media/docs/default-source/blue-print/blueprint-for-r-d-preparedness-and-response-meeting-report.pdf?sfvrsn=156d23be_2
- Jonkmans N., D’Acremont , Flahault A. Scoping future outbreaks: a scoping review on the outbreak prediction of the WHO Blueprint list of priority diseases. BMJ Glob Health. 2021;6(9):e006623. Available from: https://doi.org/10.1136/bmjgh-2021-006623
Відомості про авторів:
Задорожна В. І. — д. м. н., проф., чл.-кор. НАМН України, директор ДУ «Інститут епідеміології та інфекційних хвороб ім. Л. В. Громашевського НАМН України». Е-mail: viz2010@ukr.net
ORCID: 0000-0002-0917-2007
Шагінян В. Р. — д. м. н., старший науковий співробітник, завідувач відділу діагностики інфекційних та паразитарних хвороб ДУ «Інститут епідеміології та інфекційних хвороб ім. Л. В. Громашевського НАМН України».
ORCID: 0000-0002-2746-3414
Винник Н. П. — к. м. н., старша наукова співробітниця відділу епідеміологічного аналізу та імунопрофілактики ДУ «Інститут епідеміології та інфекційних хвороб ім. Л. В. Громашевського НАМН України».
Е-mail: vnp2006@ukr.net ORCID: 0000-0002-5608-005X
Information about the authors:
Zadorozhna V. I. — DSc (Medicine), Professor, Corresponding Member of the NAMS of Ukraine, Director of the State Institution «L. V. Hromashevskyi Epidemiology and Infectious Diseases Institute of National Academy of Medical Sciences of Ukraine».
Е-mail: viz2010@ukr.net
ORCID: 0000-0002-0917-2007
Shahinian V. R. — DSc (Medicine), Head of the Department of Diagnostics of Infectious and Parasitic Diseases of the State Institution
«L. V. Hromashevskyi Epidemiology and Infectious Diseases Institute of National Academy of Medical Sciences of Ukraine».
ORCID: 0000-0002-2746-3414
Vynnyk N. P. — PhD (Medicine), Senior Researcher of the Department of Epidemiological Analysis and Immunoprophylaxis of the State Institution «L. V. Hromashevskyi Epidemiology and Infectious Diseases Institute of National Academy of Medical Sciences of Ukraine».
Е-mail: vnp2006@ukr.net ORCID: 0000-0002-5608-005X
