Перший досвід застосування в антенатальних клініках Києва швидких тестів для одночасного виявлення серологічних маркерів ВІЛ-інфекції та сифілісу
УДК: 616.98:578.828-07+616.972-071.3:618-07(477-25) DOI:https://doi.org/10/61948/prevmed-2025-3-13
В. А. Марциновська1, 2, О. О. Недужко3, І. В. Андріанова1, О. Є. Нестерова1, О. О. Зезюлін4, О. М. Кислих2, О. В. Максименок2
1 ДУ «Центр громадського здоров’я МОЗ України»
2 ДУ «Інститут епідеміології та інфекційних хвороб ім. Л. В. Громашевського НАМН України», Київ, Україна
3 ТОВ «Європейський інститут політики громадського здоров’я»
4 БО «Український інститут політики громадського здоров’я»
ВІЛ-інфекція та сифіліс залишаються одними з найбільш значущих інфекцій, що передаються статевим шляхом (ІПСШ), які становлять серйозні ризики для здоров’я матері та дитини. Передача від матері до дитини (ПМД) може відбуватися під час вагітності, пологів або грудного вигодовування. Раннє виявлення дозволяє своєчасно розпочати лікування та запобігти ускладненням, зокрема перинатальній передачі.
Всесвітня організація охорони здоров’я (ВООЗ) рекомендує проводити планове скринінгування всіх вагітних жінок на ВІЛ-інфекцію та сифіліс під час першого візиту до жіночої консультації. Хоча охоплення тестуванням на ВІЛ-інфекцію загалом є достатнім, сифіліс під час вагітності часто залишається недіагностованим та нелікованим. Щоб усунути розрив між охопленням скринінгом на ВІЛ-інфекцію та сифіліс та запобігти несприятливим наслідкам, у 2019 році ВООЗ рекомендувала запровадити подвійні швидкі діагностичні тести (ПДШТ) для одночасного скринінгу на маркери цих інфекцій під час першого візиту до жіночої консультації (ЖК). Докази свідчать про те, що ПДШТ знижують витрати, мінімізують пропущені діагнози та дозволяють негайно розпочати лікування. Мета. Оцінити доцільність та доцільність впровадження ПДШТ для скринінгу на ВІЛ-інфекцію та сифіліс у жіночих консультаціях у Києві.
Матеріали та методи. Це дослідження з використанням змішаних методів поєднало перехресний аналіз результатів скринінгу на ВІЛ та сифіліс за допомогою ДРДТ та рутинних інструментальних методів (ІМ) серед 1 496 вагітних жінок (≥18 років) з невідомим ВІЛ/сифілісним статусом або негативним результатом при першому обстеженні, з трьома фокус-групами за участю 15 акушерів-гінекологів. Пілотний проєкт проводився у семи закладах дошкільної допомоги у Києві з використанням тесту First Response® HIV1+2/Syphilis Combo Card Test за підтримки Глобального фонду для боротьби зі СНІДом, туберкульозом та малярією.
Результати та обговорення. Середній вік учасниць становив 30,2 року; 71,5% мали вищу освіту, 74,8% були одружені, а 69,0% були працевлаштовані. Для 42,4% жінок це була перша вагітність; три мали ознаки наркотичної залежності. Результати скринінгу на ВІЛ за допомогою ДРДТ та ІМ повністю узгоджувалися, виявлено три позитивні випадки (0,2%; 95% ДІ: 0,04–0,58). На сифіліс у трьох жінок тест на ДРДТ виявився позитивним (0,2%; 95% ДІ: 0,04–0,59), з яких дві були підтверджені за допомогою ІМ. Випадків подвійної інфекції ВІЛ та сифілісу не виявлено. Усі позитивні випадки були направлені на лікування. Цільовий розмір вибірки (1 496 з 1 500 запланованих) був досягнутий у встановлені терміни. Вагітні жінки позитивно ставилися до використання ДРДТ. Показники ефективності скринінгу на ВІЛ за допомогою ДРДТ: чутливість — 100%, специфічність — 100%, ППВ — 100%, НПВ — 100%. Для сифілісу: чутливість — 66,7%, специфічність — 99,9%, ППВ — 66,7%, НПВ — 99,9%. Показники поширеності ВІЛ та сифілісу (по 0,2%) відповідали національній статистиці. Медичні працівники наголосили на доцільності, простоті та зручності ДРДТ, зазначивши, що впровадження суттєво не збільшило робоче навантаження, навіть в умовах воєнного часу. Відсутність регуляторної бази для використання ДРДТ залишається основною перешкодою. Чинний національний алгоритм тестування на ВІЛ (Наказ № 794, Міністерство охорони здоров’я України, 05.04.2019) не включає ДРДТ. Так само тестування на сифіліс на рівні первинної медичної допомоги не регулюється Наказом № 504 від 19.03.2018. Висновки. Інтеграція ДРДТ у рутинну допологову допомогу в Україні є як можливою, так і ефективною. Такий підхід пришвидшує діагностику, покращує доступ до медичних послуг та сприяє ранньому початку лікування ВІЛ та сифілісу. Рекомендується розширити використання ДРДТ у різних медичних закладах (жіночі консультації, пологові будинки, перинатальні центри), особливо у віддалених районах, а також поширити тестування на сексуальних партнерів вагітних жінок та представників ключових та вразливих груп населення з ризиком зараження ВІЛ. Ключові слова: вагітні жінки, ВІЛ-інфекція, сифіліс, подвійні швидкі діагностичні тести, допологовий догляд.
A. Martsynovska1,2, O. O. Neduzhko3, V. Andrianova1, O. Ye. Nesterova1, O. O. Zeziulin4, O. M. Kyslykh2, O. V. Maksymenok2
INITIAL IMPLEMENTATION EXPERIENCE IN ANTENATAL CLINICS OF KYIV
DUAL RAPID TESTS FOR SIMULTANEOUS DETECTION OF SEROLOGICAL MARKERS OF HIV INFECTION AND SYPHILIS
1 SI “Public Health Center of the Ministry of Health of Ukraine”
2 SI “The L. V. Hromashevsky Institute of Epidemiology and Infection Diseases of NAMS of Ukraine”, Kyiv, Ukraine
3 European Institute of Public Health Policy
4 Ukrainian Institute on Public Health Policy
HIV infection and syphilis remain among the most significant sexually transmitted infections (STIs), posing serious risks to maternal and child health. Mother-to-child transmission (MTCT) can occur during pregnancy, childbirth, or breastfeeding. Early detection enables timely treatment and the prevention of complications, particularly perinatal transmission. The World Health Organization (WHO) recommends routine screening of all pregnant women for HIV and syphilis during the first antenatal visit. While HIV testing coverage is generally adequate, syphilis in pregnancy often remains undiagnosed and untreated. To address the gap between HIV and syphilis screening coverage and prevent adverse outcomes, in 2019 WHO advised the introduction of dual rapid diagnostic tests (DRDTs) for simultaneous HIV and syphilis screening at the first antenatal clinic (ANC) visit. Evidence suggests that DRDTs reduce costs, minimize missed diagnoses, and allow for immediate treatment initiation.
Objective. To assess the feasibility and appropriateness of introducing DRDT for HIV and syphilis screening in antenatal clinics in Kyiv.
Materials and Methods. This mixed-methods study combined a cross-sectional analysis of HIV and syphilis screening results using DRDT and routine instrumental methods (IM) among 1,496 pregnant women (≥18 years) with unknown HIV/syphilis status or a negative result at their first examination, with three focus groups involving 15 obstetrician- gynecologists. The pilot project was conducted in seven ANC facilities in Kyiv, employing the First Response® HIV1+2/ Syphilis Combo Card Test, supported by the Global Fund to Fight AIDS, Tuberculosis and Malaria.
Results and Discussion. The mean age of participants was 30.2 years; 71.5% had higher education, 74.8% were married, and 69.0% were employed. For 42.4% of women, this was their first pregnancy; three showed signs of drug dependence. HIV screening results from DRDT and IM were fully concordant, with three positive cases detected (0.2%; 95% CI: 0.04–0.58). For syphilis, three women tested positive using DRDT (0.2%; 95% CI: 0.04–0.59), of which two were confirmed by IM. No cases of dual HIV and syphilis infection were identified. All positive cases were referred for treatment. The target sample size (1,496 of 1,500 planned) was reached within the set timeframe. Pregnant women expressed positive attitudes toward DRDT use. Performance indicators for HIV screening via DRDT were: sensitivity — 100%, specificity — 100%, PPV — 100%, NPV — 100%. For syphilis: sensitivity — 66.7%, specificity — 99.9%, PPV — 66.7%, NPV — 99.9%. HIV and syphilis prevalence rates (0.2% each) aligned with national statistics. Healthcare providers emphasized the feasibility, simplicity, and convenience of DRDTs, noting that implementation did not significantly increase workload, even under wartime conditions. The absence of regulatory frameworks for DRDT use remains a major barrier. The current national HIV testing algorithm (Order No. 794, Ministry of Health of Ukraine, 05.04.2019) does not incorporate DRDT. Likewise, syphilis testing at the primary healthcare level is not regulated under Order No. 504, 19.03.2018.
Conclusions. Integrating DRDTs into routine antenatal care in Ukraine is both feasible and effective. This approach accelerates diagnosis, improves access to healthcare services, and facilitates early initiation of treatment for HIV and syphilis. It is recommended to expand DRDT use across various healthcare settings (antenatal clinics, maternity hospitals, perinatal centers), particularly in remote areas, and to extend testing to sexual partners of pregnant women and members of key and vulnerable populations at risk for HIV.
Keywords: pregnant women, HIV infection, syphilis, dual rapid diagnostic tests, antenatal care.
ВІЛ-інфекція та сифіліс залишаються двома найбільш значущими інфекційними захворюваннями, що передаються статевим шляхом, які становлять серйозну загрозу для здоров’я матері та дитини. Передача від матері до дитини може відбутися під час вагітності, пологів або грудного вигодовування. Своєчасне виявлення інфекцій дозволяє вчасно розпочати лікування та запобігти розвитку ускладнень, зокрема їхньої перинатальної передачі [1]. Усі вагітні повинні проходити тестування на ВІЛ на початку вагітності, а у групах підвищеного ризику — повторно у третьому триместрі. За відсутності лікування ймовірність вертикальної передачі ВІЛ сягає 30%, тоді як при належній антиретровірусній терапії цей ризик знижується до менш ніж 1% [2]. Сифіліс, залишений без лікування під час вагітності, може призвести до мертвонародження, передчасних пологів, вроджених дефектів та інших тяжких наслідків. У 2022 р. в США було зареєстровано понад 3 700 випадків вродженого сифілісу, і близько 90% з них можна було попередити своєчасним скринінгом та лікуванням [3]. ACOG (American College of Obstetricians and Gynecologists) рекомендує тестування на серологичні маркери сифілісу тричі: на початку вагітності, у третьому триместрі та при пологах у групах ризику [4].
Рекомендований ВООЗ рутинний скринінг усіх вагітних жінок на ВІЛ та сифіліс при першому допологовому візиті проводиться у багатьох країнах світу. Якщо тестування вагітних жінок на ВІЛ забезпечується відносно на належному рівні, то сифіліс у вагітних жінок часто не діагностують і не лікують. З метою усунення розриву між охопленням тестуванням на ВІЛ та сифіліс серед вагітних та запобігання несприятливих наслідків, ВООЗ ще у 2019 р. рекомендувала країнам впроваджувати модель надання послуг з тестування із використанням подвійних швидких тестів для одночасного проведення діагностики ВІЛ-інфекції та сифілісу (далі — ШТВС) під час першого візиту вагітних до антенатальних клінік (жіночих консультацій) (далі — АНК) [5]. На думку експертів, це дає змогу зменшити витрати, уникнути пропуску діагнозу та негайно розпочати лікування. Дослідження показують, що застосування комбінованих швидких тестів у клініках значно підвищує кількість виявлених випадків та скорочує час між діагностикою та початком лікування [6].
За ініціативою ВООЗ, світова спільнота взяла зобов’язання ліквідувати вертикальну передачу ВІЛ- інфекції, сифілісу та вірусного гепатиту В до 2030 р. [7]. «Потрійна» елімінація підвищує доцільність та користь такого інтегрованого підходу у програмах охорони здоров’я матері та дитини та вимагає здійснення принаймні один раз протягом вагітності і якомога раніше скринінгу на відповідні інфекції. Рівень охоплення тестуванням на ВІЛ та сифіліс вагітних ≥95% є цільовим індикатором валідації (підтвердження) елімінації вертикальної передачі ВІЛ-інфекції та сифілісу (далі — ЕПМД) [8].
Численні дослідження доводять ефективність ШТВС у діагностиці як ВІЛ-інфекції, так і наявного або перенесеного у минулому сифілісу. Більшість тестів, що доступні для застосування, зокрема в Україні, мають чутливість при тестуванні на ВІЛ більше 99% та специфічність більше 98%, при тестуванні на сифіліс чутливість становить більше 90%, а специфічність не менше 96%, що підтверджується багатьма дослідженнями [9, 10, 11]. Проте, слід зазначити, що реактивний результат тестування з використанням подвійних ШТВС для будь- якої з даних інфекцій не є остаточним та потребує додаткових лабораторних досліджень, відповідно до національної стратегії тестування.
У країнах як з високим, так і з низьким рівнем тягаря епідемії ВІЛ-інфекції встановлено, що тестування подвійними ШТВС не має негативного впливу на охоплення тестуванням на ВІЛ і дозволяє заощадити витрати на профілактику вродженого сифілісу. Очікувана користь та переваги використання ШТВС — це впорядковані закупівлі, мінімізація складських площ, спрощена підготовка медичного персоналу, лише один прокол пальця для забору крові, скорочення часу для отримання результатів тестування та початку лікування, зниження витрат на реагенти порівняно з двома окремими тестами на ВІЛ та сифіліс, зменшення витрат на зберігання та транспортування зразків [9]. Економічна доцільність ШТВС у допологовому нагляді вивчена та доведена методом моделювання для чотирьох країн із різною поширеністю ВІЛ і сифілісу — Південно- Африканська Республіка, Кенія, Колумбія, Україна [12].
Україна, разом з іншими країнами Європейського регіону ВООЗ, прагне до валідації ЕПМД та імплементації інноваційних заходів з цієї метою. За результатами висновків міжнародних експертів ВООЗ після робочих візитів в Україну, основними проблемами в країні стали несвоєчасність початку антиретровірусної терапії (далі — АРТ) ВІЛ-позитивних вагітних на тлі високого показника раннього взяття на облік вагітних для антенатального спостереження (87%), що може бути пов’язано, зокрема з затримкою результатів тестування на ВІЛ на етапі первинного тестування вагітних, та, як наслідок, — несвоєчасним початком лікування. Рівень охоплення вагітних тестуванням на сифіліс нижче, ніж на ВІЛ, у межах між 5 та 25%, залежно від регіону; щорічно збільшується кількість хворих на сифіліс з пізньою та неуточненою формами сифілісу. Також в Україні спостерігається низький рівень якості та надійності лабораторних даних щодо сифілісу. Наявна рутинна практика тестування вагітних на ВІЛ та сифіліс з використанням інструментальних методів у лабораторних умовах є тривалою та зменшує якість надання медичної допомоги.
Отже питання доступності та якісної організації процесу діагностики ВІЛ-інфекції та сифілісу у вагітних є актуальним і зумовлює необхідність його удосконалення в Україні. Впровадження тестування вагітних за допомогою ШТВС та його масштабування потребує окремого вивчення, що було здійснено у межах пілотного проєкта «Впровадження використання подвійних швидких (експрес) тестів для діагностики ВІЛ та сифілісу в АНК, з подальшою імплементацією в систему охорони здоров’я України» (далі — пілотний проєкт).
Мета дослідження: вивчити можливість та доцільність впровадження ШТВС для скринінгової діагностики ВІЛ- інфекції та сифілісу в антенатальних клініках м. Києва.
Матеріали і методи
Пілотний проєкт впроваджувався ДУ «Центр громадського здоров’я Міністерства охорони здоров’я України» за фінансової підтримки Глобального фонду для боротьби зі СНІДом, туберкульозом та малярією із залученням національних експертів та фахівців антенатальних клінік м. Києва.
Для виконання проєкту було сформульовано декілька основних завдань, зокрема визначення показників результативності скринінгового тестування на ВІЛ та сифіліс з використанням ШТВС та порівняння їх з результатами рутинного тестування за допомогою інструментальних методів (далі — ІМ) та оцінка готовності персоналу АНК проводити тестування вагітних на ВІЛ та сифіліс з використанням ШТВС.
Обстеження вагітних за допомогою комбінованих тестів проводили на території столиці у семи АНК (жіночих консультаціях) серед вагітних, які звернулися по медичний нагляд перебігу вагітності (n=1 496).
Детальна характеристика цільових груп дослідження, критеріїв включення та виключення представлена у табл. 1.
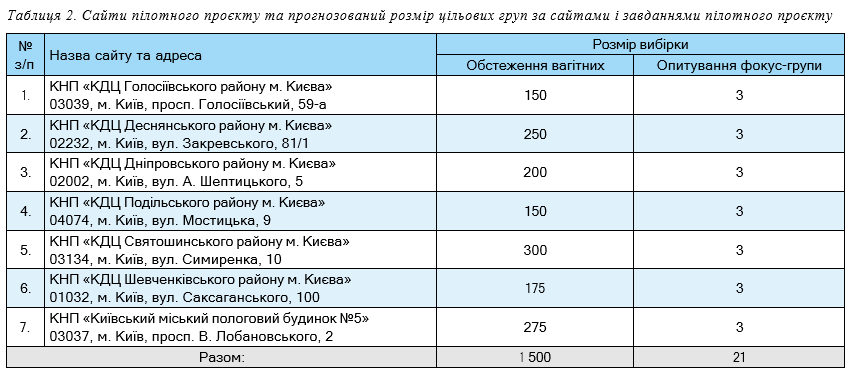
Вибір сайтів пілотного проєкту та розрахунки розміру вибірки за кожним сайтом ґрунтувалися на даних офіційної статистики, а саме окремих показниках форми звітності №21 «Звіт про медичну допомогу вагітним, роділлям та породіллям за 20 рік» та додаткових розрахункових показниках по м. Київ за 2021 рік. Обрані 7 закладів охорони здоров’я (далі — ЗОЗ) відповідали критеріям відбору сайтів дослідження, а саме: мали у структурі закладу жіночі консультації з високим рівнем навантаження щодо надання амбулаторної медичної допомоги вагітним у м. Київ.
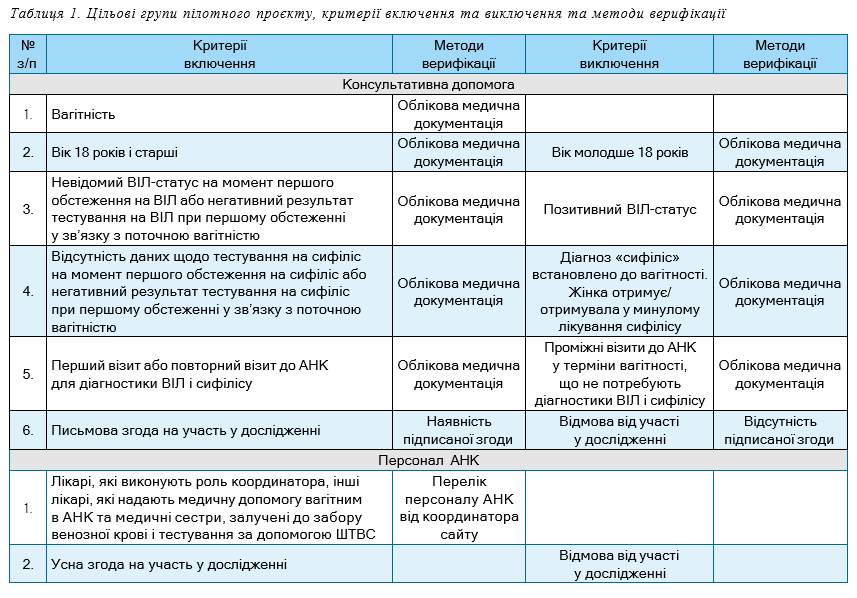
У межах виконання завдання щодо оцінки готовності персоналу АНК проводити тестування вагітних на ВІЛ та сифіліс з використанням ШТВС було проведено три фокус-групи (така кількість фокус-груп вважається мінімальною для проведення якісних досліджень). Кількість учасників кожної фокус-групи знаходилась в межах оптимальної кількості — 4–12 осіб.
Заплановані сайти пілотного проєкту і розмір цільової групи за сайтами відповідно до визначених завдань представлено у табл. 2.
Протягом одного візиту вагітних здійснювали такі дії:
- залучення до дослідження;
- дотестове консультування у зв’язку з тестуванням на ВІЛ та сифіліс;
- збір соціодемографічної та медичної інформації;
- тестування на ВІЛ та сифіліс з використанням ШТВС, а також забір венозної крові для подальшого тестування на ВІЛ та сифіліс з використанням ІМ;
- проведення опитування;
- у разі отримання позитивного результату тесту- вання на ВІЛ та/або сифіліс, перенаправлення до іншого ЗОЗ для встановлення остаточного діагнозу й отримання лікування.
Інформацію про повторний візит для отримання результатів тестування на ВІЛ та сифіліс з використанням ІМ, а також результати перенаправлення до іншого ЗОЗ у разі отримання позитивного результату тестування на ВІЛ та/або сифіліс отримували безпосередньо від вагітної та/або лікаря акушера-гінеколога АНК.
Перед проведенням фокус-груп про кожного учасника збиралася стисла соціодемографічна інформація, під час проведення фокус-груп проводився цифровий аудіозапис.
Під час пілотного проєкту тестування здійснювалося із застосуванням комбінованого швидкого тесту «Швидка відповідь Експрес-тест ВІЛ 1+2/Сифіліс Комбо» (назва англійською мовою — First Response® HIV1+2/ Syphilis Combo Card Test). Для цих тестів, відповідно до інформації виробника, чутливість 100% і специфічність 99,5% становили для тестування на ВІЛ, трепонемний компонент має чутливість 99% і специфічність 100% [5]. Послідовність процедур при проведенні лабораторного дослідження з діагностики ВІЛ-інфекції та сифілісу із застосуванням комбінованих швидких тестів виконувалась відповідно до стандартних операційних процедур, розроблених у межах пілотного проєкту.
Обстеження вагітних на ВІЛ-інфекцію та сифіліс із застосуванням ІМ здійснювали відповідно до чинних галузевих стандартів.
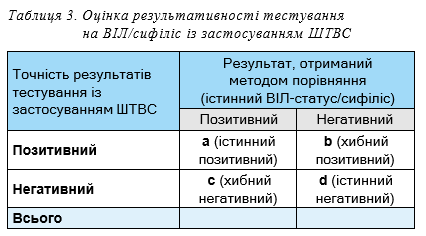
Визначення показників результативності скринін- гового тестування на ВІЛ та сифіліс з використанням ШТВС базувалося на порівнянні з результатами тестування з використанням ІМ: 1) були розраховані показники чутливості та специфічності методу діагностики ВІЛ/сифілісу із застосуванням ШТВС; 2) розраховані показники значущості позитивного (PPV) та негативного (NPV) прогностичних значень отриманих результатів при тестуванні ШТВС; 3) отримані показники абсолютної кількості та відсоток недійсних результатів тестування із застосуванням ШТВС (табл. 3).
За результатами обрахунку було визначено, яка частина всіх тестів дала правильні результати (тобто істинно негативні або істинно позитивні) та хибно негативні або хибно позитивні результати відносно до всіх, де:
Чутливість = а/(а+с)*100%;
Специфічність = d/(b+d)*100%;
PPV = a/(a+b)*100%;
NPV = d/(c+d)*100%.
Усі медичні працівники АНК перед початком польового етапу пройшли навчання щодо процедур дослідження, збору зразків крові, тестування на ВІЛ та сифіліс із застосуванням ШТВС, процедур безпеки, заповнення медичних форм, передбачених в межах реалізації проєкту. Початок польового етапу пілотного проєкту відбувся 18 жовтня 2021 р.
Результати досліджень та їх обговорення
Результати досліджень та їх обговорення
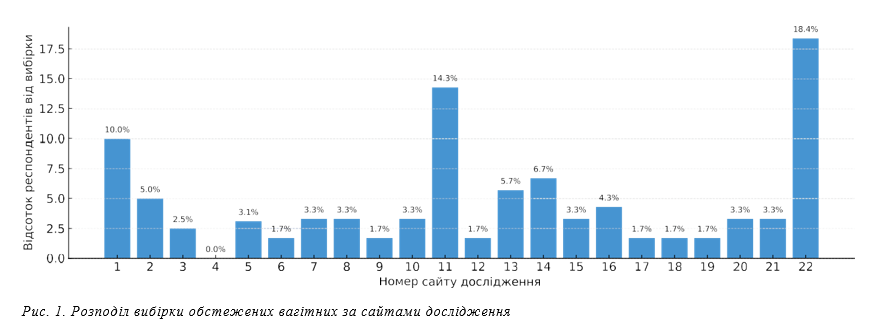
Відповідно до сформульованих завдань проєкту було набрано 1 510 респонденток з числа вагітних жінок, 14 записів виключено через невідповідність критеріям відбору, відтак до обстеження було залучено 1 496 жінок. Набір респондентів проводився у м. Києві на базі 22-х ЗОЗ та їх філій (рис. 1).
При проведені аналізу анкетних даних вагітних учасниць дослідження встановлено, що їх середній вік становив 30,2±5,3 року; вищу освіту мали 1 070 (71,5%) респонденток, середню і початкову — 411 (27,5%) і 15 (1,0%) відповідно. Про зареєстрований шлюб повідомили 1 119 (74,8%) учасниць, перебували у незареєстрованому шлюбі — 346 (23,1%), не перебувала у шлюбі 31 (2,1%) жінка; 1 032 (69,0%) респонденток вказали, що повністю або частково працевлаштовані або мають власну справу. З числа опитаних 184 (12,3%) вагітних були безробітними та не шукали роботу, перебували у декретній відпустці або були домогосподарками — 207 (13,8%) учасниць. Серед усіх вагітних, залучених до пілотного проєкту, 635 (42,4%) жінок мали першу за порядком вагітність, 501 (33,5%) — другу вагітність, 201 (13,4%) — третю вагітність, дві (0,1%) жінки повідомили про одинадцяту вагітність.
Скринінг симптомів щодо наявності наркотичної залежності проводився за допомогою шкали АССИСТ(The Alcohol, Smoking and Substance Involvement Screening Test (ASSIST)) відповідно до Міжнародної класифікації хвороб 10-го перегляду (ICD-10 Checklist). Згідно з інструкцією щодо використання АССИСТ, діагноз залежності має бути встановлений, якщо 3 або більше симптомів наявні протягом 12 місяців і більше. З усіх респонденток за допомогою АССИСТ було визначено діагноз залежності в 1 учасниці (наявність 3 симптомів протягом 12 місяців). Ще у двох учасниць було визначено одночасно 2 симптоми і в однієї учасниці — 3 симптоми, що тривали до 6 місяців.
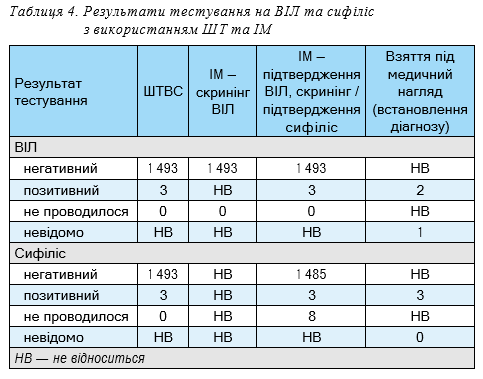
Усі вагітні, які відповідали критеріям включення та надали згоду на учать у пілотному проєкті, були протестовані на наявність серологічних маркерів ВІЛ та сифілісу з використанням ШТВС (n=1 496). Серед проведених ШТВС тестувань на ВІЛ та сифіліс було отримано по три позитивних результати (всього шість позитивних результатів). Вагітних, які одночасно мали позитивний результат тестування на ВІЛ та сифіліс виявлено не було. При проведені тестування за допомогою ШТВС не було отримано жодного недійсного результату (табл. 4).
З використанням ІМ на ВІЛ було протестовано також усіх вагітних (n=1 496) та отримано три позитивних результати у тих же вагітних, у яких відмічались позитивні результати на ВІЛ з використанням ШТВС. Тобто результати тестування на ВІЛ з використанням ШТ та ІМ співпали. Усі три вагітні з позитивним результатом тестування на ВІЛ були направлені до КМКЛ №5 для встановлення діагнозу, взяття під медичний нагляд та призначення АРТ; дві з трьох учасниць встали на облік та почали прийом АРТ. Дані щодо встановлення діагнозу, взяття на облік та початку АРТ третьої учасниці відсутні, після направлення до КМКЛ №5 зв’язок з цією вагітною був втрачений, до АНК жінка більше не поверталась.
З використанням ІМ на сифіліс було протестовано 1 488 жінок, тобто не були отримані дані щодо тестування на сифіліс з використанням ІМ для 8 вагітних. Це пов’язано з тим, що зазначеним учасницям друге тестування на сифіліс протягом вагітності проводилося з використанням ІМ. Згідно з чинним законодавством друге тестування на сифіліс здійснюється пізніше ніж друге тестування на ВІЛ, тобто ці 8 жінок отримали негативний результат першого тестування на ВІЛ та сифіліс з використанням ІМ, та були вдруге протестовані на ВІЛ з використанням ІМ, але друге тестування на сифіліс з використанням ІМ відбулося вже після закінчення польового етапу дослідження. Для 5 жінок, у зв’язку з їх приналежністю до ключових груп підвищеного ризику щодо інфікування ВІЛ, тестування на ВІЛ проводилося втретє, відповідно на момент включення їх до дослідження вони вже двічі були обстежені на сифіліс з використанням ІМ.
При проведенні тестування на сифіліс з викори- станням ІМ було отримано три позитивних результати. Дві вагітні отримали позитивний результат тестування на сифіліс з використанням ШТВС та ІМ. Одна вагітна мала позитивний результат тестування на сифіліс з використанням ШТВС та негативний результат тестування з використанням ІМ. Ще одна вагітна, навпаки, мала позитивний результат тестування на сифіліс з використанням ІМ та негативний результат з використанням ШТВС.
Згідно з унормованим алгоритмом тестування на сифіліс, позитивний результат, отриманий з використанням швидких тестів, потребує підтвердження інструментальним методом. Трьох учасниць з позитивним результатом тестування ІМ на сифіліс було направлено до лікаря дерматовенеролога для встановлення діагнозу та призначення специфічного лікування. Усі жінки звернулися до шкірно-венерологічного диспансеру, їм було підтверджено діагноз та розпочато лікування сифілісу.
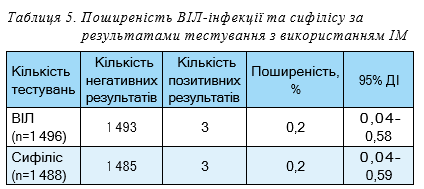
Показники результативності скринінгового тестування на ВІЛ та сифіліс з використанням ШТВС та рутинного тестування за допомогою ІМ розраховувалися серед жінок, яким проведено тестування як ІМ, так і ШТВС: ВІЛ — 1 496 жінок, сифіліс — 1 488 жінок.
Показники поширеності становили: ВІЛ — 0,2% (95% ДІ: 0,04–0,58) та сифілісу 0,2% (95% ДІ: 0,04–0,59)
(табл.5).
Показники чутливості, специфічності, значущості позитивного (PPV) та негативного (NPV) прогностичних результатів скринінгового тестування із застосуванням ШТВС наведені у табл. 6 та 7.
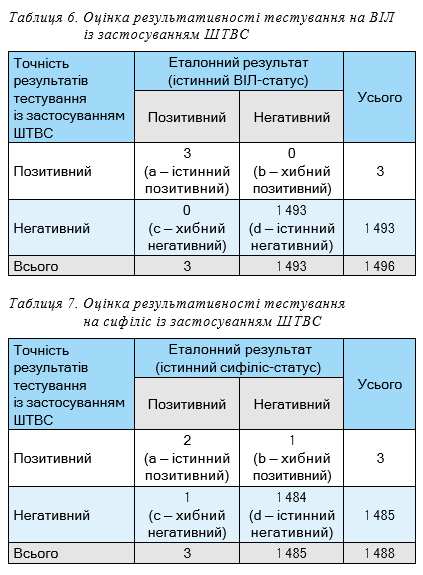
Показники результативності скринінгового тестування на ВІЛ із застосуванням ШТВС становили: чутливість — 100%, специфічність — 100%, PPV — 100% та NPV — 100%, де:
Чутливість = а/(а+с)*100%=3/(3+0)*100%=100%;
Специфічність = d/(b+d)*100%=1 493/
(0+1493)*100%=100%; PPV = a/(a+b)=3/(3+0)*100=100%;
NPV = d/(c+d)=1 493/(0+1 493)*100=100%.
Показники результативності скринінгового тестування на сифіліс із застосуванням ШТВС становили: чутливість — 66,7%, специфічність — 99,9%, PPV — 66,7% та NPV — 99,9%, де:
Чутливість = а/(а+с)*100%=2/(2+1)*100%=66,7%; Специфічність = d/(b+d)*100%=1 484/(1+1 484)*100%=99,9%; PPV = a/(a+b)=2/(2+1)*100=66,7%; NPV = d/(c+d)=1 484/(1+1 484)*100=99,9%.
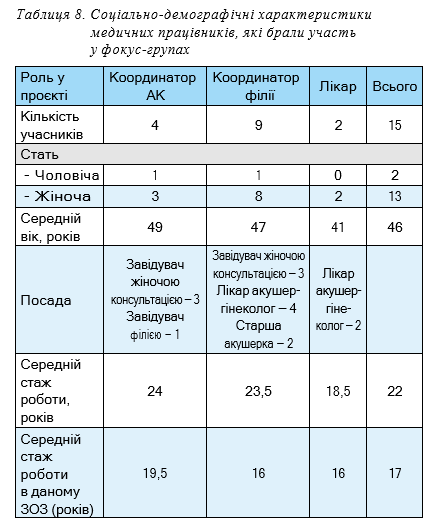
У межах виконання завдання щодо оцінки готовності персоналу АНК проводити тестування вагітних на ВІЛ та сифіліс з використанням ШТВС було проведено три фокус-групи (ФГ) по 5 учасників кожна, тобто 15 учасників проти 20–22 медичних працівників, згідно з протоколом (табл. 8). Дані зміни були зумовлені воєнним станом, введеним у країні, що призвело до змін у роботі співробітників АНК, відсутністю зв’язку з деякими учасниками проєкту, відсутністю безпечного місця для участі у ФГ, а також онлайн форматом дискусії, в якому важче утримувати фокус більшої аудиторії учасників.
В опитуванні взяли участь медичні працівники з 6-ти районів Києва:
- Голосіївський — 2 учасники;
- Дніпровський — 3 учасники;
- Подільський — 2 учасники;
- Святошинський — 3 учасники;
- Солом’янський — 2 учасники;
- Шевченківський — 3 учасники.
Незважаючи на відсутність попереднього досвіду та деякі побоювання медичного персоналу щодо правильної організації роботи, ведення документації та бажання вагітних пройти ШТВС, усі учасники ФГ відзначили, що комбіновані тести зручні у використанні, виконання проєкту не призвело до значного додаткового навантаження в роботі АНК. Впровадження у практику ШТВС жодним чином не порушило правила роботи в маніпуляційному кабінеті, процес діяльності відбувався як звичайно, ШТВС легко інтегрувалися у звичайну практику. У перший день взяття на облік у АНК вагітних обстежували рутинними методами і разом з цим проводили ШТВС. Найбільше часу забирало саме пояснення вагітним — для чого, з якою метою це робиться. Метод зарекомендував себе як більш доступний, швидкий та такий, що потребує менше всіляких логістичних навантажень на структуру.
Загалом, підсумовуючи наведене вище, можна дійти загального висновку про ефективність використання ШТВС — визначення показників результативності скринінгового тестування на ВІЛ та сифіліс з використанням комбінованих тестів та порівняння з результатами тестування з використанням ІМ, що було проведене шляхом розрахунку показників чутливості та специфічності методу діагностики ВІЛ/сифілісу, показників значущості позитивного (PPV) та негативного (NPV) прогностичних значень отриманих результатів та показників абсолютної кількості та відсотку недійсних результатів тестування підтвердило рівноцінність результатів обох методів. При цьому, показники результативності скринінгового тестування на ВІЛ з використанням ШТВС становили регламентовану чутливість та специфічність (майже 100%), однак для сифілісу отримані розрахунки чутливості виявилися значно гіршими, ніж мали б бути — 66,7% замість очікуваної мінімальної межі 93,04%, відповідно до [13]. Отже, оцінка чутливості до збудника сифілісу з використанням First Response® HIV1+2/Syphilis Combo Card Test потребує додаткового вивчення з більшим розміром вибірки.
Досягнення успіху впровадження ШТВС у різні ЗОЗ (жіночі консультації, акушерські стаціонари, перинатальні центри, центри репродуктивної та перинатальної медицини, заклади первинної медико- санітарної допомоги, лабораторії діагностики ІПСШ тощо) можливо за умови відповідної та достатньої підготовки спеціалістів до впровадження ШТВС в рутинну практику в Україні. Учасниками дослідження за результатами фокус-груп підтверджено, що ШТВС не впливають негативно на рутинні практики тестування у закладі, що свідчить про можливість інтегрування ШТВС у стандартні процедури надання медичної допомоги. Незважаючи на відсутність попереднього досвіду, усі учасники фокус-груп відзначили, що швидкі тести легкі у використанні, проєкт не вплинув на навантаження медичних працівників.
Основні обмеження виконання пілотного проєкту були пов’язані з військовим станом та військовими діями в країні, що суттєво вплинуло на графік роботи ЗОЗ. Зокрема, це скорочення часу роботи до однієї зміни або взагалі дистанційно, зменшення кількості вагітних, що звертались по медичну допомогу, евакуація персоналу клінік тощо. Також відмічено суттєвий вплив на логістику та маршрутизацію між медичними закладами, скорочення переліку обстежень вагітних у лабораторіях при КДЦ, ускладнення процедур отримання лабораторних результатів, що відтерміновувало початок лікування пацієнтки у разі отримання позитивних результатів.
Суттєвим обмеженням при виконанні проєкту була відсутність нормативної бази, яка б дозволила робити дослідження вагітним за допомогою ШТВС, що, зі свого боку, потребувало відповідно дозволу міської адміністрації охорони здоров’я на проведення такого проєкту та навчання персоналу пілотних ЗОЗ методу використання ШТВС.
Не зважаючи на певні складнощі при виконанні проєкту, аналіз отриманих результатів дозволяє зробити загальний висновок щодо можливості використання ШТВС в Україні та рекомендувати подальше впровадження тестів зазначеного формату для скринінгу на наявність серологічних маркерів ВІЛ та сифілісу з метою покращення доступності медичної допомоги вагітним і досягнення довгострокових результатів у сфері охорони здоров’я.
Висновки
Інтегроване тестування вагітних на ВІЛ та сифіліс є ефективною стратегією громадського здоров’я, що дає змогу запобігти значній кількості випадків вертикальної передачі інфекцій. Впровадження швидких комбінованих тестів, особливо у країнах із обмеженими ресурсами, має потенціал для суттєвого зниження рівня материнської та дитячої смертності.
Результати пілотного проєкту підтверджують можливість інтеграції ШТВС у рутинну антенатальну практику. Це підтверджується досягненням запланованої вибірки у визначені терміни (1 496 з 1 500 запланованих) та позитивними відгуками вагітних щодо готовності пройти тестування за допомогою швидких тестів.
Показники результативності скринінгового тестування на ВІЛ з використанням ШТВС становили: чутливість — 100%, специфічність — 100%, PPV — 100% та NPV — 100%; скринінгового тестування на сифіліс: чутливість — 66,7%, специфічність — 99,9%, PPV — 66,7% та NPV — 99,9%. Частка виявлених випадків ВІЛ становила 0,2%, сифілісу — також 0,2%, що відповідає національній статистиці.
Медичні працівники високо оцінили доцільність, легкість і зручність використання ШТВС. Зазначено, що використання тестів не створює значного навантаження на медичних працівників навіть у складних умовах воєнного часу.
Відсутність нормативного регулювання застосування ШТВС у системі охорони здоров’я залишається важливою перешкодою. Чинний національний алгоритм тестування на ВІЛ (наказ МОЗ України № 794 вiд 05.04.2019) не враховує використання ШТВС. Також не унормовано тестування на сифіліс у закладах первинної медико- санітарної допомоги відповідно до наказу МОЗ України № 504 від 19.03.2018.
Загалом впровадження ШТВС в антенатальні клініки є доцільним, ефективним та відповідає сучасним викликам системи охорони здоров’я України, сприяє пришвидшенню діагностики, покращенню доступності медичних послуг та забезпеченню раннього початку лікування ВІЛ і сифілісу. Рекомендується розширити використання ШТВС у закладах охорони здоров’я різних типів (антенатальні клініки, акушерські стаціонари, перинатальні центри тощо), особливо у віддалених районах та запровадити тестування не тільки для вагітних, але й для їхніх статевих партнерів та представників ключових та уразливих груп щодо інфікування ВІЛ.
Література
-
Screening and Testing for HIV, Viral Hepatitis, STD & Tuberculosis in Pregnancy. CDC, 2024. Available from: https://www.cdc.gov/pregnancy-hiv-std-tb-hepatitis/php/screening/index.html?utm_source.
-
AGOG. Prenatal and Perinatal Human Immunodeficiency Virus Testing. Committee Opinion Number 752, September 2018. Available from: https://www.acog.org/clinical/clinical-guidance/committee-opinion/articles/2018/09/prenatal-and-perinatal-human-immunodeficiency-virus-testing?utm_source.
-
G. N. Asher, M. Viswanathan, A. Takyi [et al]. Screening for Syphilis Infection During Pregnancy. Updated Evidence Report and Systematic Review for the US Preventive Services Task Force. JAMA. 2025;333;(22):2015-2017. doi:10.1001/jama.2025.1179.
-
ACOG Recommends Obstetrician-Gynecologists Increase Syphilis Screening for Pregnant Individuals. ACOG, 2024. Available from: https://www.acog.org/news/news-releases/2024/04/acog-recommends-obstetrician-gynecologists-increase-syphilis-screening-for-pregnant-individuals?utm_source.
-
Dual HIV/syphilis rapid diagnostic tests can be used as the first test in antenatal care. WHO, 2019. Available from: https://www.who.int/publications/i/item/WHO-CDS-HIV-19.38.
-
R. Kularatne, K. Blondeel, M. Kasaro [et al.]. Clinic-based evaluation of point-of-care dual HIV/syphilis rapid diagnostic tests at primary healthcare antenatal facilities in South Africa and Zambia. BMC Infectious Diseases. 2024. Vol. 24. A. 600. https://bmcinfectdis.biomedcentral.com/articles/10.1186/s12879-024-09463-1?utm_source.
-
Elimination of mother-to-child transmission of HIV, syphilis and hepatitis B. WHO, 2024. Available from: https://www.who.int/initiatives/triple-elimination-initiative-of-mother-to-child-transmission-of-hiv-syphilis-and-hepatitis-b?utm_source.
-
WHO. Global Guidance on Criteria and Processes for Validation: Elimination of Mother-to-child Transmission of HIV, Syphilis and Hepatitis b virus. 2021. https://iris.who.int/bitstream/hand le/10665/349550/9789240039360-eng.pdf?sequence=1&isAllowed=y.
-
K. Withers, C. Bristow, M. Nguyen, C. Stafylis, L. M. Giang, J. D. Klausner. A field evaluation of a rapid dual immunoassay for human immunodeficiency virus and syphilis antibodies, Hanoi, Vietnam. STD AIDS. 2019 Feb;30(2):173-180. doi: 10.1177/0956462418802685.
-
Kasaro M. P., Bosomprah S., Taylor M. M., Sindano N., Phiri C., Tambatamba B., Malumo S., Freeman B., Chibwe B., Laverty M., Owiredu M. N., Newman L., Sikazwe I. Field performance evaluation of dual rapid HIV and syphilis tests in three antenatal care clinics in Zambia. J STD AIDS. 2019 Mar;30(4):323–328. doi: 10.1177/0956462418800872.
-
Olugbenga I., Taiwo O., Laverty M., Ngige E., Anyaike C., Bakare R., Ogunleye V., Peterson Maddox B. L., Newman D. R., Gliddon H. D., Ofondu E., Nurse-Findlay S., Taylor M. M. Clinic-based evaluation study of the diagnostic accuracy of a dual rapid test for the screening of HIV and syphilis in pregnant women in Nigeria. PLoS One. 2018 Jul 10;13(7):e0198698. doi: 10.1371/journal.pone.0198698.
-
C. C. Bristow, E. Larson, L. J. Anderson, J. D. Klausner. Cost-effectiveness of HIV and syphilis antenatal screening: a modelling study. Sex Transm Infect. 2016 Aug;92(5):340-6. doi: 10.1136/sextrans-2015-052367.
-
Angel-Müller E., Grillo-Ardila C. F., Amaya-Guio J., Torres-Montañez N. A., Vasquez-Velez L. F. Point of care rapid test for diagnosis of syphilis infection in men and nonpregnant women. Cochrane Database of Systematic Reviews 2018, Issue 5. Art. No.: CD013036. http:www.ncbi.nlm.nih.gov/pmc/articles/PMC6494531/
Відомості про авторів:
Марциновська В. А. — к. мед. н., старший науковий співробітник лабораторії епідеміології інфекційних хвороб ДУ «Інститут епідеміології та інфекційних хвороб ім. Л. В. Громашевського НАМН України»; Головний фахівець відділу управління та протидії ВІЛ-інфекції
ДУ «Центр громадського здоров’я МОЗ України», магістр громадського здоров’я.
ORCID:0000-0001-8283-0179
Недужко О. О. — заступник директора з наукових питань ТОВ «Європейський інститут політики громадського здоров’я».
ORCID: 0000-0002-9539-246X
Андріанова І. В. — імунолог референс-лабораторії з діагностики ВІЛ/СНІДу, вірусних та особливо небезпечних патогенів ДУ «Центр громадського здоров’я МОЗ України».
Нестерова О. Є. — керівник відділу наукових досліджень ДУ «Центр громадського здоров’я МОЗ України».
ORCID: 0000-0002-6815-7894
Зезюлін О. О. — науковий директор БО «Український інститут політики громадського здоров’я».
ORCID: 0000-0003-1363-593X
Кислих О. М. — науковий співробітник лабораторії епідеміології інфекційних хвороб ДУ «Інститут епідеміології та інфекційних хвороб ім. Л. В. Громашевського НАМН України».
ORCID: 0009-0003-7387-2109
Максименок О. В. — к. б. н., старший науковий співробітник лабораторії епідеміології інфекційних хвороб ДУ «Інститут епідеміології та інфекційних хвороб ім. Л. В. Громашевського НАМН України».
ORCID: 0009-0004-3566-2124
Information about the authors:
Martsynovska V. A. — Candidate of Medical Sciences, senior researcher at the laboratory of epidemiology of infectious diseases, SI «L. V. Hromashevsky Institute of epidemiology and infectious diseases of NAMS of Ukraine»; Chief Specialist of HIV management and counteraction department, SI «Public Health Center of the Ministry of Health of Ukraine».
ORCID:0000-0001-8283-0179
Neduzhko O. O. — deputy director for science, LLC «The European Institute of Public Health Policy».
ORCID: 0000-0002-9539-246X
Andrianova I. V. — immunologist of the reference laboratory for diagnosis of HIV/AIDS, viral and particularly dangerous pathogens, SI «Public Health Center of the Ministry of Health of Ukraine».
Nesterova O. Ye. — head of the scientific research department, SI «Public Health Centre of the Ministry of Health of Ukraine».
ORCID: 0000-0002-6815-7894
Zeziulin O. O. — scientific director, CO «Ukrainian Institute on Public Health Policy»
ORCID: 0000-0003-1363-593X
Kyslykh O. M. — researcher at the laboratory of epidemiology of infectious diseases, SI «L. V. Hromashevsky Institute of epidemiology and infectious diseases of NAMS of Ukraine».
ORCID: 0009-0003-7387-2109
Maksymenok O. V. — Сandidate of Biological Sciences, senior researcher at the laboratory of epidemiology of infectious diseases, SI «L. V. Hromashevsky Institute of epidemiology and infectious diseases of NAMS of Ukraine».
ORCID: 0009-0004-3566-2124
