Флавовір® (капсули): ефективність при СOVID-19

УДК: 615.281.8:615.03 DOI: https://doi.org/10.61948/prevmed-2024-4-48
Т. В. Чабан1, Р. О. Харитонюк2, О. Й. Гриневич3, В. M. Бочаров1, Г. В. Максимчук2, Ю. О. Золотухіна3
1. Одеський Національний медичний університет, м. Одеса, Україна
2. КНП «ЦМЛ» РМР, м. Рівне, Україна
3. ТОВ «НВК «Екофарм», м. Київ, Україна
Анотація. Аналізуються матеріали результатів клінічного дослідження «Багатоцентрове, рандомізоване, подвійне-сліпе дослідження ефективності та переносимості препарату ФЛАВОВІР® (капсули) у пацієнтів з СOVID-19 середнього ступеня тяжкості, що отримують базисну терапію» (ІІ фаза). Досліджуваний препарат ФЛАВОВІР® (капсули) є розробкою ТОВ «НВК «Екофарм», представленою до клінічного вивчення, з метою доведення противірусної активності щодо вірусів SARS-CoV-2 та вирішення питання про можливість реєстрації препарату в Україні як противірусного засобу прямої дії. ФЛАВОВІР® (капсули) є новою лікарською формою зареєстрованого в Україні в 2001 році та широко застосовуваного лікарського засобу ПРОТЕФЛАЗІД® (краплі). Клінічне випробування проведено з метою підтвердження переважаючої ефективності ФЛАВОВІР® (капсули) при курсових прийомах на фоні стандартної базисної терапії у пацієнтів з СOVID-19 середнього ступеня тяжкості порівняно з плацебо на фоні стандартної базисної терапії у пацієнтів з СOVID-19 середнього ступеня тяжкості.
Матеріали та методи. Суб’єкти дослідження — 162 пацієнти з СOVID-19 середнього ступеня тяжкості. Пацієнти на основі методу блокової рандомізації у співвідношенні 1:1:1 розподілені на 3 групи по 54 пацієнти. Пацієнтам І групи призначали досліджуваний препарат ФЛАВОВІР® (капсули), перорально по 1 капсулі 2 рази на добу протягом 14 діб та одночасно плацебо по 1 капсулі 2 рази на добу протягом 14 діб (для забезпечення «подвійного маскування») на фоні стандартної базисної терапії. Пацієнтам ІІ групи призначали препарат ФЛАВОВІР® (капсули), перорально по 2 капсули 2 рази на добу протягом 14 діб на фоні стандартної базисної терапії. Пацієнтам ІІІ групи призначали препарат плацебо (капсули) перорально по 2 капсули 2 рази на добу протягом 14 діб на фоні стандартної базисної терапії. Ефективність лікування оцінювали, враховуючи такі первинні змінні ефективності: -час (у добах) до настання події, що характеризується відсутністю гіпертермії (<37,0 °С) протягом не менш ніж 3-х діб при відсутності або мінімальній вираженості симптомів ГРВІ (≤1 бала за вербальною аналоговою шкалою: 0–3 бали) в межах 14-добового періоду прийому препарату; -час (у добах) до моменту елімінації вірусів SARS-CoV-2 з носоглоткового мазка в межах 14-добового періоду прийому препарату. Оцінку переносимості досліджуваних препаратів проводили на підставі суб’єктивних скарг хворого, наявності та вираженості побічних реакцій/побічних явищ, даних об’єктивного огляду пацієнта та лабораторного обстеження.
Висновки. Лікування препаратом ФЛАВОВІР® (капсули) визнано ефективним у 94,4% пацієнтів групи І, у 94,4% пацієнтів групи ІІ та у 70,4% пацієнтів групи ІІІ. Не виявлено статистично значущої різниці в ефективності лікування за первинною змінною між групами І та ІІ. Між групами І і ІІІ та групами ІІ і ІІІ виявлено статистично значущу відмінність. Доведено гіпотезу про переважаючу ефективність препарату ФЛАВОВІР® (капсули) в двох дозуваннях порівняно з плацебо на фоні стандартної базисної терапії у пацієнтів з СOVID-19 середнього ступеня тяжкості. Дослідження показало, що препарат ФЛАВОВІР® (капсули) є ефективним у лікуванні пацієнтів з COVID-19, з високим відсотком позитивних результатів у групах І та ІІ. Продемонстровано статистично значущі відмінності між групами І і ІІІ та групами ІІ і ІІІ. Результати дослідження підтверджують гіпотезу щодо ефективності препарату ФЛАВОВІР® (капсули) в лікуванні COVID-19, що є важливим внеском у клінічну практику та наукові дослідження. Препарат ФЛАВОВІР® (капсули), який має високий потенціал як противірусний засіб у лікуванні COVID-19 середнього ступеня тяжкості, потребує подальшого дослідження та реєстрації в Україні.
Ключові слова: ФЛАВОВІР® (капсули), SARS-CoV-2, СOVID-19, противірусний засіб.
V. Chaban1, R. O. Kharitonyuk2, O. Yo Hrynevych3, M. Bocharov1, G. V. Maksymchuk2, Y. O. Zolotukhina3
FLAVOVIR® (CAPSULES): EFFECTIVENESS IN COVID-19
1. Odessa National Medical University, Odesa, Ukraine
2. KNP CML RMR, Rivne, Ukraine
3. LLC “SPC “Ecopharm”, Kyiv, Ukraine
Abstract. The materials of the clinical trial “Multicenter, randomized, double-blind study of the efficacy and tolerability of FLAVOVIR® (capsules) in patients with moderate COVID-19 receiving basic therapy are presented”. The investigational drug FLAVOVIR® (capsules) is a development of LLC “SPC “Ecopharm”, presented for clinical study, in order to prove antiviral activity against SARS-CoV-2 viruses and to resolve the issue of the possibility of registering the drug in Ukraine as a direct-acting antiviral agent. FLAVOVIR® (capsules) is a new dosage form of the drug PROTEFLAZID® (drops), registered in Ukraine in 2001 and widely used. A clinical trial was conducted to confirm the predominant efficacy of FLAVOVIR® (capsules) in course doses against the background of standard baseline therapy in patients with COVID-19, moderate severity compared to placebo against the background of standard baseline therapy in patients with moderate COVID-19.
Materials and methods. The study subjects were 162 patients with COVID-19 of moderate severity. Patients based on the method of block randomization in a ratio of 1:1:1 were divided into 3 groups of 54 patients. Patients of group I were prescribed the investigational drug FLAVOVIR® (capsules), orally 1 capsule 2 times a day for 14 days and, at the same time, placebo 1 capsule 2 times a day for 14 days (to ensure “double masking”) against the background of standard basic therapy. Group II patients were prescribed the drug FLAVOVIR® (capsules), orally 2 capsules 2 times a day for 14 days against the background of standard basic therapy. Patients of group III were prescribed a placebo, capsules, orally 2 capsules 2 times a day for 14 days against the background of standard basic therapy. The effectiveness of treatment was evaluated taking into account the following primary efficacy variables: – time (in days) before the onset of an event characterized by the absence of hyperthermia (<37.0 °C) for at least 3 days in the absence or minimal severity of ARVI symptoms (≤1 point on a verbal analog scale: 0–3 points) within a 14-day period of taking the drug; – the time (in days) until the elimination of SARS-CoV-2 viruses from the nasopharyngeal smear within the 14-day period of taking the drug. The tolerance of the studied drugs was assessed on the basis of the patient’s subjective complaints, the presence and severity of adverse reactions/side effects, the data of an objective examination of the patient and laboratory examination.
Conclusions. Treatment with FLAVOVIR® (capsules) was found to be effective in 94.4% of group I patients, in 94.4% of group II patients and in 70.4% of group III patients. No statistically significant difference in the efficacy of treatment by primary variable between groups I and II was found. A statistically significant difference was found between groups I and III and groups II and III. The hypothesis of the prevailing efficacy of FLAVOVIR® (capsules) in two dosages compared to placebo against the background of standard baseline therapy in patients with moderate COVID-19. The study showed that the drug FLAVOVIR® (capsules) is effective in the treatment of patients with COVID-19, with a high percentage of positive results in groups I and II. Statistically significant differences between groups I and III and groups II and III have been demonstrated. The results of the study confirm the hypothesis about the effectiveness of FLAVOVIR® (capsules) in the treatment of COVID-19, which is an important contribution to clinical practice and scientific research. The drug FLAVOVIR® (capsules), which has a high potential as an antiviral agent in the treatment of moderate COVID-19, requires further research and registration in Ukraine.
Key words: FLAVOVIR® (capsules), SARS-CoV-2, COVID-19, antiviral agent.
Вступ.
Актуальність. Пандемія COVID-19, спричинена вірусом SARS-CoV-2, стала серйозним викликом для систем охорони здоров’я по всьому світу. Незважаючи на досягнення у розробці вакцин, ефективне лікування COVID-19 залишається надзвичайно важливим, особливо для пацієнтів із середнім і важким ступенем тяжкості захворювання. Захворювання може мати широкий спектр клінічних проявів — від легких симптомів до важких ускладнень, таких як гострий респіраторний дистрес-синдром (ГРДС), сепсис, мультиорганна недостатність і летальний результат. Особливу загрозу становлять пацієнти з груп ризику — літні люди, пацієнти з хронічними захворюваннями (цукровий діабет, серцево-судинні хвороби, ожиріння тощо). Середній ступінь тяжкості захворювання потребує комплексного підходу до лікування, який включає противірусні засоби, антибіотики (у випадку бактеріальних ускладнень), імунотерапію, підтримуючу терапію і профілактику тромбозів [1, 2, 3].
Огляд існуючих підходів до базисної терапії [4, 5, 6,7, 8]. Базисна терапія COVID-19 включає використання етіотропних засобів і підтримуючих препаратів, які спрямовані на запобігання розвитку тяжких і ускладнених форм хвороби та подальшого її прогресування,
полегшення симптомів, попередження ускладнень та покращення загального стану пацієнтів. Основні компоненти базисної терапії направлені на пригнічення реплікації вірусів, підтримки функцій організму та запобігання розвитку серйозних ускладнень, таких як гострий респіраторний дистрес-синдром, тромбози або сепсис.
Противірусні препарати. Одним із ключових компонентів базисної терапії є використання противірусних засобів, таких як ремдесивір: затверджений для лікування COVID-19 в багатьох країнах. Він інгібує реплікацію вірусу, зменшуючи його кількість у організмі. Препарат показав певну ефективність у скороченні часу до одужання, однак його вплив на зниження смертності залишається обмеженим. Фавіпіравір: препарат, що також використовується для боротьби з вірусами, зокрема SARS-CoV-2, і показує ефективність у деяких випадках. Однак його застосування обмежене через недостатню кількість даних про безпеку та ефективність. Молнупіравір: пероральний противірусний препарат, у якого спостерігається ефективність у зниженні ризику госпіталізації та смертності у пацієнтів з легкими та середніми формами COVID-19. Паксловід: показаний для лікування коронавірусної хвороби у дорослих, які не потребують оксигенотерапії та належать до групи підвищеного ризику погіршення стану до тяжкої форми COVID-19.
Кортикостероїди. Дексаметазон: препарат став стандартом лікування пацієнтів із важкими формами COVID-19, які потребують кисневої підтримки або штучної вентиляції легень. Дексаметазон знижує запалення і, відповідно, ризик летальних ускладнень. Однак його ефективність для пацієнтів із середнім ступенем тяжкості менша, і використання кортикостероїдів у таких випадках має бути обмеженим.
Антикоагулянти. Через підвищений ризик тромбоутворення у пацієнтів із COVID-19, особливо середньої та важкої тяжкості, антикоагулянтна терапія (гепарин або низькомолекулярні гепарини) є важливим компонентом базисної терапії. Вона допомагає знизити ризик тромбозів та емболій, які можуть призводити до ускладнень, таких як інфаркти, інсульти або тромбоемболія легеневої артерії.
Киснева терапія. Для пацієнтів із середнім ступенем тяжкості COVID-19, у яких знижений рівень кисню в крові, часто застосовується киснева терапія. Вона включає подачу кисню через назальні канюлі або маски, що допомагає підтримати адекватне насичення крові киснем і запобігає розвитку гострої дихальної недостатності.
Імунотерапія. Тоцилізумаб: моноклональні антитіла, які блокують інтерлейкін-6 (IL-6), що відповідає за надмірну запальну реакцію в організмі. Він використовується для зниження ризику «цитокінового шторму», який часто є причиною важких ускладнень у пацієнтів із COVID-19. Моноклональні антитіла проти SARS-CoV-2: препарати на основі моноклональних антитіл (наприклад, казірівімаб та імдевімаб) використовуються для лікування пацієнтів із COVID-19 з високим ризиком ускладнень.
Антибіотики. Використання антибіотиків виправдане тільки при наявності бактеріальної ко-інфекції. COVID-19 є вірусним захворюванням, тому антибіотики неефективні проти самого вірусу, однак їх можна призначати для профілактики або лікування бактеріальних ускладнень. Як видно, на даний момент існує обмежена кількість лікарських засобів із доведеною ефективністю проти COVID-19. Використання деяких препаратів, таких як ремдесивір, дексаметазон та моноклональні антитіла, показало певні позитивні результати, однак ефективність та безпечність багатьох з них все ще досліджуються. Пошуки нових лікарських засобів, які можуть бути ефективними в боротьбі з інфекцією SARS-CoV-2 не припиняються [4, 5, 6, 7, 8, 9,10].
Отже, базисна терапія COVID-19 є комплексним підходом, спрямованим на намагання контролювати вірусне навантаження, знижувати запальні процеси та попереджувати ускладнення. Однак багато з існуючих препаратів мають обмежену ефективність або їх дія супроводжується серйозними побічними ефектами. Зважаючи на це, існує нагальна потреба в нових ефективних етіотропних засобах для терапії пацієнтів із середнім ступенем тяжкості захворювання COVID-19, оскільки пацієнти із середнім ступенем тяжкості COVID-19 становлять значну частину госпіталізованих хворих. У пацієнтів спостерігаються виражені симптоми інфекції, такі як пневмонія, лихоманка, задишка та зниження рівня кисню в крові, що потребує кисневої підтримки та постійного медичного спостереження. Хоча їхній стан не настільки критичний, як у пацієнтів із важкими формами захворювання, своєчасне й адекватне лікування необхідне для запобігання прогресуванню хвороби до важкого ступеня та розвитку ускладнень, таких як гострий респіраторний дистрес-синдром, коли виникає потреба в штучній вентиляції легень, або навіть можливої летальності. Через це зростає необхідність у нових терапевтичних підходах та етіотропних противірусних засобах, які б мали високу ефективність, хорошу переносимість і мінімальні побічні ефекти. Особливо важливими є засоби, що можуть зменшувати вірусне навантаження, сприяти швидшому одужанню і запобігати погіршенню стану пацієнтів.
Це створює необхідність у пошуку нових засобів, подібних до препарату ФЛАВОВІР® (капсули), який може доповнити існуючу базисну терапію та покращити результати лікування пацієнтів із середнім ступенем тяжкості COVID-19 [11]. У зв’язку з цим, актуальність дослідження препарату ФЛАВОВІР® (капсули), що належить до групи сучасних противірусних засобів, є надзвичайно високою. ФЛАВОВІР® (капсули) містить активні компоненти з доведеними противірусними властивостями, застосування засобу може значно покращити клінічні результати у пацієнтів з COVID-19 середнього ступеня тяжкості. Вивчення ефективності та безпеки препарату ФЛАВОВІР® (капсули) є важливим кроком у розвитку нових методів лікування коронавірусної інфекції. Завдяки своїм противірусним властивостям і потенційній здатності знижувати інтенсивність запального процесу, ФЛАВОВІР® (капсули) може бути ефективним інструментом для лікування COVID-19 середнього ступеня тяжкості. Його вивчення є важливим для розширення арсеналу препаратів, доступних для терапії коронавірусної інфекції, особливо в умовах, коли існуючі методи лікування є недостатньо ефективними або супроводжуються ризиками ускладнень.
ФЛАВОВІР® (капсули) є новою оригінальною розробкою ТОВ «НВК «Екофарм», представленою для клінічного вивчення, з метою вирішення питання про можливість лікування COVID-19 середнього ступеня тяжкості противірусним засобом прямої дії. ФЛАВОВІР® (капсули) — нова лікарська форма зареєстрованого в Україні в 2001 році і широко застосовуваного лікарського засобу ПРОТЕФЛАЗІД® (краплі). Код проведеного клінічного дослідження: EF/FLAV/C/NMAPO/05–
Досліджуваний препарат: ФЛАВОВІР®. Склад: діючі речовини — флавоноїди ПРОТЕФЛАЗІД® у вигляді ліпідних комплексів — не менше 0,16 мг на 1 капсулу; допоміжні речовини: олія соняшникова рафінована, бутилгідроксіанізол (Е 320). Склад оболонки капсули: желатин, титану діоксид (Е 171), барвник діамантовий синій FCF (E133). Лікарська форма: капсули. Основні фізико-хімічні властивості: тверді непрозорі желатинові капсули білого кольору з швом синьо-блакитного кольору. Виробник: ТОВ «НВК «Екофарм», Україна. Референтний препарат: назва: «Плацебо». Склад: діючі речовини — не містить; допоміжні речовини: олія соняшникова рафінована, бутилгідроксіанізол (Е 320). Склад оболонки капсули: желатин, титану діоксид (Е 171), барвник діамантовий синій FCF (E133). Лікарська форма: капсули. Основні фізико-хімічні властивості: тверді непрозорі желатинові капсули білого кольору з швом синьо-блакитного кольору. Виробник: ТОВ «НВК «Екофарм», Україна.
До показань для медичного призначення лікарського засобу ПРОТЕФЛАЗІД® (краплі), на основі якого створено препарат ФЛАВОВІР® (капсули), внесена нозологія: «гостра респіраторна вірусна інфекція». Діюча речовина ПРОТЕФЛАЗІД®, що входить до складу дослідного препарату ФЛАВОВІР® (капсули), має здатність пригнічувати реплікацію РНК-та ДНК-вірусів in vitro. При проведенні доклінічних досліджень виявлена інгібуюча активність діючої речовини препарату щодо вірусів грипу та гострих респіраторних вірусних інфекцій. Показано, що механізм прямої противірусної активності діючої речовини ПРОТЕФЛАЗІД® полягає в подавлені синтезу вірусоспецифічних ферментів ДНК-та РНК-полімераз, тимідинкінази, зворотної транскриптази, блокуванні нейрамінідази вірусів грипу та 3CL-протеази вірусів SARS-CoV-2. В доклінічних дослідженнях in vitro на декількох культурах клітин показана пряма противірусна активність діючої речовини препарату проти коронавірусів людини: CoV-229E (сезонний) та SARS-CoV-2 (пандемічний) зі значним пригніченням реплікації вірусів. Встановлено, що діюча речовина препарату нормалізує синтез ендогенних α-та γ-інтерферонів до фізіологічно активного рівня, підвищує неспецифічну резистентність організму до вірусної та бактеріальної інфекцій. Діючій речовині ПРОТЕФЛАЗІД® притаманна антиоксидантна дія завдяки активації транскрипційного фактору Nrf2, що сприяє захисту клітин організму від окислювального стресу та запалення, завдяки чому зменшується вірогідність виникнення гострого респіраторного дистрес-синдрому. ПРОТЕФЛАЗІД® зменшує інтоксикацію; сприяє відновленню організму після перенесеної інфекції та адаптації до несприятливих навколишніх умов. Модулює апоптоз, посилюючи дію апоптозіндукуючих факторів, а саме: активуючи каспазу 9, сприяє більш швидкій елімінації уражених вірусом клітин [11].
Мета дослідження: оцінити клінічну ефективність та переносимість препарату ФЛАВОВІР® (капсули), а саме — довести переважаючу ефективність препарату ФЛАВОВІР® (капсули) при курсових прийомах на фоні стандартної базисної терапії у пацієнтів з СOVID-19 середнього ступеня тяжкості порівняно з плацебо на фоні стандартної базисної терапії у пацієнтів з СOVID-19 середнього ступеня тяжкості.
Для досягнення мети:
- Досліджено переважаючу ефективність двох доз (кожної окремо) препарату ФЛАВОВІР® (капсули) (1 капсула та 2 капсули) порівняно з плацебо при курсовому прийомі протягом 14 діб на фоні стандартної базисної терапії при лікуванні пацієнтів з СOVID-19 середнього ступеня тяжкості.
- Оцінено переважаючу ефективність курсового прийому протягом 14 діб на фоні базисної терапії 2 (двох) капсул препарату ФЛАВОВІР® (капсули) порівняно з ефективністю курсового прийому протягом 14 діб на фоні базисної терапії 1 (однієї) капсули препарату ФЛАВОВІР® (капсули), при лікуванні пацієнтів з СOVID-19 середнього ступеня тяжкості.
- Показано переносимість препарату ФЛАВОВІР®(капсули) на фоні стандартної базисної терапії у пацієнтів з СOVID-19 середнього ступеня тяжкості порівняно з плацебо на фоні стандартної базисної терапії у пацієнтів з СOVID-19 середнього ступеня тяжкості.
- Порівняно такі параметри кожної з трьох груп учасників дослідження: -наявність/відсутність клінічних ознак захворювання до кінця 14-добового прийому досліджуваного препарату або раніше; -наявність/відсутність вірусу SARS-CoV-2 за результатами ПЛР-дослідження до кінця періоду прийому препарату або раніше; -наявність/відсутність ускладнень до кінця 19-добового періоду, який включає період прийому препарату 14 діб та період спостереження 5 діб; -кількість діб до зменшення симптомів (температура <37,0 °С, відсутність або мінімальна вираженість симптомів); -кількість діб до отримання негативного результату ПРЛ-дослідження на наявність вірусу SARS-CoV-2 в носоглотковому мазку в межах 14-добового прийому препарату; -кількість діб протягом усього періоду захворювання, протягом якого у пацієнта був хоча б один із симптомів: головний біль, лихоманка або озноб, біль в м’язах або суглобах, втома, біль у горлі, кашель, закладеність носа, вираженістю більше 1 балу; -кількість пацієнтів, у яких розвинулись серйозні ПЯ/ПР, що призводили до відміни досліджуваного лікарського засобу або препаратів стандартної базисної терапії протягом 19 діб дослідження; -кількість ПЯ/ПР та серйозних ПЯ/ПР, що виникли в період лікування (ознаки і симптоми ГРВІ в аналізі не враховувались); -кількість ПЯ/ПР та серйозних ПЯ/ПР, що виникли в період подальшого спостереження; -загальну оцінку переносимості за шкалою переносимості. Клінічно-дослідна оцінка ефективності та безпеки препарату є важливою основою для його подальшого внесення в схеми лікування пацієнтів з COVID-19. Якщо дослідження продемонструє позитивні результати, ФЛАВОВІР® (капсули) стане важливим доповненням до арсеналу засобів терапії COVID-19 середнього ступеня тяжкості, та сприятиме підвищенню якості лікування і зменшить ризик ускладнень.
Матеріали та методи.
Загальний дизайн і план-опис дослідження. Дослідження з оцінки ефективності та переносимості препарату ФЛАВОВІР® (капсули) здійснено за класичним підходом до клінічних випробувань, що включає: багатоцентровість, рандомізованість і подвійно-сліпий плацебо-контроль. Дослідження проведено в медичних центрах: КНП «Міська інфекційна лікарня» Одеської міської ради та КНП «Центральна міська лікарня» Рівненської міської ради, що забезпечило достатню вибірку пацієнтів і підвищило репрезентативність отриманих результатів. Рандомізація дозволила мінімізувати вплив сторонніх чинників та забезпечила збалансованість між групами за основними характеристиками (вік, стать, наявність супутніх захворювань тощо), що також підвищило наукову достовірність результатів. Подвійне засліплення є важливим інструментом у клінічних дослідженнях, який дозволив отримати найбільш об’єктивні результати щодо ефективності та безпеки препарату ФЛАВОВІР® (капсули), оскільки у подвійному сліпому дослідженні ані учасники, ані дослідники не знали, хто саме з пацієнтів отримує ФЛАВОВІР® (капсули), а хто – плацебо (капсули). Це усунуло можливість суб’єктивного впливу на результати з боку як пацієнтів (наприклад, у вигляді ефекту плацебо), так і медичного персоналу (упередженість або психологічний вплив під час оцінки стану пацієнтів). Як зазначено, в якості референтного препарату лікування використано препарат плацебо. Дослідники набирали групи пацієнтів у співвідношенні 1:1:1. Пацієнти знаходились під стаціонарним наглядом. Після підписання форми інформованої згоди кожного пацієнта лікар-дослідник включав в дослідження. Після проходження процедур скринінгу, на підставі критеріїв включення/невключення, дослідник приймав рішення про можливість продовження участі кожного пацієнта в даному дослідженні. Дослідження складалося із трьох періодів: період скринінгу (до 48 годин), період лікування (14 діб) та період спостереження (5 діб). Дослідження тривало зазначений період часу, протягом якого дослідники регулярно відстежували стан пацієнтів (клінічні показники, вірусне навантаження, побічні ефекти тощо). Тривалість лікування та спостереження зумовлена особливостями перебігу хвороби та критеріями дослідження.
Основні кінцеві точки дослідження. Ефективність: первинні кінцеві точки включали швидкість одужання, тривалість симптомів та зниження вірусного навантаження. Переносимість і безпека: кількість і характер побічних ефектів, а також будь-які серйозні небажані явища.
Опис вибору пацієнтів, критерії включення/виключення. Вибір пацієнтів для участі в клінічному дослідженні препарату ФЛАВОВІР® (капсули) здійснено на основі чітко визначених критеріїв, що гарантували репрезентативність вибірки і підвищували достовірність результатів. Учасники дослідження відповідали критеріям включення та виключення, які гарантують безпеку дослідження та дозволяють оцінити ефективність препарату у конкретній групі пацієнтів із середнім ступенем тяжкості COVID-19. Плановане число учасників дослідження — 162, розподілених в 3 групи у співвідношенні 1:1:1. Досліджувана популяція: особи обох статей віком від 18 років до 65 років (включно), які знаходяться на стаціонарному лікуванні з встановленим та підтвердженим (вірусологічно, методом ПЛР) діагнозом «СOVID-19 — гостра респіраторна вірусна інфекція середнього ступеня тяжкості». Критерії включення (вимоги до пацієнтів, які можуть брати участь у дослідженні): вік — пацієнти віком від 18 до 65 років; діагноз: підтверджений позитивний результат тестування на SARS-CoV-2 за допомогою ПЛР або іншого надійного методу діагностики. Стан захворювання: середній ступінь тяжкості COVID-19, що характеризується: наявністю симптомів пневмонії (лихоманка, кашель, утруднення та прискорення дихання); сатурацією кисню (SpO2) на рівні 92% і вище без необхідності штучної вентиляції легень або інтенсивної терапії. Критерії виключення (пацієнти, які не можуть брати участь у дослідженні): тяжкий або критичний перебіг COVID-19 (пацієнти з необхідністю інвазивної штучної вентиляції легень або перебування в палаті інтенсивної терапії). Вагітність або годування груддю: через недостатню кількість даних про безпеку препарату ФЛАВОВІР® (капсули) в цих групах. Наявність важких супутніх захворювань, таких як декомпенсовані захворювання серцево-судинної системи; тяжка печінкова або ниркова недостатність; активні онкологічні захворювання. Алергія або гіперчутливість до компонентів препарату ФЛАВОВІР® (капсули) або інших лікарських засобів, що використовуються у дослідженні. Відмова пацієнта від участі у дослідженні. Участь в інших клінічних дослідженнях за останні 30 днів, що може вплинути на результати цього дослідження. Імуносупресивна терапія або інші захворювання імунної системи, які можуть вплинути на реакцію організму на лікування.
Клінічна схема призначення досліджуваних препаратів. Група I (основна, n=54) — учасники дослідження цієї групи отримували препарат ФЛАВОВІР® (капсули), перорально по 1 капсулі 2 рази на добу та плацебо по 1 капсулі 2 рази на добу протягом 14 діб на фоні стандартної базисної терапії під контролем ПЛР. Група IІ (основна, n=54) — учасники дослідження цієї групи отримували препарат ФЛАВОВІР® (капсули), перорально по 2 капсули 2 рази на добу протягом 14 діб на фоні стандартної базисної терапії під контролем ПЛР. Група IIІ (контрольна, n=54) — учасники дослідження цієї групи отримували препарат плацебо (капсули), перорально по 2 капсули 2 рази на добу протягом 14 діб на фоні стандартної базисної терапії під контролем ПЛР. Лікування могло бути припинено достроково у разі відсутності лихоманки та покращення стану пацієнта протягом 3-х діб поспіль, що супроводжувалося негативним результатом ПЛР-тесту. Стандартна базисна терапія включала: антикоагулянтні препарати (низькомолекулярні гепарини, якщо це не протипо- казано); інфузійну та жарознижувальну терапію; при необхідності — антибактеріальні та протигрибкові засоби (відповідно до показань, особливостей перебігу захворювання) тощо. У процесі дослідження пацієнти отримували симптоматичну терапію (відхаркувальні препарати, засоби для полоскання горла тощо). Допускалося застосування лікарських засобів, що постійно використовуються пацієнтом для лікування супутніх захворювань. Супутнє лікування: у процесі дослідження не дозволялось призначення: -противірусних препаратів; – імунних сироваток та імуноглобулінів; -вакцин; -імуностимуляторів; -імуносупресорів; індукторів інтерферону. Заборонялось застосування медикаментів, що зрошують носоглотку або ротоглотку, і препаратів для розсмоктування в роті протягом 3-х годин перед процедурою взяття мазка зі слизової носоглотки. Інформацію про препарати, використані для супутньої терапії записували, включаючи назву, дозу, спосіб прийому, частоту прийому, дати початку і закінчення терапії в історію хвороби/амбулаторну карту та індивідуальну реєстраційну форму кожного хворого пацієнта.
Досліджувані показники: визначення наявності вірусу SARS-CoV-2 за результатами ПЛР-аналізу в носоглоткових мазках в період скринінгу та на 14-у добу лікування в період прийому препарату або раніше; основні параметри життєдіяльності (АТ, ЧДР, ЧСС, насичення крові киснем); -загальний аналіз крові (еритроцити, гемоглобін, тромбоцити, лейкоцити, лейкоцитарна формула, в період скринінгу, на 7-у та після 14-ї доби періоду прийому препарату; -загальний аналіз сечі (питома вага, рН, білок, глюкоза, лейкоцити, епітеліальні клітини, еритроцити, циліндри); в період скринінгу, на 7-у та після 14-ї доби періоду прийому препарату; -біохімічний аналіз крові (АЛТ, АСТ, креатинін, глюкоза, лужна фосфатаза, загальний білірубін, сечовина); в період скринінгу, на 7-у та після 14-ї доби періоду прийому препарату; -аналіз крові на вміст інтерлейкіну-6, феритину, димеру та СРБ (у кожного третього рандомізованого пацієнта всіх груп) на скринінгу, на 4-у, 7-у, 11-у та після 14-тої доби періоду прийому препарату; -інструментальне дослідження ОГК до лікування (доба 0) та після 14-ї доби періоду прийому препарату; ЕКГ в 12-ти відведеннях на скринінгу, на 7-у та після 14-ї доби періоду прийому препарату.
Змінні ефективності. Первинні кінцеві точки ефективності: -час (у добах) до настання події, що характеризується відсутністю гіпертермії (протягом не менш ніж 3-х діб при відсутності або мінімальній вираженості симптомів ГРВІ ≤1 бала за вербальною аналоговою шкалою: 0–3 бали) в межах 14-добового періоду прийому препарату; час (у добах) до моменту відсутності вірусу SARS-CoV-2 в носоглотковому мазку в межах 14-добового періоду прийому препарату.
Первинні змінні ефективності. Первинні кінцеві точки ефективності трансформуються в такі первинні змінні ефективності: -час (у добах) до настання події, що характеризується відсутністю гіпертермії (<37,0 °С) протягом не менш ніж 3-х діб при відсутності або мінімальній вираженості симптомів ГРВІ ≤1 бала за вербальною аналоговою шкалою: 0–3 бали) в межах 14-добового періоду прийому препарату; – час (у добах) до моменту відсутності вірусу SARS-CoV-2 в носоглотковому мазку в межах 14-добового періоду прийому препарату.
Вторинні кінцеві точки ефективності: -частка пацієнтів у групах, для яких були виконані такі умови: зникнення/зниження тяжкості клінічних ознак захворювання до кінця 14-добового прийому досліджуваного препарату або раніше та/або елімінація вірусу SARS-CoV-2 за результатами ПЛР-дослідження до кінця 14-добового прийому досліджуваного препарату або раніш; -час (у добах) до збільшення сатурації киснем крові на 3% і вище; -частка пацієнтів у групах з випадками розвитку ускладнень за період даного клінічного випробування (19 діб=14 діб прийому препарату + 5 діб спостереження); -час (у добах) до настання мінімальної вираженості симптомів ГРВІ ≤1 бала за вербальною аналоговою шкалою: 0–3 бали); -динаміка вираженості симптомів ГРВІ; -динаміка інтерлейкіну-6, феритину, С-реактивного білка та Д-димеру. Вторинні кінцеві точки ефективності трансформуються у такі вторинні змінні ефективності: -ефективність терапії (терапія ефективна/терапія неефективна), що оцінюється за такою дихотомічною шкалою: терапія ефективна, виконані такі умови: зникнення/зниження тяжкості клінічних ознак захворювання до кінця 14-добового прийому досліджуваного препарату або раніше та/або елімінація вірусу SARS-CoV-2 за результатами ПЛР-дослідження до кінця 14-добового прийому досліджуваного препарату або раніше. Терапія неефективна. Виконані такі умови: наявність клінічних ознак захворювання з більшою вираженістю симптомів, ніж на момент включення в дослідження після закінчення 14-добового курсу прийому препарату або прослідковується наявність вірусів SARS-CoV-2 за результатами
ПЛР-дослідження за підсумками 14-добового прийому ліків. Час (у добах) до збільшення сатурації киснем крові на 3% і вище; -дихотомічна змінна з категоріями «наявність»/«відсутність» у пацієнта випадку розвитку ускладнень за період даного клінічного випробування (19 діб= 14 діб прийому препарату + 5 діб спостереження); час (у добах) до настання мінімальної вираженості симптомів ГРВІ ≤1 бала за вербальною аналоговою шкалою: 0–3 бали), а саме: 0 балів — без ознак; 1 бал —мінімальна вираженість ознак; 2 бали — середня вираженість ознак; 3 бали — значна вираженість ознак; динаміка вираженості симптомів ГРВІ; -динаміка інтерлейкіну-6, феритину, С-реактивного білка та Д-димеру. Дотримання вимог Клінічне дослідження проведено відповідно до Закону України «Про лікарські засоби», за затвердженим Протоколом дослідження з дотриманням принципів Належної клінічної практики (GCP), у відповідності до Керівництва СТ-Н МОЗУ 42-7.0: 2008 «Лікарські засоби. Належна клінічна практика», з етичними принципами Гельсінської Декларації, діючими нормативними вимогами (Порядок проведення клінічних випробувань лікарських засобів та експертизи матеріалів клінічних випробувань і Типове положення про Комісії з питань етики», затвердженим Наказом МОЗ України № 690 від 23.09.2009 зі змінами).
Результати і обговорення.
Для зручності аналізу результати дослідження статистично опрацьовані та оформлені графічно (рис. 1–16) та у вигляді табличного матеріалу (табл. 1–11). Для головних змінних побудовано криві виживаності за методом Каплана-Мейєра та оцінено медіану виживаності та 95% довірчих інтервалів для неї в кожній групі.
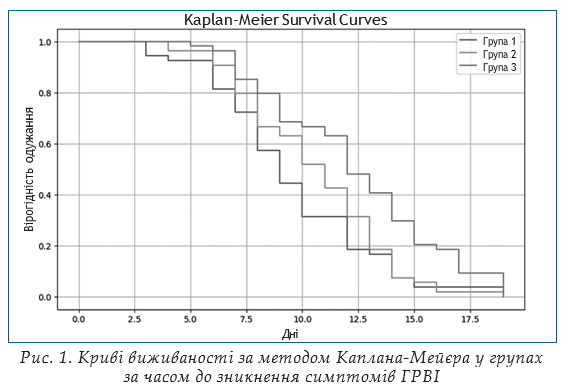
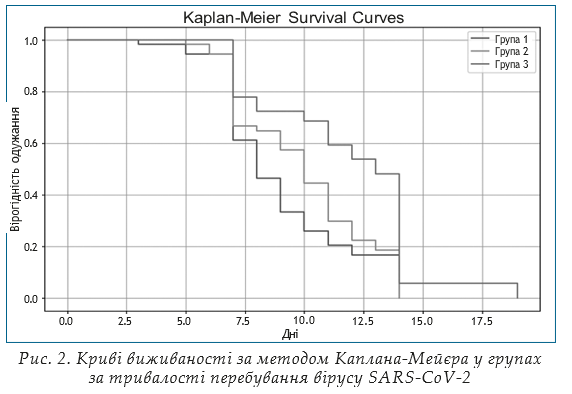
Статистичне порівняння за головними змінними ефективності виконано шляхом порівняння кривих виживаності за допомогою логрангового критерію (табл. 1).
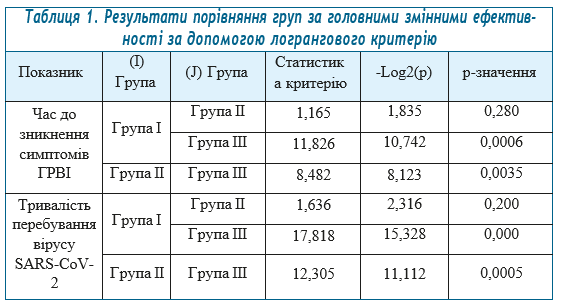
З наведених результатів видно, що групи І та ІІІ, ІІ та ІІІ статистично значущо відрізняються за основними критеріями ефективності. Таким чином, протягом усього часу (або значної частини) перша та друга групи мають більш високу ймовірність одужання, ніж група ІІІ.
Для інтерпретації результатів, згідно з даними оцінки вираженості суб’єктивних симптомів, за підсумками 14-добового прийому ліків, створена категоріальна змінна з категоріями: «вираженість симптомів захворювання після курсу лікування становить ≤1 бала» та «вираженість симптомів захворювання після курсу лікування становить >1 бала». Розподіл пацієнтів основних та контрольної груп за цією змінною представлений в табл. 2.
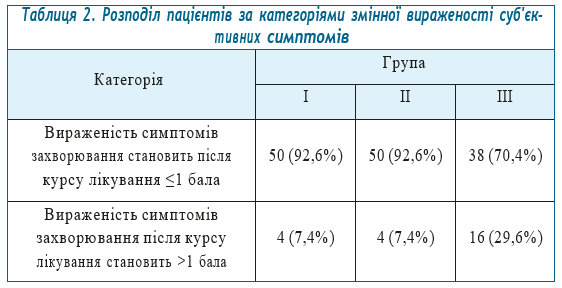
Для інтерпретації результатів, відповідно до одержаних результатів ПЛР-дослідження, за підсумками 14-добового прийому ліків створена категоріальна змінна з категоріями: «елімінація вірусів SARS-CoV-2» та «наявність вірусів SARS-CoV-2». Розподіл пацієнтів основних та контрольної груп за цією змінною представлений в табл. 3.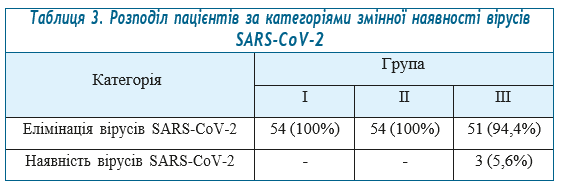
Оцінено різницю часток позитивних результатів (категорія, що відповідає ефективності лікування) та побудовані для неї 95% довірчі інтервали. Дані про розподіл в групах пацієнтів за змінною ефективності лікування представлені в табл. 4.
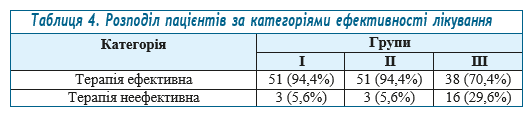
Порівняння груп за ефективністю лікування виконано за допомогою точного критерію Фішера (табл. 5).
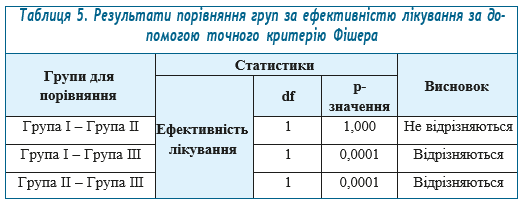
Оцінка вторинної змінної: час (у добах) до збільшення сатурації киснем крові 3% і вище. В кожній групі розраховано час (у добах), який знадобився до збільшення сатурації киснем крові на 3% і вище (табл. 6).
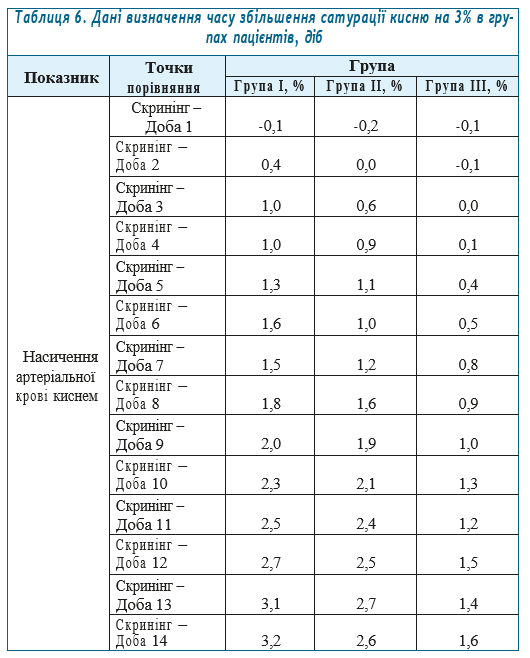
Збільшення середньої сатурації кисню крові на 3% і вище було зафіксовано у групі I на 13 добу. В інших групах збільшення сатурації кисню крові на 3% і вище не було зафіксовано за 14 діб терапії.
Оцінка вторинної змінної: наявність/відсутність у пацієнта випадків ускладнень за період даного клінічного випробування. У відповідності до протоколу, під час дослідження виконано оцінку наявності ускладнень вірусної інфекції. В групі І було виявлено 14 ускладнень у 11 хворих, в групі ІІ виявлено 12 ускладнень у 9 хворих, в групі ІІІ виявлено 30 ускладнень у 23 хворих. Дані щодо характеру і кількості ускладнень наведено в табл.7.
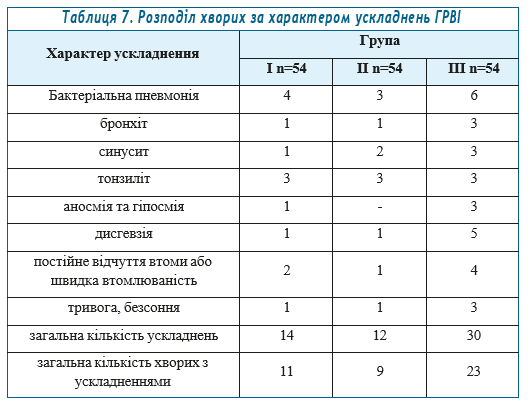
Таким чином, доля хворих з наявністю ускладнень ГРВІ після закінчення періоду спостереження в групі ІІІ була значно вищою порівняно з групами І та ІІ.
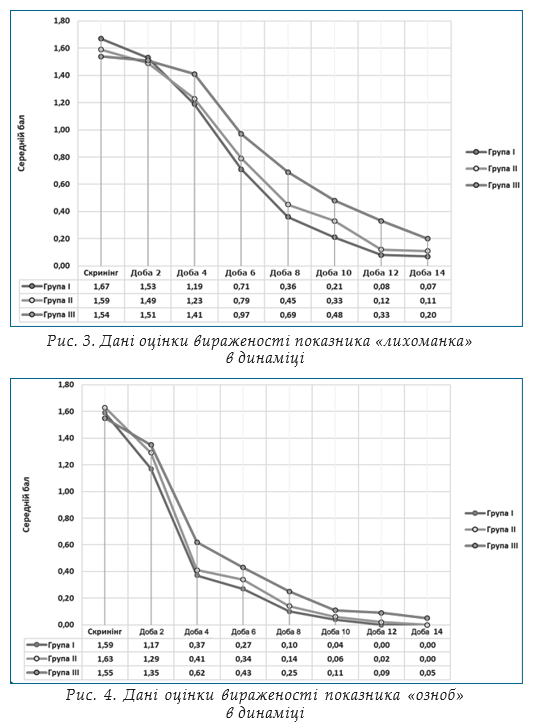
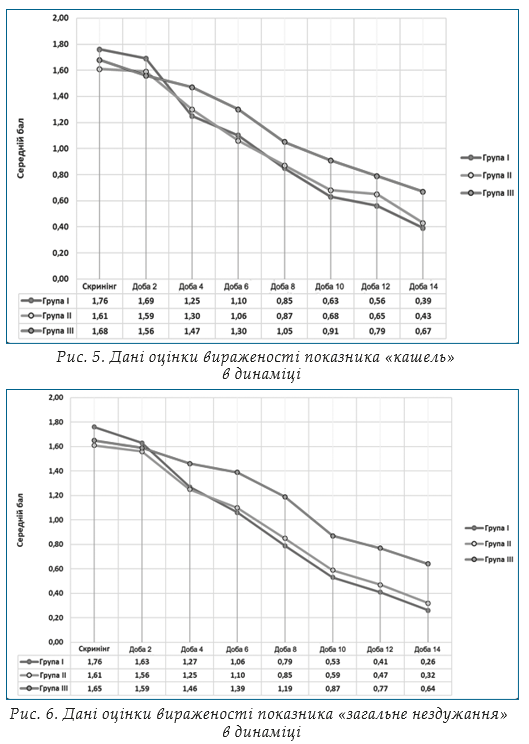
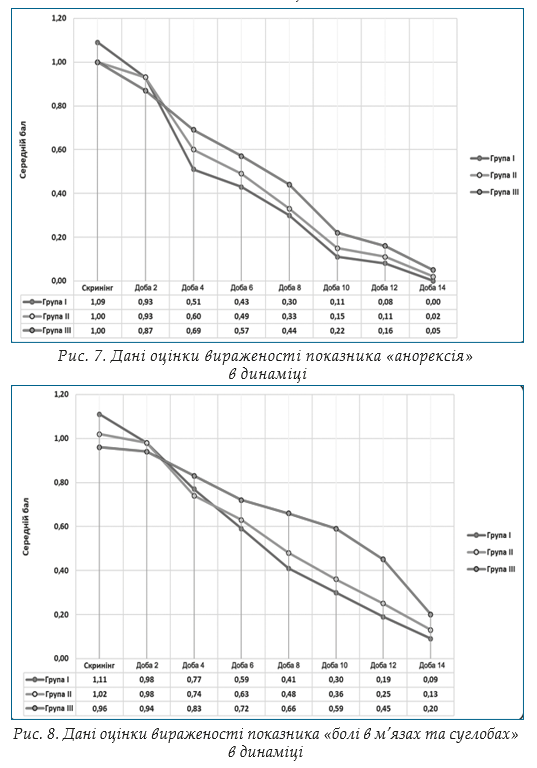
Оцінка вторинної змінної: динаміка вираженості симптомів ГРВІ. Відповідно до протоколу клінічного дослідження протягом 14 діб терапії оцінювали вираженість суб’єктивних симптомів захворювання, а саме: лихоманка, озноб, кашель, загальне нездужання (слабкість), анорексія, болі в м’язах та суглобах, задишка, головний біль, першіння, біль в горлі, закладеність носу, виділення з носу. Оцінку проводили за 4-бальною вербальною аналоговою шкалою. Результати аналізу однорідності груп за даними оцінки вираженості суб’єктивних скарг хворого в динаміці методами описової статистики наведено на рис. 3–12.
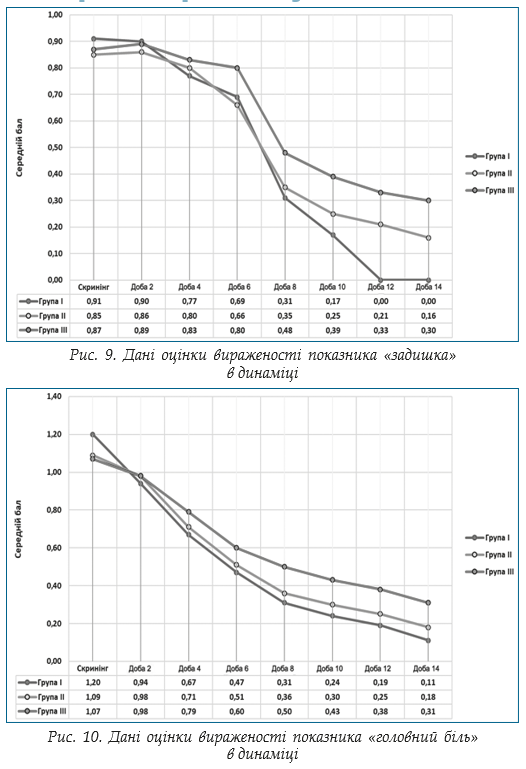
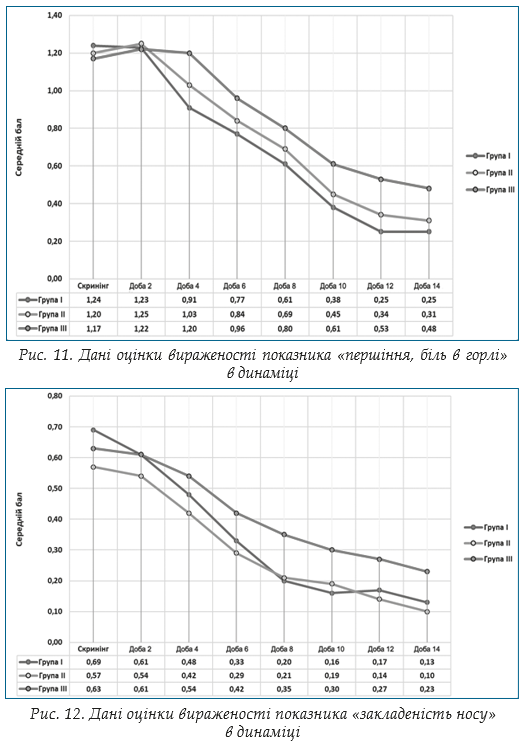
Оцінка вторинної змінної: час (у добах) до настання мінімальної вираженості симптомів ГРВІ ≤1 бала за вербальною аналоговою шкалою: 0–3. В кожній групі розраховано час (у добах), який знадобився до настання мінімальної вираженості симптомів ГРВІ ≤1 бала за вербальною аналоговою шкалою: 0–3 (табл. 8).
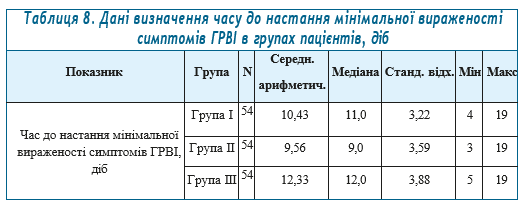
Для оцінки відмінності груп в часі до настання мінімальної вираженості симптомів ГРВІ виконано однофакторний дисперсійний аналіз (табл. 9) з подальшим застосуванням апостеріорного критерію множинних порівнянь Тьюкі (табл. 10).
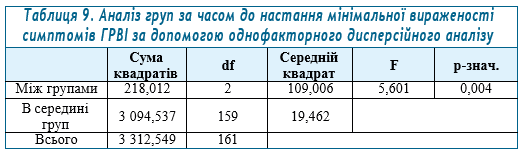
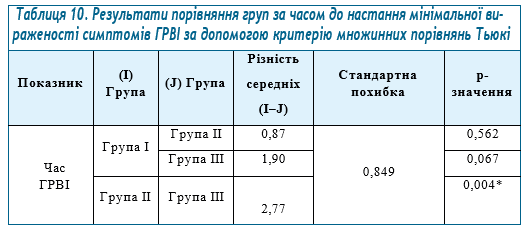
Як видно з наведеної таблиці, між групами ІІ та ІІІ присутні статистично значущі відмінності за часом до настання мінімальної вираженості симптомів ГРВІ.
Заслуговують на увагу зміни біохімічних показників крові у процесі дослідної терапії, які представлено в таблицях 11–14.
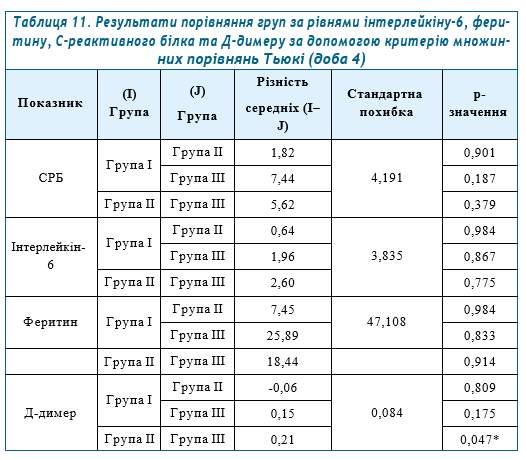
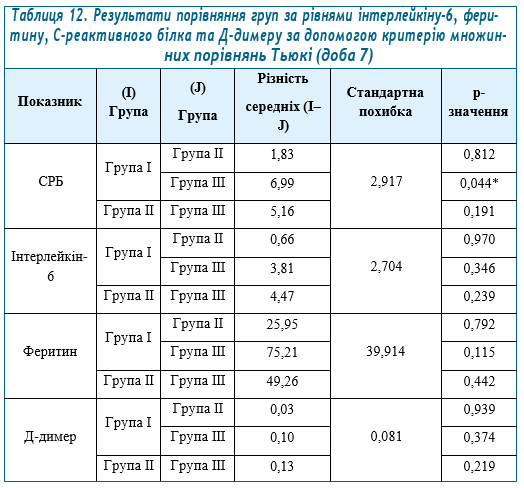
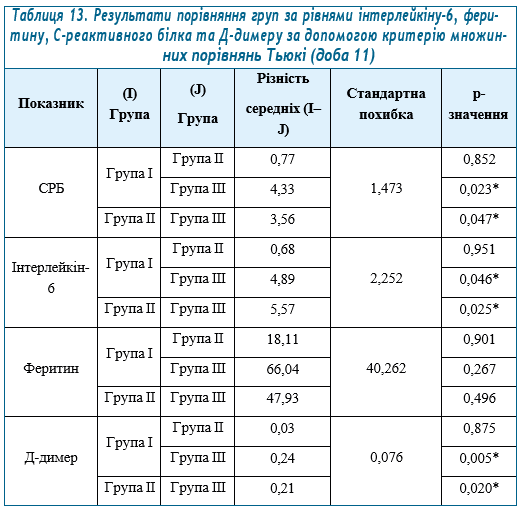
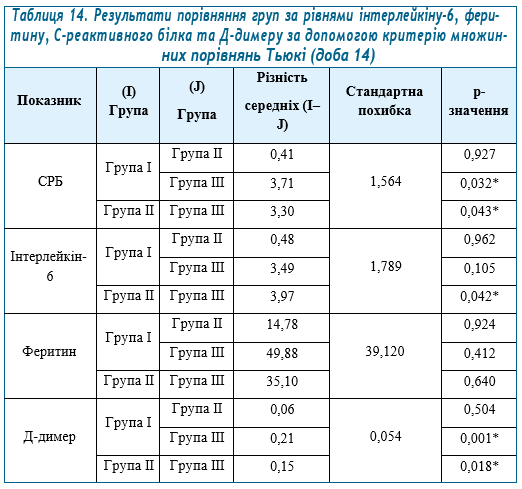
Як видно з проведеного аналізу, трапляються статистичні відмінності* між групами за динамікою рівнів інтерлейкіну-6, феритину, С-реактивного білка та Д-димеру в таких випадках: С-реактивний білок: між групами І та ІІІ на 7-у добу; між групами І та ІІІ, ІІ та ІІІ на 11-у та 14-у доби. Інтерлейкін-6: між групами І та ІІІ, ІІ та ІІІ на 11-у добу; між групами ІІ та ІІІ на 14-у добу. Феритин: не було виявлено статистично значущих відмінностей. Д-димер: між групами ІІ та ІІІ на 4-у добу; між групами І та ІІІ, ІІ та ІІІ на 11-у та 14-у доби.
Визначення сатурації артеріальної крові киснем в динаміці. Оцінку насичення артеріальної крові киснем виконували щоденно протягом всього періоду терапії за допомогою портативного пульсоксиметру. Дані визначення сатурації кисню представлено графічно в динаміці сатурації артеріальної крові киснем в групах пацієнтів на рис. 13
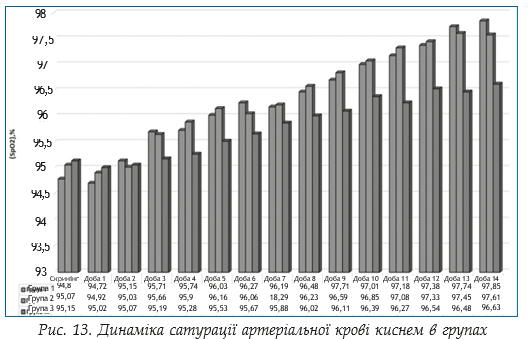
Динаміку змін частоти дихальних рухів та частоти серцевих скорочень в групах демонструють рисунки 13 та 14.
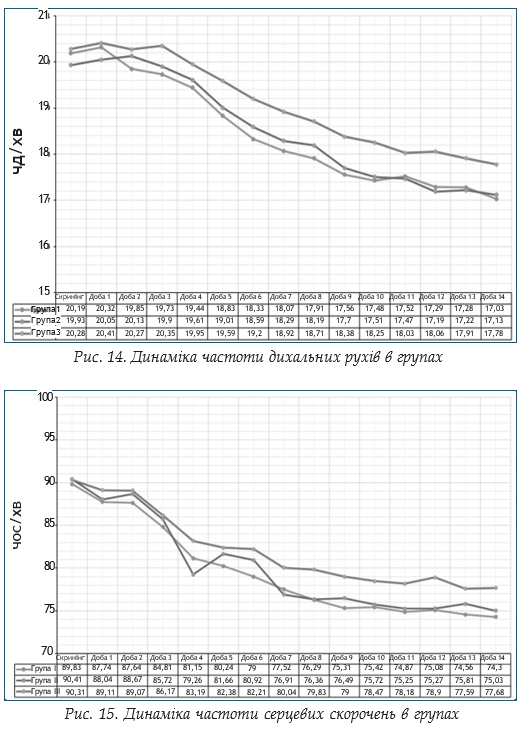
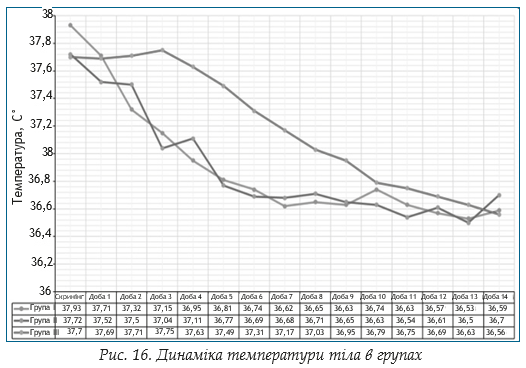
Визначення температури тіла в динаміці. Оцінку температури тіла виконували щоденно протягом всього періоду терапії. Дані визначення температури тіла в групах пацієнтів в динаміці представлено на рис. 16. Привертає увагу зниження температури тіла в групі І та в групі ІІ вже на 5 добу лікування.
Важливий момент клінічного дослідження — оцінка переносимості лікування в групах. Згідно з Протоколом випробування, після завершення періоду спостереження здійснено оцінку загальної переносимості для кожного пацієнта за категоріальною шкалою.
З огляду на відсутність суб’єктивних скарг з боку пацієнтів і негативних змін при об’єктивному і лабораторному обстеженнях, переносимість лікування у більшості пацієнтів трьох груп була розцінена як «хороша». Ґрунтуючись на результатах аналізу зроблено заключення, що групи пацієнтів значуще не відрізнялися за показником загальної переносимості.
Висновки.
- За результатами дослідження, лікування визнано ефективним у 94,4% пацієнтів групи І, у 94,4% пацієнтів групи ІІ та у 70,4% у пацієнтів групи ІІІ. Не виявлено статистично значущої різниці в ефективності лікування за первинною змінною між групами І та ІІ. Між групами І і ІІІ та групами ІІ і ІІІ виявлено статистично значущу відмінність.
- На підставі даних проведеного дослідження доведено гіпотезу про переважаючу ефективність двох доз препарату ФЛАВОВІР® (капсули) порівняно з плацебо на фоні стандартної базисної терапії у пацієнтів з СOVID19 середнього ступеня тяжкості.
- Середня тривалість симптомів ГРВІ в досліджуваних групах склала: в групі І — 10,43 доби, в групі ІІ — 9,56 доби, в групі ІІІ — 12,33 доби. Отже, на фоні прийому препарату ФЛАВОВІР® (капсули) термін маніфестації клінічних симптомів ГРВІ порівняно з плацебо, скорочується. Між групами І та ІІІ присутні статистично значущі відмінності за часом до настання мінімальної вираженості симптомів ГРВІ.
- Термін перебування вірусів SARS-CoV-2 в організмі хворих від початку лікування, за даними ПЛР, склав: в групі І — 9,96 доби; в групі ІІ — 9,06 доби; в групі ІІІ — 11,80 доби. Отже, на фоні застосування препарату ФЛАВОВІР® (капсули) скорочується термін перебування вірусів SARS-CoV-2 порівняно з плацебо.
- Відповідно до протоколу, в процесі дослідження виконано оцінку наявності ускладнень вірусної інфекції. В групі І було виявлено 14 ускладнень у 11 хворих (6,7% від загальної кількості хворих), в групі ІІ виявлено12 ускладнень у 9 хворих (5,5% від загальної кількості хворих), в групі ІІІ виявлено 30 ускладнень у 23 хворих (14,1% від загальної кількості хворих). Отже, доля хворих з наявністю ускладнень ГРВІ після закінчення періоду спостереження в групі ІІІ була значно вищою порівняно з групами І і ІІ.
- В групах досліджуваних вивчали показники інтерлейкіну-6, феритину, С-реактивного білка та Д-димеру в динаміці. Виявлено статистичні відмінності між групами за динамікою рівнів інтерлейкіну-6, феритину, С-реактивного білка та Д-димеру в таких випадках: а) С-реактивний білок: між групами І та ІІІ на 7-у добу; між групами І та ІІІ, ІІ та ІІІ на 11-у добу та 14-у добу; б) Інтерлейкін-6: між групами І та ІІІ, ІІ та ІІІ на 11-у добу; між групами ІІ та ІІІ на 14-у добу; в) Феритин: не було виявлено статистично значущих відміннос- тей; г) Д-димер: між групами ІІ та ІІІ на 4-у добу; між групами І та ІІІ, ІІ та ІІІ на 11-у та 14-у добу.
- Протягом дослідження не зареєстровано серйозних побічних реакцій або побічних явищ. Виявлено декілька випадків у змінах лабораторних показників у вигляді підвищення активності рівня амінотрансферази (7), підвищення кількості тромбоцитів (3) та лейкоцитів (5), підвищення активності лужної фосфатази (1), які не спостерігалися при повторному проведенні обстеження. За показником загальної переносимості групи пацієнтів значуще не відрізнялися.
Отже, препарат ФЛАВОВІР® (капсули) має високий потенціал як етіотропний противірусний засіб у лікуванні хворих на COVID-19 середнього ступеня тяжкості, потребує, на наш погляд, подальшого дослідження з метою державної реєстрації в Україні в якості лікарського засобу.
Література
- World Health Organization (WHO). (2021). COVID-19 Clinical Management: Living Guidance. https://www.who.int/publications/i/item/WHO-2019-nCoV-clinical-2021-2.
- Paltiel A. D., Zheng A. & Zheng A. Assessment of SARS-CoV-2 Testing in the United States. JAMA Internal Medicine. 2020;180(12):620–1624. DOI:10.1001/jamainternmed.2020.4978.
- Mahmud R. & Tarek A. A review of treatment options for COVID-19: Efficacy and safety. Journal of Medical Virology. 2022;94(2):574–586. DOI:10.1002/jmv.27679.
- Національна служба здоров’я України (НСЗУ). (2020). Протокол лікування COVID-19. https://nszu.gov.ua.
- Міністерство охорони здоров’я України. (2021). Наказ № 762 від 02.04.2020 року (із змінами). Про затвердження клінічних протоколів для лікування COVID-19. https://zakon.rada.gov.ua/rada/show/v2495282-21#Text.
- Centers for Disease Control and Prevention (CDC). (2022). Clinical Guidance for Management of Patients with Confirmed COVID-19. https://iris.who.int/bitstream/handle/10665/362783/WHO-2019-nCoV-Clinical-2022.2-eng.pdf.
- European Medicines Agency (EMA). (2021). Evaluation of Medicines for Human Use: Guidance on the clinical development of medicines for COVID-19. https://www.ema.europa.eu/en/human-regulatory-overview/public-health-threats/coronavirus-disease-covid-19/covid-19-public-health-emergency-international-concern-2020-23/guidance-medicine-developers-other-stakeholders-covid-19/covid-19-guidance-evaluation-marketing-authorisation.
- World Health Organization (WHO). (2022). Therapeutics and COVID-19: living guideline. https://iris.who.int/handle/10665/353403.
- Vegivinti CТR, Evanson KW, Lyons H, Akosman I, Barrett A, Hardy N & Touchette J. Efficacy of antiviral therapies for COVID-19: a systematic review of randomized controlled trials. BMC Infect Dis. 2022;22:107. DOI:10.1186/s12879-022-07068-0.
- Akaberi D, Båhlström A, Chinthakindi PK, Nyman Т, Sandström А, Järhult JD, Palanisamy N, Lundkvist А, Lennerstrand J. Targeting the NS2B-NS3 protease of tick-borne encephalitis virus with pan-flaviviral protease inhibitors. Antiviral Research. 190, 105074. DOI:10.1016/j.antiviral.2021.105074.
- Zhou F., Yu T. & Du R. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. The Lancet. 2020;395(10229):1054–1062. DOI:10.1016/S0140-6736(20)30566-3.
- Гриневич О. Й. (ред.). ПРОТЕФЛАЗІД®: клінічний досвід. – Київ: 2024. – с.75–103.
Відомості про автора:
Чабан Т. В. — д. мед. н., професор, завідувачка кафедрою інфекційних хвороб Одеського НМУ, лікар-інфекціоніст вищої кваліфікаційної категорії, м. Одеса,
e-mail: ttch153@gmail.com, ORCID 0000-0001-6989-5816.
Харитонюк Р. О. — к. мед. н., лікар-інфекціоніст вищої кваліфікаційної категорії, заступник медичного директора, КНП «ЦМЛ» РМР, м. Рівне.
e-mail: rayaharitonyuk@ukr.net.
Гриневич О. Й. — д. мед. н., Заслужений діяч науки і техніки України, лауреат премії КМ України, заступник генерального директора ТОВ «НВК «Екофарм», м. Київ.
e-mail: o.hrynevych@ecopharm.ua, ORCID 0000-0001-6542-8102.
Бочаров В. М. — к. мед. н., асистент кафедри інфекційних хвороб Одеського НМУ, лікар-інфекціоніст вищої кваліфікаційної категорії, м. Одеса.
e-mail: slavun.dessa@gmail.com, ORCID 0000-0003-0668-694Х.
Максимчук Г. В. — лікар-інфекціоніст вищої кваліфікаційної категорії, завідувачка інфекційного відділення КНП «ЦМЛ» РМР, м. Рівне.
e-mail: galinamaksimcuk7@gmail.com.
Золотухіна Ю. О. — лікар, керівник групи клінічних випробовувань ТОВ «НВК «Екофарм», м. Київ,
E-mail: zolotukhina@ecopharm.ua, ORCID 0000-0002-0451-0601.
Information about the authors:
Chaban T. V. — Doctor of Medical Sciences, Professor, Head of the Department of Infectious Diseases of the Odessa National Medical University, infectious disease specialist of the highest qualification category, Odessa.
e-mail: ttch153@gmail.com ORCID 0000-0001-6989-5816
Kharytonyuk R. O. — Candidate of Medical Sciences, infectious disease specialist of the highest qualification category, Deputy Medical Director, KNP “CML” RMR, Rivne.
e-mail: rayaharitonyuk@ukr.net.
Hrynevych O.Y. — Doctor of Medical Sciences, Honored Worker of Science and Technology of Ukraine, laureate of the Prime Minister of Ukraine Prize, Deputy General Director of LLC “NVK “Ecopharm”, Kyiv.
e-mail: o.hrynevych@ecopharm.ua ORCID 0000-0001-6542-8102
Bocharov V. M. — Candidate of Medical Sciences, Assistant of the Department of Infectious Diseases of the Odessa National Medical University, Infectious Diseases Physician of the Highest Qualification Category, Odessa.
e-mail: slavun.dessa@gmail.com ORCID 0000-0003-0668-694Х
Maksymchuk G. V. — Infectious Diseases Physician of the Highest Qualification Category, Head of the Infectious Diseases Department of the Clinical Research Center “CML” of the RMR, Rivne.
e-mail: galinamaksimcuk7@gmail.com
Zolotukhina Yu. O. — IPhysician, Head of the Clinical Trials Group of LLC “NVK “Ecopharm”, Kyiv.
E-mail: zolotukhina@ecopharm.ua ORCID 0000-0002-0451-0601
