Застосування азоксимера броміду в комплексній терапії лайм-бореліозу

УДК 616.995.42+616.8+616-07-085
DOI : https://doi.org/10.61948/prevmed-2024-2-21
В. Ю. Клюс, П. А. Дьяченко
ДУ «Інститут епідеміології та інфекційних хвороб ім. Л. В. Громашевського НАМН України», Київ
В роботі вивчено поліморфізм клінічних проявів Лайм-бореліозу (ЛБ) при застосуванні препарату азоксимера броміду в комплексній терапії для лікування цього захворювання.
Мета — вивчити клінічні особливості перебігу Лайм-бореліозу у хворих при застосуванні препарату азоксимера броміду.
Матеріали і методи. Обстежено 72 хворих на Лайм-бореліоз. Вік хворих складав 37,5±2,5 року. Проводилась оцінка неврологічного статусу, магнітно–резонансна томографія головного та спинного мозку, офтальмоскопія, електронейроміографія, комплексна імунограма. Серологічна діагностика ЛБ була основана на дослідженні сироватки крові на антитіла IgM та IgG до борелій за допомогою імуноферментного аналізу і\ або імуноблоту.
Результати та їх обговорення. Всі хворі з ураженням нервової системи були розподілені на 2 дослідних групи: Пацієнти 1-ої групи (група А) отримували етіотропну (цефтриаксон, метронідазол у середньотерапевтичних дозах), патогенетичну (нейропротекція, протизапальні, протинабрякові препарати тощо) терапію та азоксимера бромід.
Пацієнтів 2-ої групи (група В) лікували цефтриаксоном внутрішньовенно в середньо терапевтичних дозах.
Застосування препарату показало: збільшення функціональної активності ефекторних клітин імунної системи, зниження вираженості аутоімунних реакцій та скорочення терміну перебування хворого у стаціонарі на 3,5±1,2 дня, водночас відзначалася його висока етіологічна ефективність і відсутність ускладнень при застосуванні, що підтверджує доцільність застосування його в комплексній терапії ЛБ.
Ключові слова: системний кліщовий бореліоз, Лайм-бореліоз (ЛБ), азоксимера бромід, лікування, терапія.
Yu. Klyus, P. A. Dyachenko
THE USE OF AZOXIMER BROMIDE IN COMPLEX THERAPY OF LYME BORRELIOSIS
SI “L. V. Hromashevskyi Institute of Epidemiology and Infectious Diseases of NAMS of Ukraine”, Kyiv
Azoximer bromide in complex therapy for the treatment of this disease is studied.
The goal is to study the clinical features of the course of Lyme borreliosis in patients with the use of the drug azoximer bromide.
Materials and methods. 72 patients with Lyme borreliosis were examined, the age of the patients was 37.5±2.5 years. An assessment of the neurological status, magnetic resonance imaging of the brain and spinal cord, ophthalmoscopy, electroneuromyography, and a complex immunogram were performed. Serological diagnosis of LB was based on the examination of blood serum for IgM and IgG antibodies to Borrelia using enzyme immunoassay and/or immunoblot
Results and their discussion. All patients with damage to the nervous system were divided into 2 experimental groups:
Patients of the 1st group — (group A) received etiotropic (ceftriaxone, metronidazole in medium therapeutic doses), pathogenetic (neuroprotection, anti-inflammatory, anti-edema drugs, etc.) therapy and azoximer bromide.
Patients of the 2nd group — (group B) were treated with a combination of ceftriaxone intravenously in medium therapeutic doses.
The use of the drug showed: an increase in the functional activity of effector cells of the immune system, a decrease in the severity of autoimmune reactions and a reduction in the patient’s stay in the hospital by 3.5±1.2 days, while its high etiological efficiency and the absence of complications during use were noted, which confirms the feasibility of use his in the complex therapy of LB.
Key words: systemic tick-borne borreliosis, Lyme borreliosis (LB), azoximer bromide, treatment, therapy.
Лайм-бореліоз — (іксодовий кліщовий бореліоз, хвороба Лайма, ЛБ) — інфекційне поліорганне природно-вогнищеве трансмісивне захворювання, збудником якого є спірохета комплексу Borrelia burgdorferi sensu lato, що проявляється ураженням шкіри, опорно-рухового апарату, нервової та серцево-судинної систем, печінки, очей [1, 2, 3].
Переносниками ЛБ є іксодові кліщі. Їх спонтанна інфікованість бореліями в природних вогнищах становить 10–70%, змішаної інфекції з вірусом кліщового енцефаліту — до 15%. Від 7–9% до 24–50% кліщів у ендемічних вогнищах можуть бути інфіковані одночасно двома або трьома різними бореліями [11, 14].
Основні клінічні прояви захворювання відомі з кінця XIX — початку XX століття. Мігруюча ерітема (МЕ) була описана в 1909 році шведським дерматологом А. Афцеліусом. Особливості мігруючої еритеми у 1913 році детально описав австрійський бактеріолог та дерматолог Б. Ліпшюц. Випадок МЕ з подальшим розвитком менінгіту був описаний в 1930 році С. Хеллестромом [3]. Перші випадки синдрому Баннварта, менінгорадикулоневропатії, яка розвинулася після присмоктування кліща і МЕ, були повідомлені Гаре і Буйо в 1922 р, а в 1944 році — Баннвартом [4]. У 1960 році Шальтенбранд та інші європейські неврологи вивчали великі групи хворих з больовою радікулоневропатією, невропатією черепних нервів або лімфоцитарним менінгоенцефалітом, які розвивалися внаслідок присмоктування кліща [14]. Інтенсивне дослідження ЛБ почалося лише з 1970-го року після опису в США Аленом Стиром Лайм-артриту і відкриття Віллі Бургдорфером збудника захворювання [13]. Низкою подальших досліджень [10, 12, 13] було доведено етіологічну спільність всіх перерахованих вище синдромів. Стало очевидно, що ЛБ — дуже поширений зооноз.
Захворювання Лайм-бореліозу на територіях північної Америки, Центрально-Східної Європи, в тому числі й України, Азії, північної Африки та Австралії посідають перше місце серед природно-осередкових інфекцій, а за темпами розповсюдження — друге місце після ВІЛ-інфекції, що становить від 10 до 50 випадків більше ніж на 100 тис. населення щорічно [4, 6]. Про перші випадки захворювання людей на хронічний Лайм-бореліоз в Україні стало відомо тільки в 1994 p., а офіційна реєстрація захворювання ведеться лише з 2000 р. [6]. За даними ВООЗ, середня багатолітня захворюваність ЛБ в Україні складала 0,9±0,2 на 100 тис. населення [7], і зустрічається у всіх 23 адміністративних областях країни. Високий рівень захворюваності спостерігається в м. Києві, Чернігівській, Черкаській, Сумській, Львівській і Донецькій областях [14]. Частота уражень нервової системи при хронічному Лайм-бореліозі — від 10 до 40% [2, 8, 9]. Захворюваність на нейробореліоз у 2–4 рази вища, ніж на кліщовий енцефаліт [4]. Віддалені ураження нервової системи проявляються через місяці та роки після початку захворювання, часто після тривалого латентного періоду, включаючи ознаки ураження всіх відділів нервової системи. Виділяють [10–12] такі форми хронічного ЛБ з ураженням нервової системи: прогресуючий енцефаломієліт, церебральний васкуліт, енцефалопатія, радикулопатія, поліневропатія, хронічний лімфоцитарний менінгіт.
Дані вітчизняної та зарубіжної літератури достатньо повно висвітлюють особливості етіопатогенезу в різних країнах та областях, клінічний перебіг гострого та хронічного Лайм-бореліозу, діагностичні критерії та методи лікування. Але, водночас клініко-імунологічні особливості Лайм-бореліозу, що супроводжується ураженням нервової системи, а також питання, пов’язані з діагностикою та комплексною етіопатогенетичною терапією таких хворих, залишаються не вирішеними і потребують подальшого дослідження [1, 4, 7].
Усі відомі нині імунотропні засоби представлені надзвичайно широким поєднанням природного та синтетичного походження і спектр їх на фармацевтичному ринку постійно розширюється. При цьому дуже важлива здатність препарату здійснювати спрямований імунотропний регулюючий вплив на певні фактори імунної відповіді: фагоцитоз, цитотоксичну активність лімфоцитів або синтез антитіл, відновлюючи нормальну міжклітинну кооперацію і противірусний імунний захист. Такими властивостями володіє препарат азоксимера бромід (сополімер N-окси-1,4-етиленпіперазину і (N-карбокси) -1,4-етиленпіперазиній броміду). У дослідах in vitro мішенями дії азоксимера броміду були клітини фагоцитарної системи: моноцити і нейтрофіли. При взаємодії з мононуклеарами периферійної крові азоксимера бромід індукує синтез моноцитами цитокінів: чинник некрозу пухлин-α (ФНП-α) та інтерлейкін-β, а також посилює цитотоксичність NK-клітин, але тільки при початково низьких або середніх їх рівнях. Експериментальними методами також встановлено, що препарат практично не проникає в лімфоцити. В умовах in vitro лімфоцити периферійної крові не змінюють своєї активності під впливом азоксимера броміду. Крім того, азоксимера бромід не має здатності індукувати синтез інтерферонів [6]. Ці властивості препарату зумовлюють патогенетичну доцільність його застосування у пацієнтів з вірусною та бактеріальною інфекцією.
Мета — вивчити клінічні особливості перебігу
Лайм-бореліозу у хворих при застосуванні препарату азоксимера бромід.
Матеріали і методи. Обстежено 72 хворих на Лайм-бореліоз, з них жінок — 42, чоловіків — 30. Середній вік хворих складав 37,5±2,5 роки. Проводилась оцінка неврологічного статусу, магнітно-резонансна томографія головного та спинного мозку, офтальмоскопія, електронейроміографія, комплексна імунограма. Серологічна діагностика ЛБ була основана на дослідженні сироватки крові на антитіла IgM та IgG до борелій за допомогою імуноферментного аналізу і\ або імуноблоту.
Результати та їх обговорення.
Встановлено такі клінічні діагнози: ураження шкіри у вигляді кільцеподібної еритеми у 18 хворих, опорно-рухового апарату — у 4, нервової системи — у 50 хворих, переважали жінки, хворіли особи працездатного віку. Встановлено, що ураження нервової системи, вірогідно, можна пов’язати з Borrelia garini, яку було виявлено у 80% пацієнтів з Лайм-бореліозом, що супроводжувався неврологічними проявами.
Всі хворі з ураженням нервової системи були розподілені на 2 дослідних групи:
1-ша група — 24 хворих (основна група А) — отримувала етіотропну (цефтриаксон, метронідазол у середньотерапевтичних дозах), патогенетичну (нейропротекція, протизапальні, протинабрякові препарати etc.) терапію та азоксимера бромід внутрішньом’язово по 6 мг 1 раз на 48 годин 10 днів.
Пацієнтів 2-ої групи — 26 хворих, группа (В) — лікували комбінацією цефтриаксоном внутрішньовенно в середньо терапевтичних дозах.
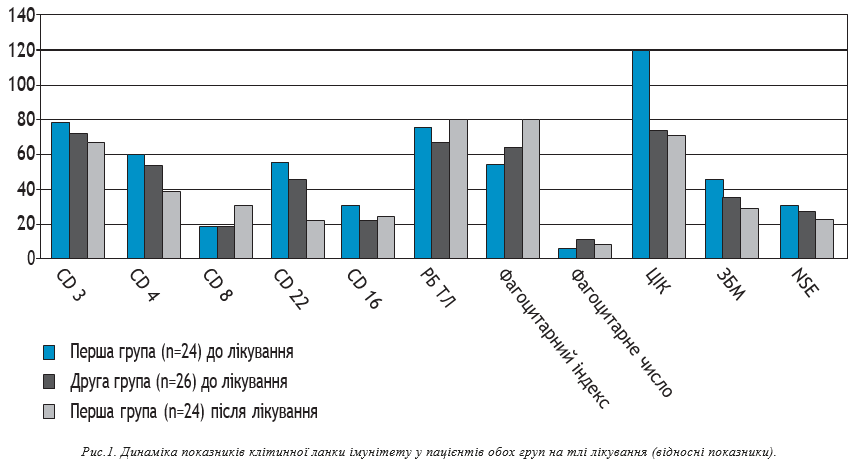
Дослідження імунного статусу виявили характерні для цієї патології зміни в обох групах пацієнтів, які проявлялись у деякому зниженні рівня лімфоцитів у крові та дисбалансом у складі окремих їх субпопуляцій.
В обох групах хворих було виявлено підвищення рівня показників аутоімунних реакцій (ЦІК, сенсибілізації NSE, рівня антитіл до загального білку мієліну (ЗБМ), та зниження імунорегуляторного індексу, спонтанної фагоцитарної активності нейтрофілів).
Порівняльний аналіз інтенсивності синдромів захворювання (коефіцієнт ознаки першої/другої групи) при Лайм-бореліозі представлено в таблиці 1.
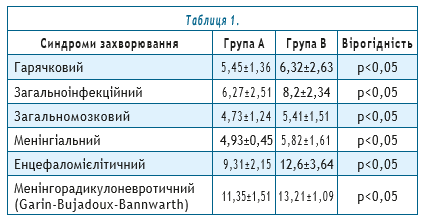
Гарячковий синдром у групі пацієнтів, що отримували азоксимера бромід в (84,5%) випадків був коротший на 2,1±0,2 дня, повторних спалахів підвищення температури тіла не спостерігалося. Температурна реакція становила 37,6±1,2 0С (37–39 0С), порівняно з другою групою (В) нижче на 1,6±0,7 0С, але в (11,8%) випадків на тлі субфебрильної лихоманки відзначалися «фебрильні сплески».
Загальноінфекційний синдром в обох групах відповідно проявлявся: загальною слабкістю і втомою 32,8 і 47,5 (р>0,05); нездужанням і швидкою стомлюваністю 33,8 і 36,3 (р<0,05); болем, напруженням м’язів шиї 17,9 і 22,4 (р<0,05); болем у тілі та міалгіями 39,8 і 47,5 (р<0,05); артралгіями 14,5 і 18,2 (р<0,05); ознобом 17,9 і 25,6 (р<0,05); гіпергідрозом 19,6 і 27,1 (р>0,05); вегетативною дистонією 39,6 і 41,3 (р<0,05); порушенням сну 11,6 і 14,8 (р<0,05); астенією 36,3 і 56,1 (р<0,05).
Загальномозковий синдром (при гарячковій формі): цефалгія — 32,1 і 48,6 (р<0,05); нудота, блювота 17,9 і 18,6 (р<0,05); запаморочення 16,4 і 21,9 (р<0,05).
Менінгеальний синдром проявлявся у вигляді помірної та вираженої цефалгії 51,2 і 78,4 (р<0,05); нудоти 29,7 і 36,2 (р<0,05); болем при русі очних яблук 37,3 і 38,6 (р<0,05); гіперстезією до звуків і світлобоязню 36,9 і 38,1 (р<0,05).
Енцефаломієлітичний синдром в (47,1%) починався з больових відчуттів у місці присмоктування кліща, які (41,2%) посилювалися вночі та супроводжувалися парастезіями і сенестопатіями. Згодом на тлі лихоманки з’являлися болі в спині, хребті, відзначалися порушення чутливості за корінцевим типом, які з однаковою частотою зустрічалися у всіх відділах хребта в обох групах. Найбільш виражені болі були в грудному відділі. Больові прояви супроводжувалися відчуттям стиснення, тиску, онімінням, в одній чверті випадків (обох групах), у скаргах спостерігалася гіпо- і гіперестезія, слабкість м’язів. На 18±5,7 день в (21,7%) у цих зонах можна було спостерігати гіпотрофію м’язів. Корінцеві болі майже в 50% випадків зберігалися протягом усього захворювання і могли змінюватися характером та інтенсивністю. Водночас відзначалася мала чутливість цих хворих до анальгетиків, а враховуючи, що в (47,1%) загальномозкові та гарячкові прояви були слабко виражені, то створювалося враження «компресії корінця».
При прогресуванні процесу можна було спостерігати не тільки клініку ураження периферичного нерва, але залучення нервових сплетінь — у 3 випадках (17,7%). Чутливі порушення зустрічалися в — 36,2% випадках; зниження больової чутливості — 49,3%; тактильної — 46,7%; гіпестезії — 48,5%; гіпералгезії — 36,2%; зниження вібраційної чутливості — 48,4%; рефлекторні порушення — 36,2%; рухові — 73,4%; парези і м’язова гіпотрофія — 16,6%. Симптомів, які відрізнялися частотою або проявом інтенсивності, в обох групах не спостерігалося.
Спинномозкова рідина при менінгіальному синдромі нейробореліозу за своїми показниками в обох групах була однорідною: прозора, в 46,9% і 41,0% спостерігався помірний лімфоцитарний плеоцитоз. У перші дні захворювання в 15,2% переважали нейтрофіли до 55,1±5,0%, вміст білка до 0,66 г/л, показники глюкози у всіх випадках були ½ від вмісту в плазмі крові. Показники лейкоцитарного індексу інтоксикації: при ЛБ (відповідно в групах) 0,74+0,21 і 1,14±0,12 (р<0,01), порівняльна оцінка критеріїв синдрому системної запальної реакції (СЗР) (з використанням автоматизованого статистичного пакету Statistica 6.0.) При ЛБ у 26 пацієнтів, що отримували азоксимера бромід (в порівняння з контрольною групою) показала співвідношення 2,2/2,7.
Зниження термінів захворюваності (стаціонар) при застосуванні азоксимера броміду склало на 3,5±1,2 днів.
При дослідженні імунного статусу хворих при лікуванні препаратом азоксимера бромідом, були відмічені такі позитивні зміни: підвищення фагоцитарного індексу, фагоцитарного числа, РБТЛ з ФГА, зниження ЦІК.
Висновки.
Поліморфізм клінічних проявів Лайм-бореліозу зумовлює необхідність застосування комплексної терапії для лікування цього захворювання.
Застосування азоксимера броміду для лікування кліщового бореліозу при всіх клінічних формах проявів захворювань є досить ефективним. При використанні препарату в якості імунотропного препарату при лікуванні Лайм-бореліозу у хворих виявлено збільшення функціональної активності ефекторних клітин імунної системи, стимуляцію фагоцитарної активності та зниження вираженості аутоімунних реакцій, що свідчить про нормалізацію функціональних взаємозв’язків імунної відповіді. Застосування препарату дозволило скоротити терміни лікування в стаціонарі на 3,5±1,2 днів, при цьому відзначалася висока етіологічна ефективність і відсутність ускладнень, крім того він зручний для застосування і може бути включений в комплексне лікування іксодового кліщового бореліозу.
Література
- Bamm V., Ko J. T., Mainprize I. L., Sanderson V. P., Wills M. B. Lyme disease frontiers: reconciling Borrelia biology and clinical conundrums. Pathogens. 2019;8(4):299. doi:10.3390/ pathogens8040299.
- Adkison H., Embers M. E. Lyme disease and the pursuit of a clinical Front Med (Lausanne). 2023 May 24;10:1183344. doi: 10.3389/ fmed.2023.1183344..
- Hellerström S. «Erythema chronicum migrans Afzelii». Acta Derm.-1930; 11: 315–21. (нім).
- Клюс В. Ю, Руденко А. О., Дьяченко П. А., Муравська Л. В., Пархомець Б. А., Шагінян В. Р., Фільчаков В. І.. Діагностика уражень нервової системи у хворих на Лайм-бореліоз. Досягнення біології та медицини». 2017; №1(29): 68–71.
- Sebastian Rauer, Stephan Kastenbauer, Heidelore Hofmann, Volker Fingerle, Hans-Iko Huppertz, Klaus-Peter Hunfeld et al. Guidelines for diagnosis and treatment in neurology — Lyme neuroborreliosis. Ger Med 2020; 18: Doc03 . doi: 10.3205/000279.
- Луценко В. Ю., Руденко А. О. Застосування препарату поліоксидонію в комплексній терапії Лайм-бореліозу. Проблеми військової охорони здоров’я. Збірник наукових праць Української військово-медичної академії . 2015; 44 (2): С. 231–2
- Зінчук О. М. Cинтропічне ураження серця у хворих на Лайм-бореліоз: (клініко-електрокардіоґрафічні ознаки; опис клінічного випадку). Львів. клін. вісн. 2013;(2):49–51.
- Gyllemark P., Wilhelmsson P., Elm C., Hoornstra D., Hovius J. W., Johansson et al. Are other tick-borne infections overlooked in patients investigated for Lyme neuroborreliosis? A large retrospective study from South-eastern Sweden. Ticks Tick Borne Dis. 2021 Sep;12(5):101759. doi: 10.1016/j.ttbdis.2021.101759.
- Haahr R., Tetens M. M., Dessau R. B., Krogfelt K. A., Bodilsen J., Andersen N. S. et al. Risk of neurological disorders in patients with European Lyme neuroborreliosis: A nationwide, population-based cohort study. Clin Infect 2020 Sep 12;71(6):1511–1516. doi: 10.1093/ cid/ciz997.
- Geebelen L., Lernout T., Devleesschauwer B., Kabamba-Mukadi B., Saegeman V., Belkhir L. et al. Non-specific symptoms and posttreatment Lyme disease syndrome in patients with Lyme borreliosis: a prospective cohort study in Belgium (2016–2020). BMC Infect Dis. 2022 Sep 28;22(1):756. doi: 1186/s12879-022-07686-8.
- Федонюк Л. Я., Довбуш А. В., Багрій М. М. Клінічно-епідеміологічна характеристика Лайм-бореліозу в Тернопільській області. Буковин. мед. вісн. 2013;17(1):194–8.
- Asbrink The man behind the syndrome. Arvid Afzelius. The first to recognize the key symptom in tick-transmitted borreliosis. Lakartidningen. 1990;87(23):2046–8.
- Steere A. C., Malawista S. E. Cases of Lyme disease in the United States: locations correlated with distribution of Ixodes Ann Intern Med. 1979;91(5):730–3. doi:10.7326/0003-4819-91-5-730.
- Про затвердження Переліку інфекційних захворювань: наказ МОЗ України від 04.2016 № 362 [Інтернет]. Київ; 2016 [оновлено 2020 Січ 10; цитовано 2020 Трав 13]. Доступно: https://zakon.rada. gov.ua/laws/show/z0714-16#Text.
Відомості про авторів:
Дьяченко П. А. — к. м. н., завідувач відділу нейроінфекції Центру інфекційних уражень нервової системи ДУ «Інститут епідеміології та інфекційних хвороб імені Л. В. Громашевського НАМН України».
ORCID: 0000-0002-0459-9861
Клюс В. Ю. — к. м. н., с. н. с. відділу нейроінфекції Центру інфекційних уражень нервової системи ДУ «Інститут епідеміології та інфекційних хвороб імені Л. В. Громашевського НАМН України».
Information about the authors:
Dyachenko P. A. — PhD of medicine, Head of the department of neuroinfection Cеntег of infectious disorders of the nervous system, SI “L. V. Hromashevskyi institute of epidemiology and infection diseases of NAMS of Ukraine”.
ORCID: 0000-0002-0459-9861
Klyus V. Yu. — PhD of Medicine, senior researcher of the neuroinfection department of the Center for Infectious Lesions of the Nervous System of the SI “L. V. Hromashevskyi Institute of Epidemiology and Infectious Diseases of NAMS of Ukraine”.
