COVID-19 і ВІЛ-інфекція. Імунологічна відповідь на вакцину та ефективність вакцинації
УДК 578.834+616.98:578.828+351.774.7
В. Р. Шагінян, І. В. Фільчаков, Т. А. Сергеєва, О. М. Кислих, О. В. Максименок, С. М. Антоняк, О. В. Мурашко
ДУ «Інститут епідеміології та інфекційних хвороб ім. Л. В. Громашевського НАМН України»
Питання ефективності вакцинації проти COVID-19 людей, які живуть із ВІЛ (ЛЖВ) активно вивчаються. Згідно з даними досліджень, ЛЖВ, у яких кількість CD4 на рівні понад 500 кл/мкл демонструють таку саму імунологічну відповідь на вакцину, як і ВІЛ-негативні особи. Захисна дія вакцинації для попередження випадків захворювання остаточно не вивчена.
Мета роботи: вивчення імунологічної відповіді на вакцинацію проти COVID-19 та протективної дії вакцини у ЛЖВ.
Матеріали та методи. Перший етап (листопад 2022 р.) — проведено опитування 558 пацієнтів з ВІЛ-інфекцією. Медіана віку пацієнтів — 42 роки, 52,8% — чоловіки. Медіана кількості CD4 — 578,5 кл/мкл. У 96,4% був невизначуваний рівень вірусного навантаження ВІЛ. Отримували АРТ понад 6 місяців 95,7% пацієнтів. Повний курс вакцинації проти COVID-19 отримали 56,8% осіб. На другому етапі (січень–березень 2023 р.) обстежено 481 пацієнта (медіана віку 43 роки, медіана CD4 — 567,5 кл/мкл) на наявність та рівень антитіл до Spike-антигену SARS-CoV-2. Використовували імуноферментні тест-системи для кількісного визначення IgG до Spike-антигену коронавірусу SARS-CoV-2 виробництва «Діапроф-Мед» (Україна). Обстеженню передувало анонімне анкетування.
Результати та їх обговорення. За результатами опитування, показник охоплення щепленнями ЛЖВ виявився вищим, ніж населення України загалом, водночас захворюваність на COVID-19 ЛЖВ була вищою порівняно із показниками захворюваності в Україні на період проведення опитування. Випадки захворювань серед щеплених ЛЖВ зустрічалися частіше, ніж серед населення країни загалом. Переважна більшість (94,4%) захворілих на COVID-19 ЛЖВ не потребувала госпіталізації. При обстеженні 481 ЛЖВ високий рівень антитіл встановлений у 34 (7,1%) обстежених, середній — у 343 (71,3%), низький — у 36 (7,5%), антитіла не виявлені — у 68 (14,1%). Антитіла достовірно частіше (р<0,005) виявлялись у щеплених (95,4%), ніж у нещеплених (72,6%). Імунна відповідь на вакцини проти COVID-19 у ЛЖВ була в межах, задекларованих виробниками в інструкціях до вакцин (95,4%). Відсоток осіб із захисним рівнем антитіл (високий та середній) був вищим серед щеплених (90,8%), ніж серед нещеплених (61,2%). У 64% нещеплених ЛЖВ були виявлені антитіла до SARS-CoV-2 за відсутності захворювання на COVID-19 в анамнезі, що дозволяє припустити в них безсимптомний перебіг хвороби. У 76,9% вакцинованих серонегативних ЛЖВ кількість CD4 Т-клітин була менше 500 кл/мкл. Встановлено, що не захворіли на COVID-19 60,7±3,4% нещеплених ЛЖВ проти 45,4±3,0% щеплених, р<0,05. Повторні випадки захворювання на COVID-19 відмічали 5,2% обстежених ЛЖВ. Серед щеплених частота повторних випадків була вищою (6,4%), ніж серед нещеплених (3,5%). За результатами проведених розрахунків зв’язок між вакцинацією та ймовірністю захворювання на COVID-19 в обстеженій групі ЛЖВ виявився несуттєвим.
Висновки. Наше дослідження продемонструвало хорошу імунну відповідь на вакцину проти COVID-19 у ЛЖВ. Водночас нами не доведена ефективність вакцинації для попередження випадків COVID-19.
Ключові слова: COVID-19, ВІЛ-інфекція, рівень антитіл до Spike-антигену, ефективність вакцинації.
V. R. Shahinian, I. V. Filchakov, T. A. Serheieva, O. M. Kyslykh, V. Maksymenok, S. M. Antoniak, O. V. Murashko
COVID-19 and HIV-infection. Immunological response to the vaccine and effectiveness of vaccination
State Institution “L. V. Gromashevsky Institute of Epidemiology and Infectious Diseases of National Academy of Medical Science of Ukraine”
The effectiveness of vaccination against COVID-19 of people living with HIV (PLWH) is being actively studied. According to studies, PLWH with a CD4 count of more than 500 cells/μL show the same immunological response to the vaccine as HIV-negative individuals. The protective effect of vaccination to prevent cases of the disease has not been definitively studied.
The purpose of the work: to study the immunological response to vaccination against COVID-19 and the protective effect of the vaccine in PLWH.
Materials and methods. The first stage (November 2022) — a survey of 558 patients with HIV infection was conducted. The median age of patients is 42 years, 52.8% are men. The median CD4 count is 578.5 cells/μl. 96.4% had an undetectable HIV viral load. 95.7% of patients received ART for more than 6 months. 56.8% of people received a full course of vaccination against COVID-19. At the second stage (January-March 2023) 481 patients (median age 43 years, median CD4 — 567.5 cells/μl) were examined for the presence and level of antibodies to the SARS-CoV-2 Spike antigen. Immunoenzyme test systems were used for the quantitative determination of IgG to the Spike antigen of the SARS-CoV-2 coronavirus manufactured by Diaprof-med (Ukraine). The examination was preceded by an anonymous questionnaire.
Results and their discussion. According to the results of the survey, the rate of vaccination coverage of PLWH was higher than the population of Ukraine as a whole, at the same time, the incidence of COVID-19 among PLWH was higher compared to the incidence rates in Ukraine during the survey period. Disease cases among vaccinated PLWH occurred more often than among the population of the country as a whole. The vast majority (94.4%) of PLWH infected with COVID-19 did not require hospitalization. During the examination of 481 PLWH, a high level of antibodies was established in 34 (7.1%) of the examined, an average level — in 343 (71.3%), a low level — in 36 (7.5%), antibodies were not detected — in 68 (14.1%). Antibodies were significantly more often (p<0.005) detected in vaccinated (95.4%) than in unvaccinated (72.6%). The immune response to the vaccines against COVID-19 in PLWH was within the limits declared by the manufacturers in the vaccine instructions (95.4%). The percentage of persons with a protective level of antibodies (high and medium) was higher among the vaccinated (90.8%) than among the unvaccinated (61.2%). Antibodies to SARS-CoV-2 were detected in 64% of unvaccinated PLWH in the absence of a history of COVID-19 disease, which allows us to assume that they have an asymptomatic course of the disease. In 76.9% of vaccinated seronegative PLWH, the number of CD4 T cells was less than 500 cells/μl. It was established that 60.7±3.4% of unvaccinated PLWH did not get sick with COVID-19 compared to 45.4±3.0% of vaccinated people, p<0.05. Repeated cases of COVID-19 were noted by 5.2% of examined PLWH. Among the vaccinated, the frequency of repeated cases was higher (6.4%) than among the unvaccinated (3.5%). According to the results of the calculations, the relationship between vaccination and the probability of COVID-19 disease in the examined group of PLWH turned out to be insignificant.
Conclusion. Our study demonstrated a good immune response to vaccine against COVID-19 in PLWH. At the same time, we have not proven the effectiveness of vaccination to prevent cases of COVID-19.
Key words: COVID-19, HIV infection, the level of antibodies to the Spike antigen, the effectiveness of vaccination.
На початку пандемії COVID-19 серйозну стурбованість медичної спільноти викликав її можливий вплив на людей, які живуть із ВІЛ (ЛЖВ).
Найважливішими були питання клінічного перебігу ко-інфекції. Чи збільшує ВІЛ-інфекція ризики ускладнень і важкого перебігу COVID-19 та які фактори можуть впливати на клінічний перебіг COVID-19 у ЛЖВ? Чи є ЛЖВ групою ризику щодо інфікування SARS-CoV-2? На теперішній час, згідно з даними низки оглядів, захворюваність на COVID-19 серед ЛЖВ у країнах Європи знаходиться в межах 0,3–5,7% осіб у рік [1, 2, 3], а відсоток ЛЖВ серед госпіталізованих пацієнтів з COVID-19 складає 0,26–1,0% [4, 5]. За узагальненими даними, наведеними в огляді, опублікованому у 2022 р., захворюваність на COVID-19 серед ЛЖВ не відрізняється від захворюваності населення загалом [6]. Результати систематизованого огляду та метааналізу свідчать про те, що ЛЖВ, які отримують антиретровірусну терапію (АРТ), не мають підвищеного ризику ускладнень COVID-19 порівняно з ВІЛ-негативними особами [7]. З початку впровадження вакцинації проти COVID-19 активно вивчаються питання імуногенності різних вакцин у ЛЖВ, яких все-таки вважають групою ризику, що насамперед підлягає вакцинації. Дані різних джерел доволі неоднозначні, хоча більшість дослідників та фахівців, які узагальнюють результати різних досліджень в оглядах, стверджують, що у відповідь на вакцинацію проти COVID-19 ЛЖВ, які знаходяться на АРТ, що дозволяє підтримувати кількість CD4 Т-клітин на рівні більше 500 кл/мкл, демонструють таку саму гуморальну відповідь, як і ВІЛ-негативні особи, водночас ЛЖВ, у яких кількість CD4 Т-клітин є меншою за 200 кл/мкл, гірше відповідають на вакцинацію проти COVID-19 [8, 9, 10, 11]. З’явилися повідомлення і про те, що у ЛЖВ частота «прориву інфекції» (випадки захворювань у щеплених) є вищою, ніж у ВІЛ-негативних осіб, переважно при інфікуванні варіантами Delta та Omicron [6, 12]. Загалом дані щодо впливу вакцинації на наслідки COVID-19 у ЛЖВ обмежені.
Мета роботи. Оцінити імунологічну відповідь на вакцинацію проти COVID-19 та протективну дію вакцин у ЛЖВ.
Матеріали та методи. З метою первинної оцінки захворюваності на COVID-19 та стану охоплення щепленнями проти SARS-CoV-2 ЛЖВ було розроблено анкету/опитувальник для пацієнтів з ВІЛ-інфекцією, які перебували під систематичним наглядом у відділенні СНІДу клініки ДУ «Інститут епідеміології та інфекційних хвороб ім. Л. В. Громашевського НАМН України». Анкетування проводилось за принципом Convenience samling. Це швидкий, недорогий і зручний метод формування вибірки, який найчастіше застосовується та широко використовується у клінічних дослідженнях. Він є оптимальним підходом для проведення пілотних досліджень [13]. Загальна кількість учасників дослідження склала 558 пацієнтів, з них 295 чоловіків (52,9%) та 263 (47,1%) жінки. Медіана віку пацієнтів — 42 роки. Показник кількості CD4 (медіана) на момент проведення дослідження — 578,5 (кл/мкл). Понад 6 місяців отримували АРТ 534 (95,7%) пацієнти. У переважної більшості з них — 515/534 (96,4%) був невизначуваний рівень вірусного навантаження ВІЛ (<40 РНК ВІЛ копій/мл).
Повний основний курс вакцинації проти COVID-19 отримали 317 (56,8%) осіб. Анкетування ЛЖВ проведено впродовж 8–28 листопада 2022 року.
На другому етапі дослідження (січень–березень 2023 р.) було обстежено 481 пацієнта на наявність та рівень антитіл до Spike-антигену SARS-CoV-2: 181 жінка (37,6%) та 300 чоловіків (62,4%). Обстеженню передувало анонімне анкетування, метою якого було з’ясування факту захворювання на COVID-19 (лабораторне підтвердження діагнозу, дата захворювання), отримання вакцини проти COVID-19 (назва вакцини, кількість доз, дати вакцинації). Згідно з даними анкетування, обстежені ЛЖВ були щеплені різними вакцинами. Найчастіше (40%) щеплення були проведені вакциною Pfizer-BioNTech. Вакциною CoronaVac щеплено 34% обстежених, Moderna — 14%, комбінацію з різних вакцин отримали 9%, Covishield (Oxford/ AstraZeneca) — 3%, Janssen (Johnson & Johnson) — 1%. Середній вік обстежених був 43 роки (від 20 до 60 років). Показник кількості CD4 (медіана) серед учасників другого етапу дослідження – 567,5 (кл/мкл). Отримували АРТ 458 із 481 (95,2%) пацієнта. У 431/458 (94,1%) ЛЖВ, які отримували АРТ, був невизначуваний рівень вірусного навантаження ВІЛ (<40 РНК ВІЛ копій/мл).
Для визначення рівня антитіл використовували імуноферментні тест-системи для кількісного визначення IgG до Spike-антигену коронавірусу SARS-CoV-2 виробництва«Діапроф-Мед»(Україна).КонцентраціюIgG у кожному досліджуваному зразку визначали в BAU/мл згідно з інструкцією до тест-системи: <8 BAU/мл — негативний результат; >125 BAU/мл — високий рівень антитіл; 30–125 BAU/мл — середній рівень антитіл; 8–30 BAU/мл — низький рівень антитіл.
Статистична обробка даних проводилася за допомогою комп’ютерної програми Statisticа 6.0 (StatSoft Inc., США) та програми Excel.
Результати та їх обговорення. При попередньому опитуванні 558 ЛЖВ, не пов’язаному з тестуванням, були отримані такі дані. Перехворіли на COVID-19 304 ЛЖВ (54,5%). З них 73% перехворіли на COVID-19 один раз, 20,7% — двічі, 6,3% — тричі та більше. Слід зазначити, що діагноз був підтверджений лабораторно тільки у 65,8% пацієнтів. Внаслідок захворювання на COVID-19 були госпіталізовані 17 осіб (5,6%), із них один пацієнт — у відділення інтенсивної терапії. Даний пацієнт отримав три щеплення проти COVID-19. Серед опитаних хоча б одну дозу вакцини проти COVID-19 отримали 59,9% осіб. Цей показник вищий, ніж серед дорослого населення України загалом. Згідно з даними ЦГЗ МОЗ України, на період проведення опитування одну та більше доз вакцини отримали менше 40% населення. Дві дози вакцини отримали 56,8% ЛЖВ. Бустерні дози вакцини отримали 79 пацієнтів, з них одну дозу — 20,4%, дві — 3,3%. Серед 304 захворілих ЛЖВ 191 (62,8%) був щеплений проти COVID-19, з них 94,2% отримали повний курс вакцинації (2 дози вакцини).
Отже, за результатами опитування показник охоплення щепленнями ЛЖВ виявився вищим, ніж населення України загалом, водночас захворюваність на COVID-19 ЛЖВ була вищою порівняно із показниками захворюваності по Україні на період проведення опитування (≈4 000 на 100 тис. населення). Випадки захворювань серед щеплених ЛЖВ зустрічалися частіше, ніж серед населення країни загалом (відповідно до даних звітності ЦГЗ на цей період). Зокрема, згідно з даними ЦГЗ, станом на 24.11.2022 р. частка вакцинованих серед захворілих в Україні за період з 01.06.2021 р. складала 16,1%, з коливаннями від 3,8% до 30,7% в окремих регіонах. Оскільки показник охоплення щепленнями серед ЛЖВ був вищим, ніж серед загального населення, вищим виявився і відсоток щеплених серед захворілих (62,8%), тобто вакцинація не вплинула на захворюваність даної групи пацієнтів. Слід зазначити, що переважна більшість захворілих ЛЖВ (94,4%) не потребувала госпіталізації, що свідчить про нетяжкий перебіг хвороби.
При обстеженні 481 ЛЖВ на наявність та рівень антитіл до Spike-антигену SARS-CoV-2 (далі — антитіла) були отримані такі результати.
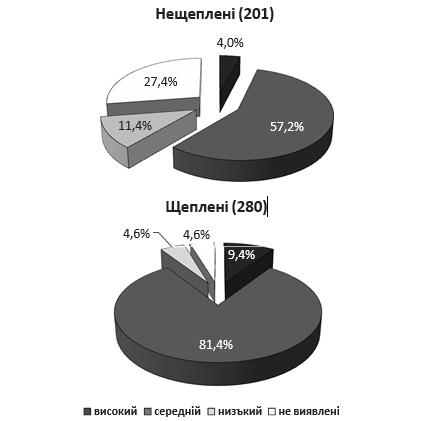
Високий рівень антитіл був виявлений у 34 (7,1%) обстежених, середній — у 343 (71,3%), низький — у 36 (7,5%), антитіла не виявлені — у 68 (14,1%). Оскільки серед обстежених були як щеплені (280 осіб), так і нещеплені (201 особа) ЛЖВ, ми розрахували показники виявлення антитіл різного рівня (високий, середній, низький, антитіла не виявлені) в цих групах окремо. Дані наведено на рис. 1.
Рис. 1. Частота виявлення антитіл різного рівня в групах обстежених ЛЖВ
Загалом антитіла в тій чи іншій концентрації достовірно частіше (р<0,005) виявлялись у щеплених (95,4%), ніж у нещеплених (72,6%). Відсоток осіб із захисним рівнем антитіл (високий та середній) був вищим серед щеплених (90,8%), ніж серед нещеплених (61,2%). Відповідно, серед нещеплених відсоток серонегативних осіб був достовірно вищим, аніж серед щеплених (27,4% та 4,6% відповідно). Згідно з даними літератури, в більшості випадків наявність високих титрів антитіл знижує ризик зараження SARS-CoV-2 [14, 15]. Отже, за результатами нашого обстеження можна вважати, що 90,8% щеплених ЛЖВ, за рівнем антитіл (високий або середній), теоретично, мали бути захищеними від захворювання. Проте, як серед щеплених, так і серед нещеплених ЛЖВ були особи, які перехворіли на COVID-19.
Відомо, що вакцинація у перехворілих (так само як і захворювання після вакцинації) посилює імунну відповідь на антигени SARS-CoV-2. Відповідно, рівень антитіл у перехворілих щеплених мав бути вищим, ніж у перехворілих нещеплених. У попередні роки було показано, що вакцинація перехворілих на COVID-19 сприяла підсиленню імунної відповіді навіть після однієї дози вакцини [16]. Дані, наведені на рис. 2, це підтверджують. Антитіла на захисному рівні були визначені у 94,1% щеплених перехворілих. Загалом антитіла виявлені у 98,0% щеплених перехворілих та у 86,1% нещеплених перехворілих (р>0,05). Відсутність достовірної різниці може бути зумовлена, зокрема, невеликою вибіркою в групах.
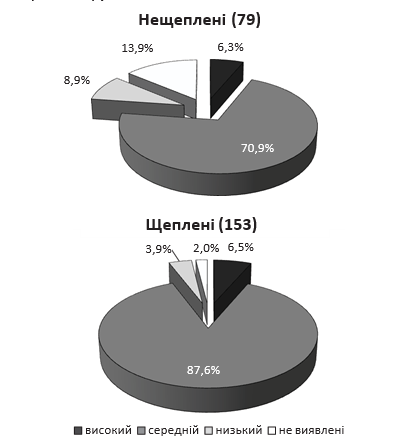
Рис. 2. Частота виявлення антитіл різного рівня у перехворілих на COVID-19 ЛЖВ
У певної частки нещеплених ЛЖВ, які не вважали, що перехворіли на COVID-19, були виявлені антитіла до SARS-CoV-2. Такі випадки можна вважати безсимптомним перебігом COVID-19. Ми розрахували його частоту серед обстежених ЛЖВ. Серед нещеплених хворіли 79 осіб, відповідно 122 ЛЖВ вважали, що не хворіли на COVID-19, не зверталися з цього приводу до лікаря та не були обстежені. Серед зазначених 122 осіб антитіла були виявлені у 78 (64,0%), з них у 62 (79,5%) на захисному рівні. Отже, безсимптомну форму COVID-19 перенесли принаймні 64% нещеплених ЛЖВ, майже у 80% з них були антитіла на захисному рівні. Ці дані узгоджуються з результатами, отриманими іншими авторами [17]. Оцінити частоту безсимптомного перебігу COVID-19 у щеплених неможливо, оскільки в них будуть виявлені антитіла, сформовані внаслідок вакцинації.
У групі обстежених ЛЖВ кількість перехворілих та неперехворілих на COVID-19 суттєво не відрізнялась. За результатами опитування, перехворіли на COVID-19 232 особи (48,2%), не хворіли — 249 (51,8%). В таблиці 1 наведено дані щодо розподілу перехворілих на COVID-19 серед щеплених та нещеплених ЛЖВ
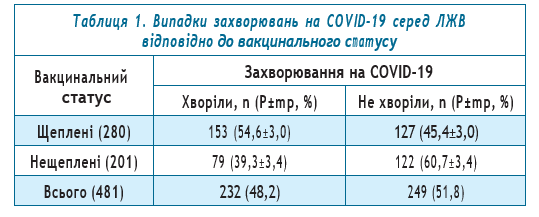
Розподіл обстежених за ознаками захворювання на COVID-19 серед щеплених та нещеплених ЛЖВ був неоднаковим. Серед щеплених відсоток тих, хто хворів був вищим, ніж серед нещеплених (54,6% та 45,4%, відповідно). Але ми вирішили не порівнювати ці показники, оскільки слід враховувати, коли було захворювання — до або після щеплення. Розрахунки зв’язку між вакцинацією та ризиком захворіти на COVID-19 після щеплення будуть надані нижче. Більш важливим, на наш погляд, є порівняння відсотків тих, хто не хворів на COVID-19. Задача будь якої вакцинації — зменшення кількості випадків захворювань. Відомо, що жодна вакцина не дає 100% захисту, але відсоток захищених — тих, хто не захворів серед вакцинованих, має бути вищим, ніж серед невакцинованих. Проте, за нашими результатами, виявилось навпаки. Відсоток тих, хто не захворів на COVID-19 серед нещеплених ЛЖВ, виявився достовірно вищим (р<0,05), ніж серед щеплених (60,7% та 45,4% відповідно). Слід нагадати, що імунна відповідь на антигени, які містять вакцини проти COVID-19, була визначена нами більш ніж у 90% щеплених. Отже, виникає логічне питання – чи захищають антитіла, які виробляються на вакцину, від захворювання на COVID-19? У цьому контексті, можливо, стає зрозумілим твердження, що рутинне тестування на індуковану вакциною гуморальну імунну відповідь на SARS-CoV-2 не рекомендується використовувати як параметр «захисного імунітету» після вакцинації проти COVID-19 [18]. Іншими словами, наявність гуморальної імунної відповіді на вакцину не є тотожною захисту від захворювання.
Багаторічний досвід проведення вакцинопрофілактики свідчить, що у 5–10% щеплених не виникає імунологічної відповіді на вакцину (це так звані ареактивні особи). Ми розрахували відсоток серонегативних осіб серед щеплених ЛЖВ. Із 280 щеплених антитіла були відсутні на момент обстеження у 13 (4,6%), що загалом вкладається у відсоток осіб, які не відповідають виробленням антитіл на будь-яку вакцину. Серед них 2 дози вакцини отримали 12 осіб (92,3%). Всі повністю щеплені отримали останню дозу вакцини не більш ніж за 6 місяців до обстеження. Серед 13 серонегативних ЛЖВ захворіло на COVID-19 три пацієнти, всі – до вакцинації. У двох із трьох захворілих вірусне навантаження ВІЛ було вищим за визначуваний рівень (>40 копій/мл) та рівень CD4 Т-клітин менше за 200 кл/мкл. Відповідно, не захворіло 10 осіб (76,9%). Тобто відсутність імунної відповіді на вакцину не відобразилась на збільшенні рівня захворюваності на COVID-19. Але чому не відбулася імунна відповідь на вакцинні антигени? У 6 із 13 серонегативних щеплених кількість CD4 Т-клітин була менше за 200 кл/мкл, ще у 4 — менше за 500 кл/мкл. Тобто у 10 із 13 (76,9%) серонегативних ЛЖВ був рівень Т-хелперів, який може позначатися на погіршенні імунної відповіді порівняно з ВІЛ-негативними особами. Наші дані узгоджуються із результатами іншого дослідження, в якому вказується, що у ЛЖВ з кількістю CD4 Т-клітин ≥500 кл/мкл відмічалась така сама імунна відповідь на мРНК-вакцини проти COVID-19, як і у ВІЛ-негативних осіб, а у ЛЖВ з кількістю CD4 Т-клітин менше за 200 кл/мкл, вона була гіршою [10]. Згідно з нашими даними, серед серонегативних щеплених пацієнтів у трьох вірусне навантаження ВІЛ було вищим за визначуваний рівень (>40 копій/мл) та рівень CD4 Т-клітин менше за 200 кл/мкл, із них двоє хворіли на COVID-19.
Медіана кількості CD4 Т-клітин у пацієнтів, які перехворіли на COVID-19 склала 568,5 кл/мкл, що не відрізняється від медіани CD4 Т-клітин серед усіх пацієнтів, включених у дослідження загалом (567,5 кл/мкл).
Для оцінки епідеміологічної ефективності вакцинації проти COVID-19 в обстеженій когорті пацієнтів ми зробили такі розрахунки. Підрахували кількість випадків захворювання у щеплених, які відбулися до та після вакцинації. Із загальної кількості щеплених (280) вилучили осіб, які перехворіли до вакцинації (68 осіб). У нас залишилося 212 щеплених, які не хворіли до вакцинації. З них після вакцинації захворіли на COVID-19 85 осіб, не захворіли 127. Із 201 нещепленого ЛЖВ хворіли на COVID-19 79 осіб, не хворіли, відповідно, 122 особи. Для розрахунку зв’язку між вакцинацією та захворюванням на COVID-19 була використана таблиця 4-х полів (табл. 2). Під фактором ризику йдеться про відсутність щеплення як чинника, що може підвищувати ризик захворювання на COVID-19.
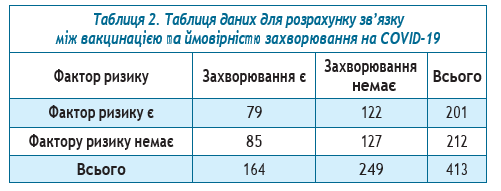
При проведенні розрахунків за допомогою онлайн-калькулятора були отримані такі дані. Критерій хі-квадрат — 0,870, точний критерій Фішера — р>0,05. Сила зв’язку між щепленням та відсутністю захворювання (за критеріями φ, коефіцієнтом сполученості Пірсона, нормоване значення коефіцієнта Пірсона) — несуттєва.
Відомо, що люди можуть хворіти на COVID-19 декілька разів. Дотепер наукового пояснення нетривалого імунного захисту, крім появи нових штамів внаслідок досить швидкої мінливості вірусу немає. На думку деяких авторів [19], варіанти B.1.351 SARS-CoV-2 є частково стійкими до нейтралізації моноклональними антитілами спайкового білка або плазмою реконвалесцентів та сироватками крові від осіб, які отримали вакцини проти COVID-19. На це може вказувати також невідповідність між високим рівнем захисних антитіл в осіб після нещодавнього захворювання (<6 місяців) та поширенням інфекції серед них. Водночас відомі випадки неодноразових захворювань під час циркуляції того самого штаму вірусу. Зокрема, в дослідженні [20] не було виявлено різниці в частоті інфікування між серопозитивними та серонегативними особами (5,2% порівняно з 5,3%), що, на думку авторів, свідчить про відсутність захисного ефекту після попередньої інфекції. Сероепідеміологічне дослідження в бразильському місті Манаус також показало можливість повторного зараження через 6–8 місяців після перенесеної хвороби [21]. Серед обстежених нами пацієнтів два або три рази хворіло на COVID-19 25 осіб (5,2%). Серед щеплених відсоток тих, хто хворів неодноразово склав 6,4%, серед нещеплених — 3,5%. Відповідно, більшість серед тих, хто хворів неодноразово, склали щеплені ЛЖВ – 72%.
Висновки
- Згідно з даними опитування, ЛЖВ хворіли на COVID-19 частіше, ніж населення України загалом. Водночас показники охоплення щепленнями проти COVID-19, навпаки, були вищими. Легкий перебіг хвороби відмічали 94,5% перехворілих на COVID-19 ЛЖВ.
- У 64% нещеплених ЛЖВ були виявлені антитіла до SARS-CoV-2 за відсутності захворювання на COVID-19 в анамнезі, що дозволяє припустити у них безсимптомний перебіг хвороби.
- Імунна відповідь на вакцини проти COVID-19 у ЛЖВ була в межах, що задекларовані виробниками в інструкціях до вакцин (95,4%).
- У 76,9% вакцинованих серонегативних ЛЖВ кількість CD4 Т-клітин була меншою за 500 кл/мкл.
- Встановлено, що не захворіли на COVID-19 (60,7±3,4)% нещеплених ЛЖВ проти (45,4±3,0)% щеплених, (р<0,05).
- Повторні випадки захворювання на COVID-19 відмічали 5,2% обстежених ЛЖВ. Серед щеплених частота повторних випадків була вищою, ніж серед нещеплених (6,4% та 3,5%, відповідно).
- Як показали розрахунки, зв’язок між вакцинацією та ймовірністю захворювання на COVID-19 в обстеженій групі ЛЖВ виявився несуттєвим.
Література
- Vizcarra P., Pérez-Elías M. J., Quereda C. et al. Description of COVID-19 in HIV-infected individuals: a single-centre, prospective Lancet HIV. 2020; 3018:1–11
- Gervasoni C., Meraviglia P., Riva A., Giacomelli A., Oreni L., Minisci D., Atzori C., Ridolfo A., Cattaneo D. Clinical features and outcomes of HIV patients with coronavirus disease. Clin Infect Dis. 2020 Nov. 19; 71(16): 2276–2278. doi: 1093/cid/ciaa579.
- Nomah K., Reyes-Urueña J., Llibre J. M. et al. HIV and SARS-CoV-2 Co-infection: Epidemiological, Clinical Features,and Future Implications for Clinical Care and Public Health for People Living with HIV (PLWH) and HIV Most-at-Risk Groups. Current HIV/AIDS Reports. 2022; 19:17–25. https://doi.org/10.1007/ s11904-021-00596-5;
- Geretti A. M., Stockdale A. J., Kelly S. H. et al. Outcomes of coronavirus disease 2019 (COVID-19) related hospitalization among people with human immunodeiciency virus (HIV) in the ISARIC World Health Organization (WHO) Clinical Characterization Protocol (UK): a prospective observational Clinical Infectious Diseases, Volume 73, Issue 7, 1 October 2021, Pages e2095–e2106, https://doi. org/10.1093/cid/ciaa1605
- Blanco J. L., Ambrosioni J., Garcia F., Martinez E., Soriano A., Mallolas , Miro J. M. COVID-19 in patients with HIV: clinical case series. Lancet HIV. 2020; 7:e314–6;
- Spinelli A., Jones B. L. H., Gandhi M. COVID-19 Outcomes and Risk Factors Among People Living with HIV Current HIV/AIDS Reports. 2022;19:425–432 https://doi.org/10.1007/s11904-022-00618-w;
- Lee W., Yap S. F., Ngeow Y. F., Lye M. S. COVID-19 in People Living with HIV: A Systematic Review and Meta-Analysis. Int J Environ Res Public Health. 2021 Mar 30;18(7):3554. doi: 10.3390/ijerph18073554.
- Wu , Shi Zou, Ming F. et al. Humoral immune response to inactivated COVID-19 vaccination at the 3rd month among people living with HIV. BMC Infect Dis. 2023 Jan 20; 23(1):34. doi: 10.1186/s12879-023-07982-x;
- Frater , Ewer K. J., Ogbe A. et al. Safety and immunogenicity of the ChAdOx1 nCoV-19 (AZD1222) vaccine against SARS-CoV-2 in HIV infection: a single-arm substudy of a phase 2/3 clinical trial. Lancet HIV. 2021 Aug; 8(8):474-485. doi: 10.1016/S2352-3018(21)00103-X. Epub 2021 Jun 18.
- Malin J. J., Suárez I., Biehl L. M. et al. Immune response to mRNA based COVID-19 booster vaccination in people living with HIV. HIV 2023 Mar 8. doi: 10.1111/hiv.13481.
- Yin , Chen Y., Li Y. et al. Immunogenicity and efficacy of COVID-19 vaccines in people living with HIV: a systematic review and meta analysis. Int J Infect Dis. 2022 Nov; 124: 212-223. doi: 10.1016/j. ijid.2022.10.005. Epub 2022 Oct 12;
- Donadeu L., Tiraboschi J. M., Scévola S., Torija A., Meneghini M., Jouve T., Favà A. et al. Long-lasting adaptive immune memory specific to SARS-CoV-2 in convalescent coronavirus disease 2019 stable people with AIDS. 2022 Aug 1;36(10):1373–1382;
- Casado L.,. Vizcarra P., Martín-Colmenarejo S. et al. Lower T cell response against SARS-CoV-2 variants of concern after mRNA vaccine and risk of breakthrough infections in people with HIV. AIDS. 2023 May 1; 37(6): 877–882. doi: 10.1097/ QAD.0000000000003504. Epub 2023 Feb 7.
- Elfil , Negida A. Sampling methods in Clinical Research; an Educational Review. Emerg (Tehran). 2017; 5(1):e52. Epub 2017 Jan 14. PMID: 28286859; PMCID: PMC5325924.
- Perry J., Osman S., Wright J., Richard-Greenblatt M., Buchan S. A., Sadarangani M. et al. Does a humoral correlate of protection exist for SARS-CoV-2? a systematic PloS One 2022;17(4):e0266852. doi: 10.1371/journal.pone.0266852 [PMC free article] [PubMed] [CrossRef] [Google Scholar] [Ref list].
- Wu J., Liang B., Chen C., Wang H., Fang Y., Shen S. et al. SARS-CoV-2 infection induces sustained humoral immune responses in convalescent patients following symptomatic COVID-19. Nat 2021;12(1):1813. doi: 10.1038/s41467-021-22034-1 [PMC free article] [PubMed] [CrossRef] [Google Scholar] [Ref list].
- Krammer , Srivastava K., Alshammary H., Amoako A. et al. Antibody responses in seropositive persons after a single dose of SARS-CoV-2 mRNA vaccine. N Engl J Med 2021; 384:1372-1374DOI: 10.1056/ NEJMc2101667. [PMC free article] [PubMed] [CrossRef] [Google Scholar] [Ref list].
- Des Jarlais C., Weng C. A., Feelemyer J. et al. COVID-19 vaccination and HIV transmission among persons who inject drugs during the first two years of the COVID-19 pandemic in New York City. Harm Reduction Journal, 03 May 2023, 20(1):63 https://doi.org/10.1186/s12954-023-00791-0 PMID: 37138304 PMCID: PMC10156073
- Annapaola Santoro, Andrea Capri, Daniele Petrone et al. SARS-CoV-2 Breakthrough Infections According to the Immune Response Elicited after mRNA Third Dose Vaccination in COVID-19-Naïve Hospital Personnel 2023 Apr 23;11(5):1247. doi: 10.3390/ biomedicines11051247
- Madhi A. et al. Efficacy of the ChAdOx1 nCoV-19 covid-19 vaccine against the B.1.351 variant. N. Engl. J. Med. 2021 doi: 10.1056/ NEJMoa2102214. [PMC free article] [PubMed] [CrossRef] [Google Scholar] [Ref list];
- Shinde et al. Preliminary efficacy of the NVX-CoV2373 Covid-19 vaccine against the B.1.351 variant. medRxiv. 2021 doi: 10.1101/2021.02.25.21252477. [PMC free article] [PubMed] [CrossRef] [Google Scholar] [Ref list];
- Sabino C. et al. Resurgence of COVID-19 in Manaus, Brazil, despite high seroprevalence. Lancet. 2021;397:452–455. [PMC free article] [PubMed] [Google Scholar] [Ref list].
Відомості про авторів:
Шагінян В. Р. — д. м. н., старший науковий співробітник, завідувач відділу діагностики інфекційних та паразитар- них хвороб ДУ «Інститут епідеміології та інфекційних хво- роб ім. Л. В. Громашевського НАМН України», Київ
ORCID: 0000-0002-2746-3414
Фільчаков І. В. — к. м. н., провідний науковий співробіт- ник відділу діагностики інфекційних та паразитарних хвороб ДУ «Інститут епідеміології та інфекційних хвороб ім. Л. В. Громашевського НАМН України»
Сергеєва Т. А. — д. м. н., старший науковий співробітник, завідувач лабораторії епідеміології парентеральних ві- русних гепатитів та ВІЛ-інфекції ДУ «Інститут епідеміоло- гії та інфекційних хвороб ім. Л. В. Громашевського НАМН України»
ORCID: 0000-0001-6488-4042
Кислих О. М. — науковий співробітник лабораторії епі- деміології парентеральних вірусних гепатитів та ВІЛ-ін- фекції ДУ «Інститут епідеміології та інфекційних хвороб ім. Л. В. Громашевського НАМН України».
ORCID: 0009-0003-7387-2109
Максименок О. В. — к. б. н., старший науковий співро- бітник лабораторії епідеміології парентеральних вірусних гепатитів та ВІЛ-інфекції ДУ «Інститут епідеміології та ін- фекційних хвороб ім. Л. В. Громашевського НАМН Украї- ни».
Антоняк С. В. — науковий співробітник відділу вірусних ге- патитів та СНІДу ДУ «Інститут епідеміології та інфекційних хвороб ім. Л. В. Громашевського НАМН України».
Мурашко О. В. — науковий співробітник відділу науко- во-організаційної роботи та міжнародних зв’язків ДУ «Ін- ститут епідеміології та інфекційних хвороб ім. Л. В. Грома- шевського НАМН України».
ORCID: 0009-0005-6980-1249
Information about the authors:
Shaginyan V. R. – Doctor of medicine, senior researcher, head of the department of diagnostics of infectious and parasitic diseases of the State Institution «L. V. Groma- shevsky Institute of Epidemiology and Infectious Diseases of National Academy of Sciences of Ukraine», Kyiv.
ORCID: 0000-0002-2746-3414
Filchakov I. V. – PhD of medicine , leading researcher of the Department of Infectious and Parasitic Diagnosticsof dis- eases of the State Institution «L. V. Gromashevsky Institute of Epidemiology and Infectious Diseases of National Academy of Sciences of Ukraine», Kyiv
Sergeeva T. A. – Doctor of medicine , senior researcher, head of the laboratory of parenteral epidemiologyof viral hepatitis and HIV infection of the State Institution «L. V. Gro- mashevsky Institute of Epidemiology and Infectious Diseas- es of National Academy of Sciences of Ukraine», Kyiv ORCID: 0000-0001-6488-4042
Kislyh O. M. – Researcher of the laboratory of epidemiology of parenteral viral hepatitis and HIV infection of the State Institu- tion «L. V. Gromashevsky Institute of Epidemiology and Infectious Diseases of National Academy of Sciences of Ukraine», Kyiv ORCID: 0009-0003-7387-2109
Maksimenok O. V. – PhD of biological, senior researcher of the laboratory of epidemiology of parenteral viral infections senior researcher of the laboratory of parenteral viral epide- miology of hepatitis and HIV infection of the State Institution
«L. V. Gromashevsky Institute of Epidemiology and Infectious Diseases of National Academy of Sciences of Ukraine», Kyiv
Antonyak S. V. – Researcher at the Department of Viral Hepatitis and AIDS of the State Institution «L. V. Groma- shevsky Institute of Epidemiology and Infectious Diseases of National Academy of Sciences of Ukraine»
Murashko O. V. – Researcher at the Department of Scientific Organizational Work and International Relations of the State Institution «L. V. Gromashevsky Institute of Epidemiology and In- fectious Diseases of National Academy of Sciences of Ukraine». ORCID: 0009-0005-6980-1249